Clear Sky Science · tr
LbuCas13a ile insan hücrelerinde tali RNA kesiminin zamansal dinamikleri
Bir Bakteriyel Savunmayı Hassas Bir Hücre İmha Aracına Dönüştürmek
Araştırmacılar, bir bakteri bağışıklık proteinini insan hücreleri için son derece seçici bir “kendi kendini imha” anahtarına dönüştürmenin bir yolunu keşfettiler. LbuCas13a adlı bir CRISPR enzimi kullanarak, hücre içindeki seçilmiş bir RNA iletisini tanıyıp sonra o hücrenin neredeyse tüm diğer RNA’larını parçalıyorlar. Popüler okuyucu için bu ilgi çekici çünkü RNA iletileri bir hücrenin hangi proteinleri üreteceğini kontrol eder; bunları istenildiğinde silmeyi öğrenmek kanser için yeni tedavilere, antiviral stratejilere ve güçlü araştırma araçlarına kapı açıyor.
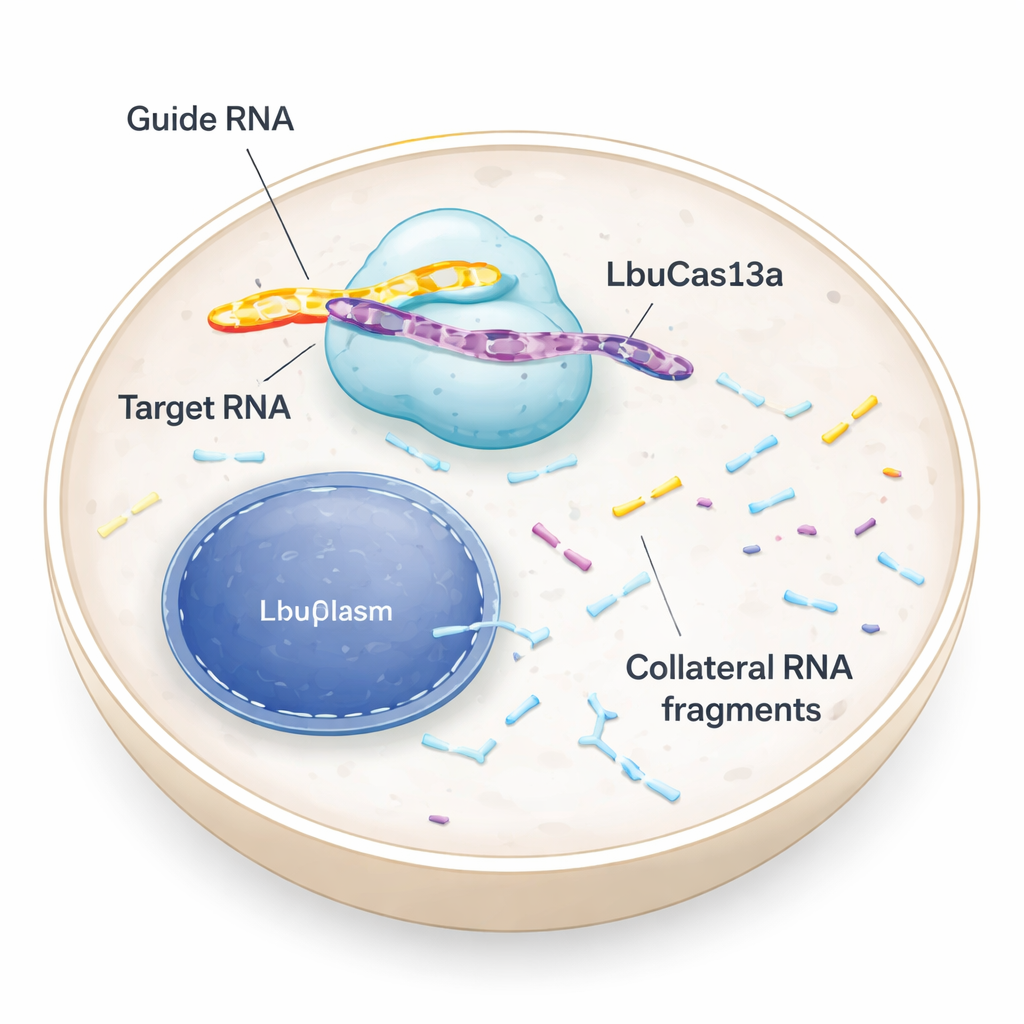
DNA Değil; RNA’yı Hedefleyen Moleküler Makas
Birçok kişi genetik kodu yeniden yazan DNA kesen CRISPR araçlarını duymuştur. LbuCas13a farklıdır: DNA’dan hücrenin protein fabrikalarına talimat taşıyan geçici iletiler olan RNA’yı tanır ve keser. Bakterilerde Cas13 enzimleri antiviral bir savunma parçasıdır. Bir viral RNA’yı fark ettiklerinde yalnızca o istilacıyı dilimlemekle kalmazlar, aynı zamanda etraflarındaki birçok diğer RNA’yı da kesmeye başlarlar. Bu sözde “tali” aktivite enfekte hücreleri dormansa veya ölüme itebilir ve bakteri topluluğunu korumaya yardımcı olur. Hayvan ve insan hücrelerindeki erken testler Cas13’ün tali kesiminin zayıf veya yok olduğunu düşündürdüğünden enzim ağırlıklı olarak hassas bir RNA “kapatıcı” olarak kullanıldı. Yeni çalışma bu varsayımı yeniden ele alıyor ve doğru koşullar altında insan hücrelerinde tali aktivitenin hem güçlü hem de faydalı olabileceğini gösteriyor.
İnsan Hücrelerinde Tali Kesimin Serbest Bırakılması
Takım birkaç Cas13 varyantını karşılaştırdı ve LbuCas13a’nın özellikle güçlü olduğunu buldu. Önceden kısa bir kılavuz RNA ile yüklü saflaştırılmış LbuCas13a proteininin doğrudan insan hücrelerine verildiği, ribonükleoprotein (RNP) teslimatı olarak adlandırılan bir tür moleküler “protein enjeksiyonu” uyguladılar. Kılavuz hedef RNA ile eşleştiğinde—örneğin bir floresan işaretçi geni ya da GAPDH ve 18S ribozomal RNA gibi bol bulunan doğal iletiler—enzim önce o hedefi kesti ve sonra birçok diğer RNA’yı parçalamaya başladı. Yaklaşık 50 dakika içinde hücrenin genel RNA profili dramatik şekilde değişti ve belirgin kesim parçacıkları ortaya çıktı. Bu tali etki farklı teslimat yöntemleriyle ve çeşitli hücre tiplerinde gözlendi; böylece tek bir hücre hattının veya yapay hedefin bir tuhaflığı olmadığı anlaşıldı.
RNA Parçalanmasından Hücre Ölümüne ve Seçime
RNA iletileri aniden kaybolan bir hücrede ne olur? Canlı hücre görüntüleme kullanarak, araştırmacılar hedef RNA’yı ifade eden hücrelerin kademeli olarak apoptoza—hücresel yapının parçalanmasından önce görülen karakteristik “erken uyarı” sinyalleriyle belirgin, düzenli bir programlı hücre ölümü formuna—girdiğini gözlemlediler. Önemli olarak, hedef RNA’yı ifade etmeyen komşu hücreler büyük ölçüde etkilenmedi; bu, kendi kendini imhanın seçici olduğunu gösterdi. Grup daha sonra bu özelliği bir seçim aracı olarak kullandı. Hedef taşıyan hücreleri normal hücrelerle karıştırıp LbuCas13a’yı aktive ettiklerinde hedef hücreler birkaç gün içinde seçici olarak azaldı. Tedaviyi tekrar etmek, bu hücrelerin oranını daha da düşürdü. Başarılı gen düzenlenmiş hücreleri zenginleştirebileceğini gösterdiler ve ayrıca, burada CDK4 olan bir onkogeni aşırı üreten kanser hücrelerini hedef almak için ayarlanabileceğini; bu RNA’yı çok daha az üreten ilişkili hücreleri ise koruyabileceğini gösterdiler.
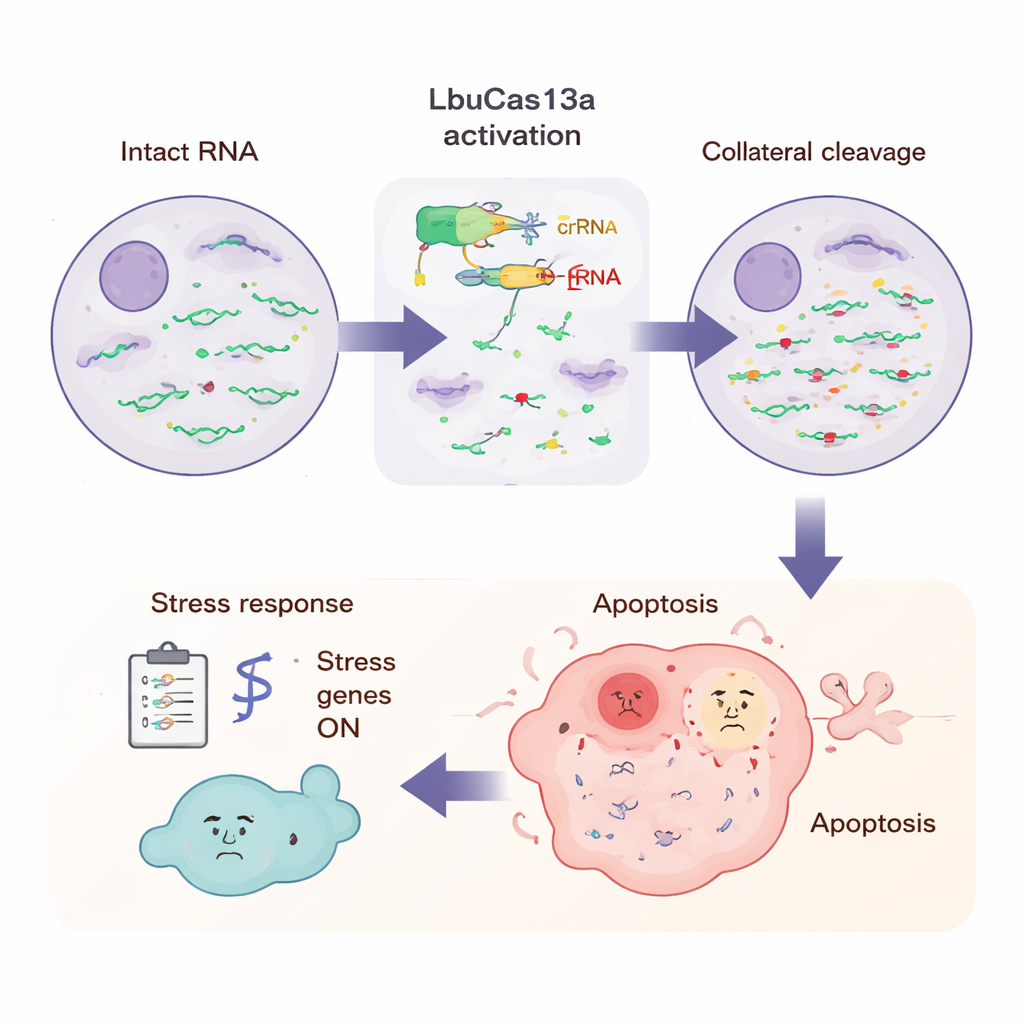
Saldırı Sırasında Hücrenin Deneyimlediği Şey
Büyük resmi görmek için bilim insanları LbuCas13a aktivasyonundan sonra birkaç zaman noktasında hücredeki tüm RNA’ları ölçtüler. Bilinen RNA standartlarını spik-in olarak ekleyerek sitoplazmadaki çoğu protein kodlayan RNA’nın birkaç saat içinde yarıdan fazla azaldığını; buna karşın mitokondriyal iletiler ve bazı nükleer kodlamayan RNA’lar gibi belirli RNA’ların büyük ölçüde korunduğunu tespit ettiler. Uzun okuma dizileme, kesimin tekrar eden, belirli nükleotid pozisyonlarında gerçekleştiğini; genellikle urasil bakımından zengin, esnek loop bölgelerinde olduğunu gösterdi ve bu desenler test tüpü deneylerinde görülenlerle örtüştü. Daha sonraki zaman noktalarında birçok stres ve doğal bağışıklık geni açıldı; iltihap sinyalleri ve antiviral savunmalarla ilişkili genler de dahil. Bu desen, hücrenin aniden ortaya çıkan kırık RNA uçlarını bir viral enfeksiyonu algıladığı gibi algıladığını ve apoptoza yol açan bir alarm programını tetiklediğini düşündürüyor.
Neden Önemli ve Nereye Götürebilir
Basitçe söylemek gerekirse, çalışma LbuCas13a’nın RNA kılavuzlu bir “öldürme anahtarına” dönüştürülebileceğini gösteriyor: bir hücre belirli bir RNA’yı çok fazla üretiyorsa, o RNA’ya karşı LbuCas13a’yı aktive etmek neredeyse genel bir RNA kaybına, bağışıklık benzeri bir alarma ve ardından kontrollü hücre ölümüne yol açıyor. Sürecin hedef RNA’nın bolluğuna güçlü şekilde bağlı olması nedeniyle, belirli kanser hücreleri gibi zararlı genleri aşırı ifade eden hücreleri ortadan kaldırmak veya araştırma ya da hücre tedavisi üretimi sırasında karışık kültürlerde istenmeyen hücreleri temizlemek için kullanılabilir. Aynı zamanda çalışma uyarıcı bir öykü: RNA’yı hedefleyen CRISPR araçlarının güçlü yan etkileri olabilir ve bunların dikkatle yönetilmesi gerekir. Tali RNA kesiminin ne zaman ve nasıl gerçekleştiğini anlamak, Cas13 teknolojilerinin tıp ve biyoteknolojide güvenli kullanımı için esastır.
Atıf: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
Anahtar kelimeler: CRISPR-Cas13, RNA kesimi, hücre ölümü, kanser hedefleme, gen düzenleme araçları