Clear Sky Science · tr
Multimodal yapay zeka ile ERS–CAF immün düzenleyici ekseninin çözümlenmesi ve pan-kanser prognostik ile tedaviye öngörü değeri
Bıçağa Gerek Kalmadan Tümörlere Bakmak
Onkologlar giderek daha fazla, bir tümörü çevreleyen dokunun tümörün kendisi kadar önemli olabileceğini kabul ediyor. Ancak bu gizli mahalleyi tekrarlayan biyopsilerle örneklemek invazivdir ve genellikle pratik değildir. Bu çalışma, yapay zekânın (YZ) rutin tıbbi görüntüleri ve mikroskop görüntülerini okuyarak tümör içindeki zor ölçülen bağışıklık ve skar benzeri süreçleri çıkarabileceğini gösteriyor; böylece günlük görüntülemeyi farklı kanser türlerinde işe yarayan bir tür "dijital biyopsiye" dönüştürebilir.
Kanseri Şekillendiren Gizli Destek Hücreleri
Birçok solid tümör, fibroblast adı verilen uzman destek hücreleri tarafından yapılan sert, lifli bir kabukla sarılıdır. Bu hücreler endoplazmik retikulumda (hücrenin protein fabrikasında) stres altına girdiklerinde, saldırgan ve kanseri destekleyen bir duruma geçerler. Nadir bir kemik kanseri olan kordomada, bu stres altındaki fibroblastlar yoğun bir matriks inşa eder ve bağışıklık hücrelerinin girmesini engelleyerek tedavileri daha az etkili kılar. Benzer fibrotik, bağışıklık açısından fakir ortamlar pankreas ve kolorektal tümörler gibi diğer kanserlerde de gözlenir; bu da bu biyolojinin tek bir hastalığa özgü olmadığını öne sürer. Zorluk, bu stres altındaki fibroblastları ve onların bağışıklığı engelleyen davranışlarını ölçmenin mevcut yollarının doku örneklerine ve kompleks moleküler testlere dayanmasıdır; bunlar tekrarlanması zor ve tümörün önemli bölgelerini kaçırma riski taşır.
Görünmez Biyolojiyi Görmesi İçin YZ'yi Eğitmek
Araştırmacılar, standart ameliyat öncesi MR görüntüleri ve rutin H&E patoloji lamlarının bu stres altındaki fibroblast immün bariyeri hakkında görsel ipuçları içerip içermediğini sordular. Tümör RNA dizilemesinden üç sayısal "referans skoru" oluşturdular: biri fibroblastlardaki stres programının ne kadar aktif olduğunu yakalayan; biri bu hücrelerin immün hücrelere ne kadar güçlü sinyal gönderiyor görünümünü özetleyen; ve biri çevredeki immün ve destek hücre popülasyonlarının ne kadar çeşitli olduğunu tanımlayan. Binlerce geni tahmin etmek yerine, YZ’leri yalnızca görüntülerden bu üç biyolojik olarak anlamlı skoru tahmin edecek şekilde eğitildi. Bunu yapmak için ekip iki dalı birleştirdi: biri MR dokusunun ve şekil özelliklerinin analizine odaklanırken, diğeri dijital slayttaki binlerce küçük bölgeyi tarayıp lifli, immün açıdan fakir dokuya karşı uzman tanımlarına uyan alanlara odaklanmak için dil yönlendirmeli dikkat mekanizması kullandı.
Görüntüleri ve Lamları Birleştirerek Daha Güçlü Sinyaller
Eşleşmiş MR, patoloji lamları, RNA verisi ve izlem bilgisi olan 126 kordoma hastasında, birleşik YZ modeli yalnızca MR veya yalnızca slayt kullanan modellerden daha iyi performans gösterdi. Üç moleküler skorunun tahminleri RNA’ya dayalı ölçümlerle yakından uyuştu ve farklı hastaneler ile tarayıcılar arasında iyi kalibreli kaldı. Patologlar bağımsız olarak fibrotik ve immün‑dışlanmış bölgeleri işaretlediğinde, YZ’nin "sıcak noktaları" genellikle aynı alanlarda aydınlandı; bu da modelin sadece tümör boyutunu değil, gerçek biyolojiyi izlediğini düşündürdü. Model ayrıca prognostik bilgiyi yakaladı: daha yüksek tahmin edilen stres‑fibroblast ve sinyalleşme skorları daha kötü sağkalımla ilişkilendirildi, oysa daha yüksek tahmin edilen mikroçevre çeşitliliği kısmi koruma sağladı. Bu YZ kaynaklı skorların rutin klinik faktörlere eklenmesi, zaman içinde yüksek ve düşük riskli hastaları ayırma yeteneğini artırdı.
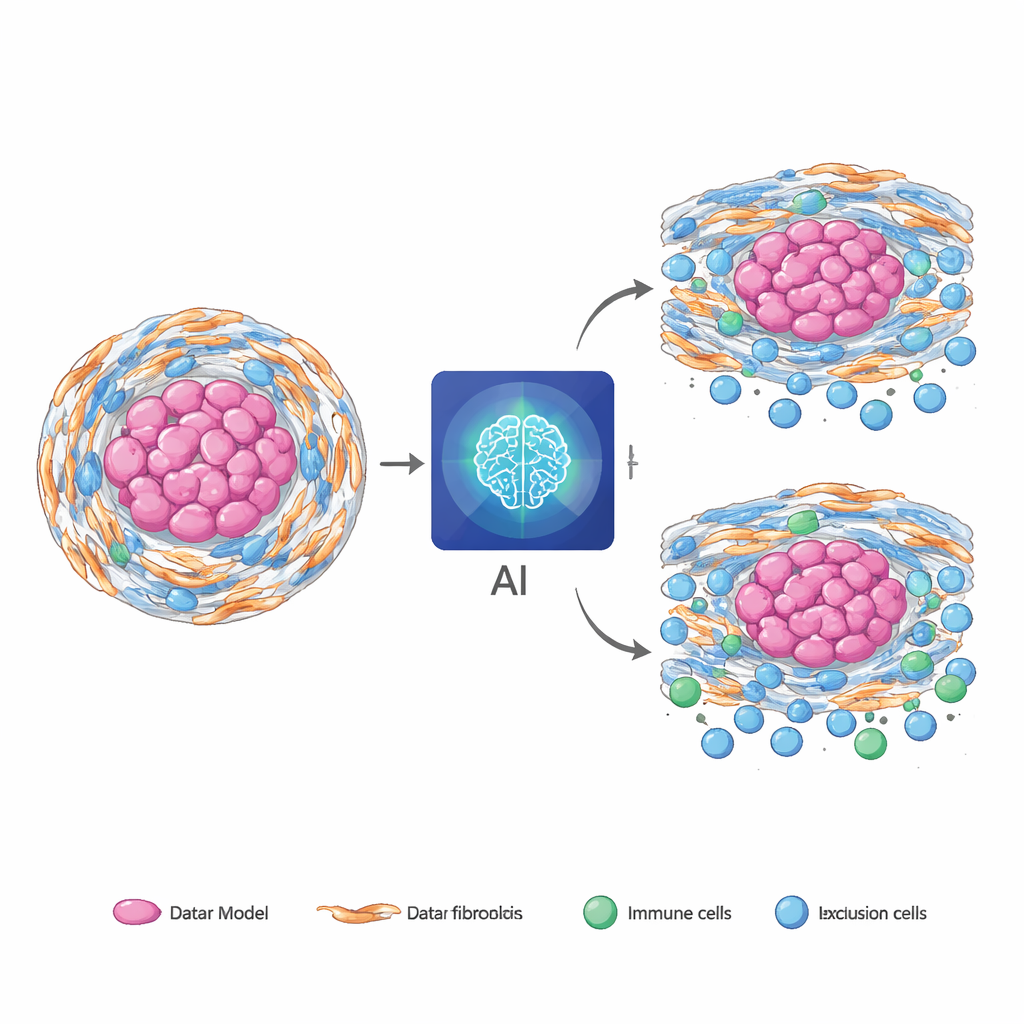
Nadir Tümörlerden Yaygın Kanserlere
Anahtar bir test, tamamen kordomada eğitilmiş bir modelin diğer, daha yaygın kanserlerde "olduğu gibi" kullanılıp kullanılamayacağıydı. Yeniden eğitilmeden büyük kamu veri kümelerinden alınan pankreas, mide ve kolorektal tümörlere uygulandığında, yalnızca slayt sürümü bile görüntü tabanlı tahminleri ile yeni hesaplanmış RNA‑temelli skorlar arasında anlamlı bir uyum gösterdi. Bu kanserlerin bazılarında, YZ skorları hasta sağkalımını standart klinik bilgilerin ötesinde daha iyi tahmin etti ve hangi hastaların kemoterapiden daha fazla yarar görebileceğini ayırt etmeye yardımcı oldu. Dijital patolojinin sınırlı olduğu ortamlarda yöntemi dağıtmayı kolaylaştırmak için ekip, tam multimodal modeli daha hızlı çalışan ve daha az hesaplama gücü kullanan ancak öngörü gücünün çoğunu koruyan yalnızca MR sürümüne dönüştürdü.
Bu Hastalar İçin Ne Anlama Gelebilir
Bir arada değerlendirildiğinde sonuçlar, rutin tıbbi görüntülerin stres altındaki destek hücreleri, immün dışlama ve mikroçevre çeşitliliği hakkında—normalde pahalı moleküler testler gerektiren—bilgiler sessizce kodladığı fikrini destekliyor. Mevcut çalışma geriye dönük olup prospektif doğrulamaya ihtiyaç duysa da, standart bir görüntüleme ve lamın invaziv olmayan şekilde düşmanca, fibrotik bir immün bariyere sahip tümörleri işaretleyebileceği, hangi hastaların ek testler veya hedeflenmiş tedavilerden fayda görebileceğini yönlendirebileceği ve bunu hastalar üzerinde ek bir yük olmadan birden çok kanser türünde yapabileceği bir geleceğe işaret ediyor.
Atıf: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
Anahtar kelimeler: tümör mikroçevresi, kanser görüntüleme, yapay zeka, fibroblastlar, immünoterapi