Clear Sky Science · tr
Sitoloji veya histopatoloji tüm slayt görüntülerini kullanarak malignite ve tümör kökeni tahmini için derin öğrenme
Akciğer ve karın çevresindeki sıvıların neden önemi var
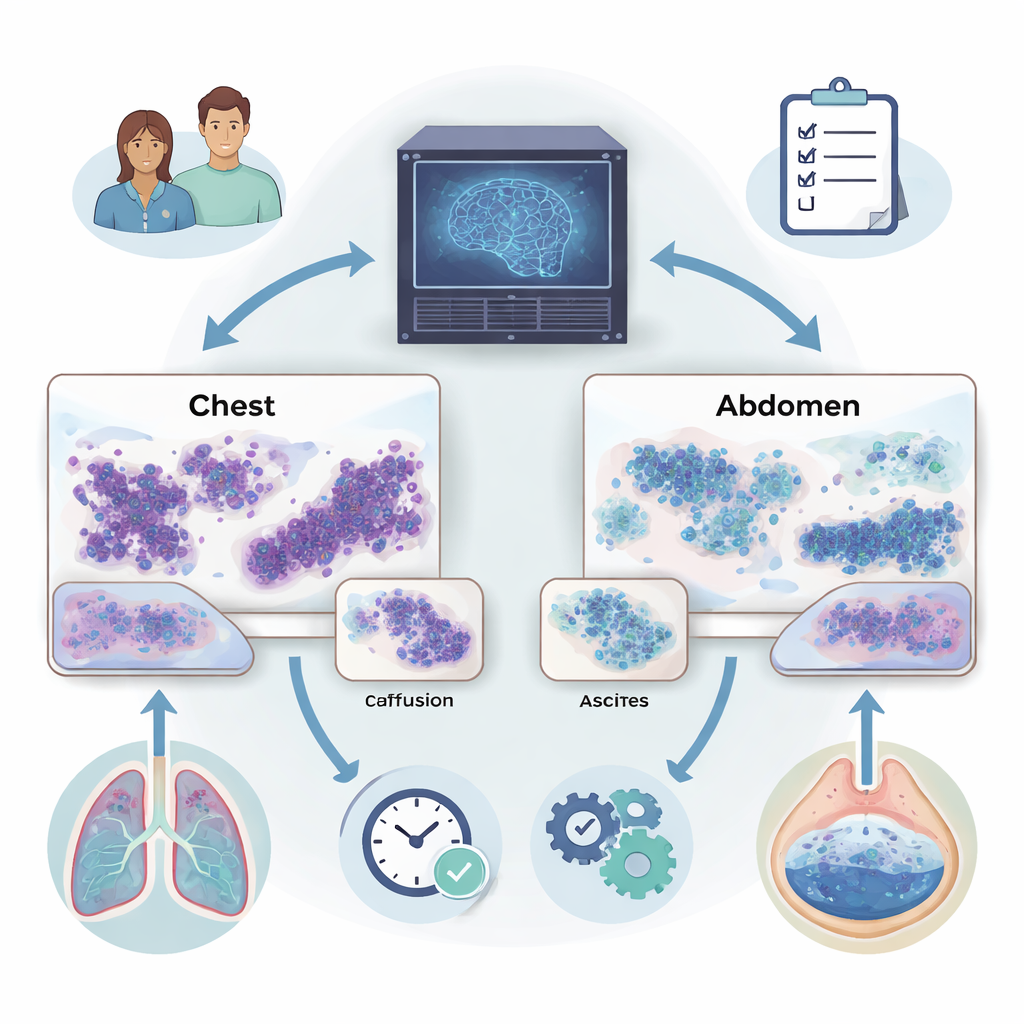
Akciğer çevresinde (plevral efüzyon) veya karın içinde (asit) sıvı birikmesi, kanserin yayılmış olabileceğinin erken bir işareti olabilir. Doktorlar bu sıvıları mikroskop altında kanser hücrelerini aramak için inceler, ancak bu görev zahmetlidir ve uzmanların bile bazen fikir ayrılığı olabilir. Bu çalışma, bu sıvıların tüm dijital slaytlarını tarayabilen, kanser olup olmadığını belirlemeye yardımcı olabilen ve hatta tümörün vücutta muhtemelen nerede başladığına dair öneriler sunabilen yeni bir yapay zeka (YZ) sistemini tanımlıyor.
Mikroskop lamlarını dijital haritalara dönüştürmek
Modern patoloji laboratuvarları cam lamları ultra yüksek çözünürlüklü dijital görüntülere tarayabiliyor; her biri milyonlarca hücre içeriyor. Araştırmacılar bu çalışmada iki tür preparattan elde edilen tüm slayt görüntülerini kullandı: hücrelerin ince “yayma” (smear) preparatları ve küçük doku örneklerini andıran sıkı “hücre blokları” (cell block). İncelemelerini büyük bir hastaneden alınan göğüs ve karın sıvıları ile geniş bir uluslararası kanser veritabanından ek doku örnekleri üzerine odakladılar. Her bir kanser hücresini elle işaretlemek bu ölçekle mümkün olmadığı için ekip, “malign” veya “benign” gibi slayt düzeyi etiketlerden, ayrıntılı anotasyonlara gerek kalmadan öğrenebilen bir yöntem geliştirdi.
Kendini eğiten bir YZ
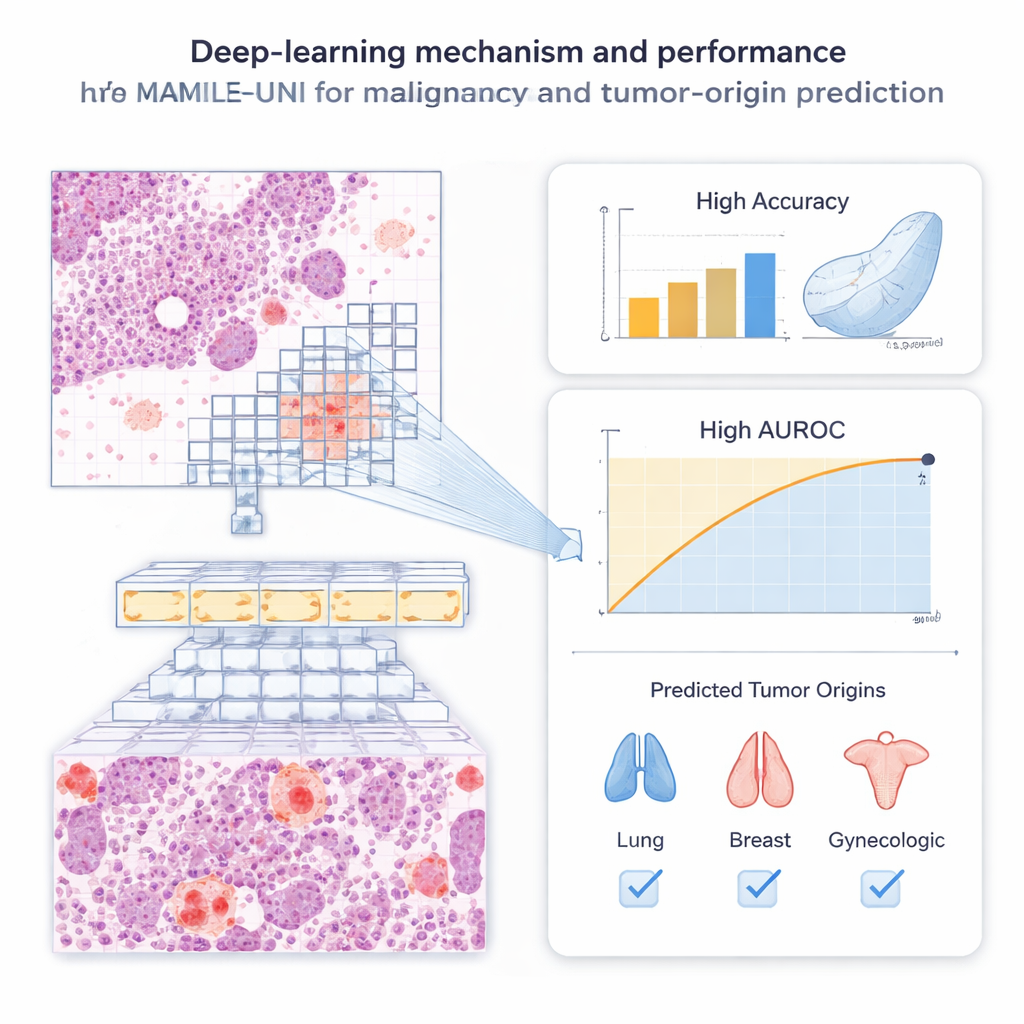
MAMILE‑UNI adını taşıyan sistem iki ana fikri birleştiriyor. Öncelikle, her slaytı birçok küçük görüntü yamalarına (patch) bölüyor ve bunları, milyonlarca patoloji görüntüsü üzerinde insan etiketlerine ihtiyaç duymadan önceden eğitilmiş güçlü bir “transformer” ağına geçiriyor. Bu kendi kendine eğitim adımı, modelin hücre kümeleri ve doku dokuları gibi faydalı görsel desenleri kendi başına keşfetmesine olanak tanıyor. İkinci olarak, bir dikkat (attention) modülü hangi yamaların bir slayt için en önemli olduğunu öğreniyor; bu, bir patologun şüpheli alanları tarama biçimini etkili bir şekilde taklit ediyor. Kararda güçlü etkisi olan yamalar vurgulanıyor ve algoritmanın bir slaytı kanserli veya değil olarak etiketlerken nerelere “baktığını” gösteren ısı haritaları üretiliyor.
Göğüs ve karın sıvılarında kanseri tespit etmek
Ekip, MAMILE‑UNI’yi plevral efüzyonlar ve asitlerden elde edilmiş 1.250 sıvı slayt üzerinde değerlendirdi. Beş önde gelen derin öğrenme yöntemiyle karşılaştırıldığında, yeni sistem tutarlı biçimde daha doğru bulundu. Plevral efüzyonlar için, hem yayma hem de hücre bloklarında malign ile benign slaytları yaklaşık 10 slayttan 9’unda doğru ayırdı. Asit örneklerinde benzer doğruluğa ulaştı ve özellikle hem yüksek duyarlılığı (gerçek kanserleri yakalama) hem de yüksek özgüllüğü (yanlış alarmlardan kaçınma) koruma konusunda güçlüydü. İstatistiksel testler, tahminlerinin gerçek tanılarla yakından uyuştuğunu ve rekabet eden YZ modellerinden anlamlı şekilde daha iyi olduğunu gösterdi. Önemli olarak, sistem bir slaytta kanser hücreleri nadir olduğunda bile güvenilirliğini korudu; bu durum insan okuyucuları sıklıkla zorlar.
Kanserin nereden geldiğini izlemek
Sadece maligniteyi işaretlemenin ötesinde, yazarlar YZ’nin metastatik bir tümörün nerede başladığını çıkarıp çıkaramayacağını da sorguladılar—birincil köken bilinmediğinde büyük bir zorluktur. Plevral efüzyon ve asitlerden elde edilen sitoloji yaymalarını kullanarak model, slaytları akciğer, meme, gastrointestinal kanal veya jinekolojik organlar gibi geniş köken gruplarına atamayı öğrendi. Özellikle akciğer ve meme kanserleri için oldukça doğruydu; daha nadir veya görsel olarak değişken tümörlerde performans daha ılımlıydı. Genelliği test etmek için araştırmacılar MAMILE‑UNI’yi dünya çapında 69 hastaneden 1.196 doku kesitine de uyguladı. Bu histoloji slaytlarında sistem, tümör kökenini belirlemede çarpıcı derecede yüksek doğruluk gösterdi ve gerçek tanılarla neredeyse mükemmele yakın uyum sağladı.
Hız, verim ve klinisyenlere destek
Patologlar genellikle tek bir dijital sitoloji slaydını dikkatle incelemek için en az on dakika harcar. Buna karşılık, MAMILE‑UNI bir slaytı sıkıştırıp gigabayt düzeyindeki görüntüleri kompakt özellik kümelerine dönüştürdükten sonra standart bir grafik kartında iki dakikanın altında işleyip bir tahmin döndürebiliyor. Eğri tabanlı değerlendirmeler, modelin gerçekten malign olan vakaları öncelik sıralamasında genelde üstlere koyma eğiliminde olduğunu, karar eşiklerinde fayda ve zarar arasında uygun bir denge sunduğunu ve olasılık skorlarının gerçek dünya sonuçlarıyla iyi örtüştüğünü gösterdi. Dikkat haritaları uzman patologların işaretlediği alanlarla yakın örtüşme gösterdi; bu da YZ’nin odağının keyfi değil, klinik olarak anlamlı olduğunu öneriyor.
Bu hastalar ve doktorlar için ne anlama geliyor
Göğüs veya karında sıvısı olan hastalar için zamanında ve doğru tanı tedavi kararlarını güçlü biçimde şekillendirir; yine de mevcut testler yavaş, öznel ve maliyetli olabilir. Bu çalışma, dikkatle tasarlanmış bir YZ sisteminin dijital sıvı ve doku slaytlarını güvenilir şekilde tarayabileceğini, kanser belirtilerini tespit edebileceğini ve hastalığın nereden başladığına dair ipuçları sağlayabileceğini; üstelik makul bilgi işlem kaynakları kullanarak gösterebileceğini ortaya koyuyor. Yazarlar, MAMILE‑UNI’nin patologların yerini almak için değil, iş yükünü azaltabilecek, tutarlılığı artırabilecek ve özellikle uzmanlık ve ileri laboratuvar testlerinin sınırlı olduğu ortamlarda yüksek kaliteli kanser tanısına erişimi genişletebilecek bir destek aracı olduğu vurgusunu yapıyorlar.
Atıf: Wang, CW., Chu, TC., Wu, TK. et al. Deep learning for malignancy and tumor origin prediction using cytology or histopathology whole slide images. npj Digit. Med. 9, 175 (2026). https://doi.org/10.1038/s41746-026-02359-1
Anahtar kelimeler: sitoloji AI, plevral efüzyon, asit, tümör kökeni tahmini, dijital patoloji