Clear Sky Science · tr
AXL–SHC1 sinyal ekseni, HER2 anormallikli akciğer ve mide kanserlerinde HER2 hedefli tirozin kinaz inhibitörlerine karşı adaptif direnci aracılık eder
Bazı kanserler yeni ilaçları neden alt eder
Hedefe yönelik kanser ilaçları, tümör büyümesini sürükleyen belirli moleküllere odaklanarak birçok hasta için tedaviyi dönüştürdü. Yine de bu kesin amaçlı ilaçlarla bile tam ve kalıcı remisyonlar nadirdir. Bu çalışma, HER2 adlı bir gen tarafından yönlendirilen akciğer ve mide kanserli kişiler için yakıcı bir soruyu ele alıyor: HER2’yi engelleyen haplarla başlangıçta küçülen tümörler neden hemen hemen her zaman daha sonra nüksü besleyen inatçı bir hücre çekirdeği bırakır — ve hekimler bu kaçış yolunu en başından nasıl kapatabilir?
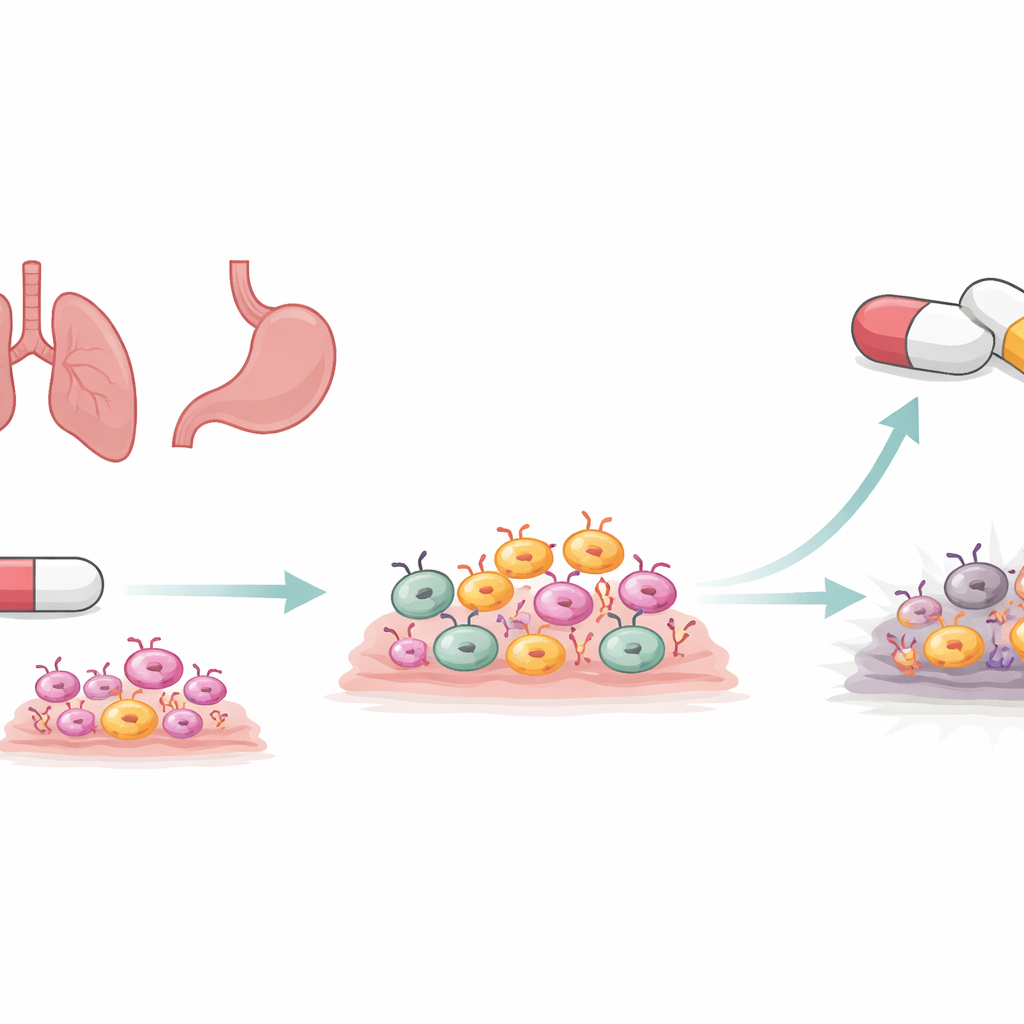
HER2 tarafından yönlendirilen tümörlere daha yakından bakış
HER2, hücrelerin büyümesine ve hayatta kalmasına yardımcı olan bir sinyal merkezidir. Değiştiğinde veya aşırı üretildiğinde meme, mide veya akciğerdeki normal hücreleri kansere dönüştürebilir. Mobocertinib ve benzerleri dahil olmak üzere birkaç modern ilaç, kanser hücrelerindeki HER2’yi kapatmak üzere tasarlanmış tirozin kinaz inhibitörleridir (TKI). Bu ilaçlar tümörleri küçültebilir ve ilerlemeyi geciktirebilir. Ancak akciğer ve mide kanserlerinde faydaları sıklıkla geçicidir. Tümör hücrelerinin küçük bir kısmı başlangıçtaki ilaç saldırısını toleranslı bir durumda atlatmayı başarır ve daha sonra tamamen dirençli tümörlere evrilebilir. Bu hayatta kalan hücrelerin neyin devam etmesini sağladığını anlamak, daha akıllı birinci basamak tedaviler tasarlamak için hayati önemdedir.
AXL adında bir yedek hayat hattı
Araştırmacılar, HER2 değişikliğine sahip akciğer ve mide kanseri hücre hatlarını tarayarak hangi diğer sinyal anahtarlarının hücrelerin HER2 hedefli TKI’lara dayanmasına yardımcı olduğunu incelediler. Bir reseptör olan AXL’i kilit bir oyuncu olarak tanımladılar. Hücreler HER2’yi engelleyen ilaçlara maruz kaldığında, ana HER2 kaynaklı sinyaller zayıflasa bile AXL aktive oldu ve açık kaldı. Bu aktivasyon AKT–mTOR olarak bilinen önemli bir hayatta kalma yolunun çalışmasını sürdürdü. Genetik araçlarla AXL’i susturmak veya deneysel ilaçlarla bloke etmek, kanser hücrelerini bir dizi HER2 hedefli TKI’ya karşı dramatik biçimde daha duyarlı hale getirdi, laboratuvar ortamında hücre büyümesini azalttı ve hücre ölümünü artırdı.
Yardımcı proteinler kaçış yolunu nasıl kuruyor
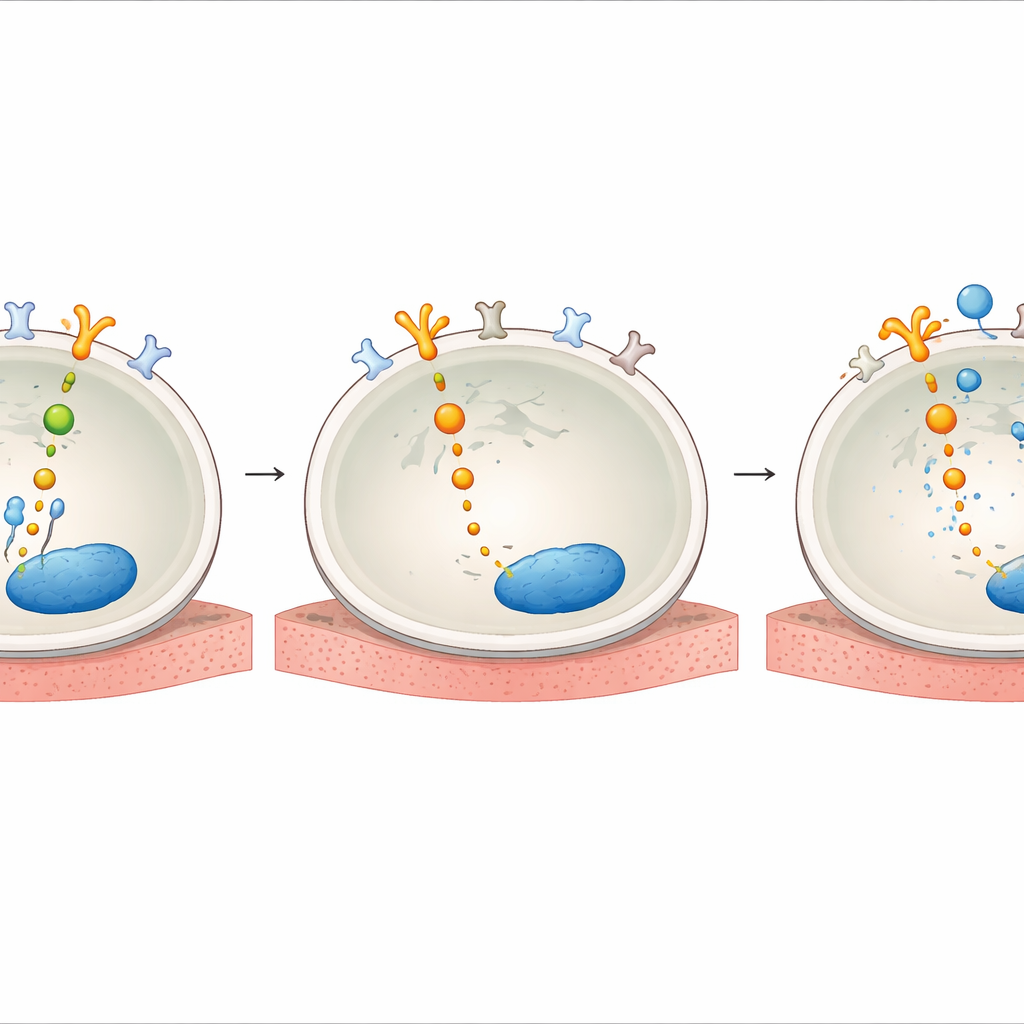
Grup daha sonra AXL’in ilaç baskısı altında nasıl bu kadar etkili hâle geldiğini araştırdı. HER2 TKI’ları ile tedavinin, AXL’i hücre yüzeyinde açan doğal partner molekül GAS6 düzeylerini artırdığını buldular. Ayrıca ilaç maruziyetinden sonra AXL’in fiziksel olarak HER2 ve akrabaları EGFR ile HER3’e bağlanarak HER2’nin normalde kontrol ettiği aynı hayatta kalma devresine etkili biçimde eriştiğini gösterdiler. Hücre içinde SHC1 ve SHCBP1 adlı adaptör proteinleri birer bağlantı merkezi gibi davrandı. HER2 bloke edildiğinde SHC1, SHCBP1’den ayrıldı ve bunun yerine AXL’e bağlandı; SHCBP1 ise çekirdeğe girip hücre döngüsünü ilerletmeye yardımcı oldu. SHC1 veya SHCBP1’i baskılama AKT sinyalini zayıflattı ve hücre hayatta kalmasını azalttı; bu da HER2 inhibe edildiğinde büyümeyi sürdüren bir AXL–SHC1–SHCBP1 eksenini ortaya koydu.
İlaç-tolerant hücreler yerleşmeden önce durdurmak
Araştırmacılar hastalarda olanı taklit etmek için mobocertinib varlığında günlerce kanser hücrelerinin büyümesine izin verip ilacı tolere eden küçük bir popülasyonu seçtiler. Bu ilaç-tolerant hücreler yavaş büyüdü ancak orijinal hücrelere kıyasla HER2 inhibitörüne belirgin şekilde daha az duyarlıydı. Hayatta kalmaları hâlâ büyük ölçüde AXL’e bağlıydı: bir AXL blokeri eklemek büyümelerini keskin biçimde azalttı ve AKT aktivitesini düşürdü. AXL-pozitif, HER2 değişikliğine sahip akciğer tümörlerini taşıyan fare modellerinde mobocertinib ile bir AXL inhibitörünün kombinasyonu tümörleri daha çok küçülttü, bölünen hücreleri azalttı ve HER2 ilacı tek başına verildiğine kıyasla programlanmış hücre ölümünün işaretlerini artırdı — ek toksisite olmadan. AXL’i aşırı üreten şekilde tasarlanmış tümörler mobocertinib’e tek başına belirgin derecede daha az yanıt verdi, ancak AXL inhibitörü eklendiğinde yine yanıt verdiler.
Gelecek tedaviler için bunun anlamı ne olabilir
Önemli olarak, HER2 değişikliğine sahip akciğer ve mide kanserli hastalardan alınan doku örnekleri, yaklaşık dörtte birinde yüksek AXL düzeyleri olduğunu ve çoğunda en azından bir miktar AXL bulunduğunu ortaya koydu. Bu, hastaların hatırı sayılır bir grubunun direnç ortaya çıkmasını beklemek yerine baştan bir HER2 hedefli TKI ile AXL inhibitörünü eşleştiren bir tedavi stratejisinden yararlanabileceğini düşündürür. Basitçe söylemek gerekirse, çalışma birçok HER2 kaynaklı tümörün yedek bir büyüme anahtarı — AXL’i — bekleme modunda tuttuğunu gösteriyor. HER2 bloke edildiğinde AXL devreye girer ve kanser hücrelerini yaşatmaya devam eder. Her iki anahtarı aynı anda kapatmak çok daha fazla kanser hücresinin ölümüne yol açar ve ilaç-tolerant hayatta kalanların ortaya çıkmasını yavaşlatır veya önler. Klinik denemelerde doğrulanırsa, bu çift hedefli yaklaşım HER2 değişikliğine sahip akciğer ve mide kanserlerinin daha uzun süre kontrol altında tutulmasını sağlayabilir.
Atıf: Ishida, M., Yamada, T., Katayama, Y. et al. AXL–SHC1 signaling axis mediates adaptive resistance to HER2-targeted tyrosine kinase inhibitors in HER2-aberrant lung and gastric cancers. npj Precis. Onc. 10, 142 (2026). https://doi.org/10.1038/s41698-026-01385-2
Anahtar kelimeler: HER2 hedefli tedavi, AXL inhibitörü, ilaç direnci, akciğer kanseri, mide kanseri