Clear Sky Science · tr
WHO 2021 glioma alt tiplerinin belirlenmesi için patoloji ve radyoloji temel modellerinin multimodal füzyonu
Beyin Tümörüne İlişkin İki Görünümü Bir Araya Getirmek
Bir kişiye beyin tümörü teşhisi konduğunda, doktorların yalnızca tümörün varlığını bilmesi yetmez; tümörün tam olarak hangi tür olduğu da bilinmelidir. Farklı tümör türleri cerrahi, radyasyon ve ilaçlara çok farklı yanıt verir. Bugün bu ayrıntılı “alt tip belirleme” genellikle yavaş, maliyetli ve her yerde erişilebilir olmayan genetik testler gerektirir. Bu çalışma, hem beyin görüntülerine hem de tümör dokusunun mikroskop görüntülerine bakan akıllı bir bilgisayar sisteminin bu alt tipleri güvenilir şekilde çıkarıp çıkaramayacağını, böylece kesin tedaviye erişimi hızlandırıp genişletebileceğini araştırıyor.
Tümör Türünün Neden Önemi Var
Yetişkin diffüz gliomlar en ölümcül beyin kanserleri arasında yer alır, ancak genellikle standart görüntülerde ve mikroskop altında benzer görünürler. Güncel kılavuzlar bunları agresiflikleri ve hastaların yaşam süresi açısından büyük ölçüde farklılık gösteren üç genetik alt tipe ayırır. Bu alt tipleri ayırt etmenin güncel altın standardı tümör DNA’sının moleküler testlerine dayanır. Bu testler ek doku, uzman laboratuvarlar ve günler ila haftalar süren bekleme gerektirir. Yazarlar, rutin olarak toplanan manyetik rezonans görüntüleme (MRI) ve dijital patoloji slaytlarının, bu genetik incelemelerin bir kısmının yerine geçecek kadar bilgi sunup sunmayacağını soruyorlar.
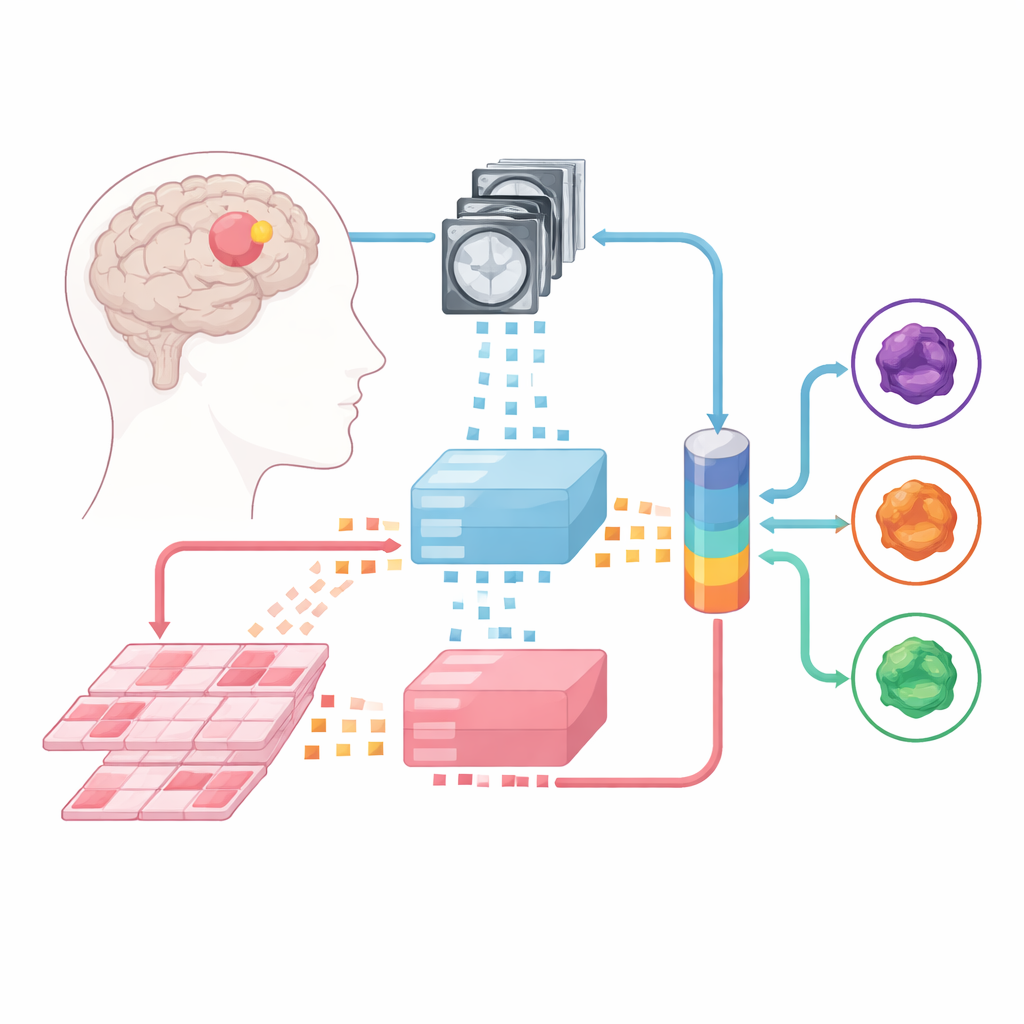
Makinelere Görüntüleri ve Slaytları Okutmak
Ekip, önceden devasa tıbbi görüntü koleksiyonları üzerinde eğitilmiş güçlü görüntü çözücüler olan büyük “temel modeller” üzerine inşa etti. Bu modellerden biri çok parametreli MR görüntülerini, diğeri ise tümör dokusundan elde edilen yüksek çözünürlüklü patoloji slaytlarını işler. Her vaka küçük görüntü yamalarına bölünür ve temel modeller bu yamaları sayısal parmak izlerine dönüştürür. Bu sabit “uzmanların” üzerine araştırmacılar, MRI ile patoloji bilgisini birleştirmeyi öğrenen üç tür füzyon modeli eğittiler: geç füzyon (late-fusion), erken füzyon (early-fusion) ve her kaynağa ne kadar güvenileceğine dinamik olarak karar verebilen daha esnek bir uzman karışımı (mixture-of-experts) mimarisi.
Hastaları Eşleştirmeden Modları Karıştırmak
Böyle multimodal yöntemler için pratik bir engel, hastanelerde nadiren her hastaya ait hem MRI hem de patoloji görüntülerinin eksiksiz ve eşleştirilmiş büyük veri kümelerinin bulunmasıdır. Kusursuz eşleştirilmiş verilere güvenmek yerine, yazarlar ayrı koleksiyonlar bir araya getirdiler: birkaç merkezden yüzlerce MRI vakası ve başka bir kaynaktan yüzlerce patoloji vakası ile her iki görüntüye de sahip olan 171 hastalık daha küçük bir kamu kanser projesi seti. Eğitim sırasında, tümörler aynı alt tipe ait olduğu sürece bir kişinin MRI’sını başka bir kişinin patoloji slaytı ile eşleştirdiler. Şaşırtıcı şekilde, böyle “eşleştirilmemiş” verilerle eğitilen modeller, gerçek hasta eşleştirmeleriyle eğitilenler kadar iyi performans gösterdi ve iki ayrı tek-modallik modelin basitçe ortalamasından açıkça daha iyiydi.
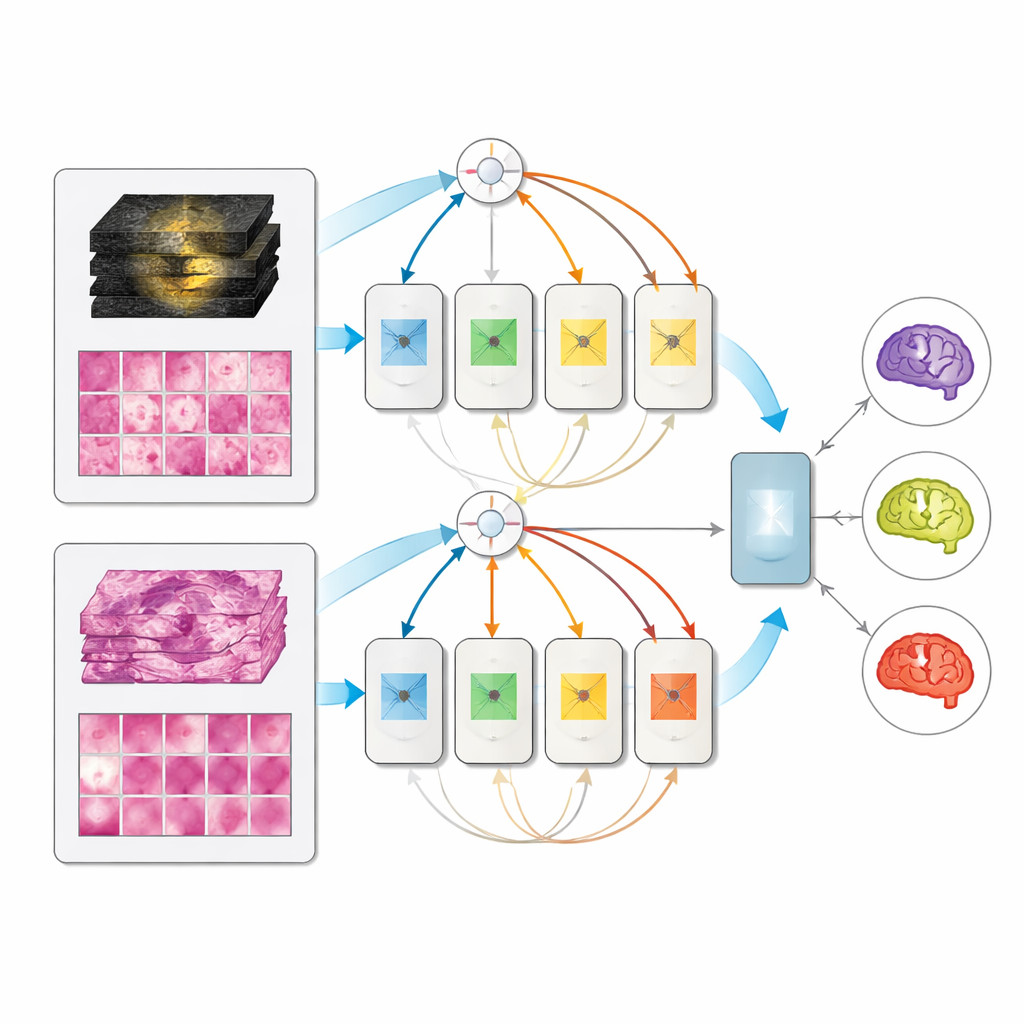
Mevcut Olanla Uyarlanan Tek Bir Model
Tam olarak karakterize edilmiş 171 hastalık ayrılmış test setinde, tüm multimodal modeller tek girdili muadillerini yendi ve uzman karışımı tasarım en iyi performansı göstererek üç alt tipi ayırmada çok yüksek skorlar elde etti. Dikkate değer olarak, test sırasında yalnızca MRI veya yalnızca patoloji sağlandığında multimodal model çökmüyordu; adanmış tek-modallik modeller kadar iyi performans gösteriyordu. Bu, bir kliniğin her senaryo için ayrı araçlar bulundurmak yerine mevcut bilgiye göre çalışan tek bir birleşik sistemi devreye alabileceği anlamına geliyor—sadece ameliyat öncesi taramalar, sadece ameliyat sonrası doku ya da her ikisi birlikte.
Modelin Ne Gördüğünü Görmek
Sistemin kararlarına güven oluşturmak için araştırmacılar modelin “nereye baktığını” ve hangi görüntü özelliklerinin en önemli olduğunu incelediler. Dikkat haritaları, ortak modelin dikkatini hem MRI’de hem de doku slaytlarında tümör ve çevresine daha geniş biçimde yaydığını ve daha yaygın dikkatin genellikle doğru tahminlerle örtüştüğünü gösterdi. Öğrenilen özelliklerin daha derin analizi, bilinen tıbbi ipuçlarıyla uyumlu desenler ortaya koydu: örneğin, kontrast tutan tümör çekirdeklerini ve bozulmuş sıvı boşluklarını vurgulayan MRI özellikleri daha agresif tümörleri ayırmaya yardımcı olurken, klasik hücre şekilleri ve dokularını yakalayan doku özellikleri belirli glioma alt tiplerini tanımada fayda sağladı. İlginç boşluklar da ortaya çıktı: model en agresif tümörlerin bazı ders kitabı işaretlerini güçlü biçimde kodlamıyordu; bu da modelin bu grubu, daha elverişli bir alt tipe dair güçlü kanıt yoksa genellikle bir “varsayılan” olarak ele aldığını destekliyor.
Bu Hastalar İçin Ne Anlama Gelebilir
Düz bir ifadeyle, bu çalışma beyin taramaları ile mikroskop görüntülerini birleştiren bir yapay zekâ sisteminin yalnızca tek tür görüntüye bakan sistemlerden daha isabetli tümör sınıflaması yapabildiğini ve iki görüntü türü aynı hastalardan gelmediğinde bile eğitilebileceğini gösteriyor. Daha büyük ve daha çeşitli gruplarda daha fazla doğrulandığında, bu tür araçlar genetik testlerin sınırlı olduğu ortamlarda doktorların tümör alt tipini daha erken ve daha yaygın tahmin etmesine yardımcı olabilir. Moleküler testlerin yerini almasalar da, cerrahlar ve onkologları en olası tanıya ve en uygun tedavi yoluna yönlendiren hızlı, düşük maliyetli rehberler olarak işlev görebilirler.
Atıf: Saueressig, C., Scholz, D., Raffler, P. et al. Multimodal fusion of pathology and radiology foundation models for WHO 2021 glioma subtyping. npj Precis. Onc. 10, 118 (2026). https://doi.org/10.1038/s41698-026-01366-5
Anahtar kelimeler: glioma alt tip belirleme, multimodal görüntüleme, yapay zeka, MRI ve patoloji, beyin kanseri tanısı