Clear Sky Science · tr
Midostaurin yanıtı AML’de, SMAC taklitçileri tarafından seçici olarak hedeflenen progenitör-benzeri hücre durumu tarafından şekillendirilir
Neden bazı lösemi ilaçları etkisini yitirir?
Akut myeloid lösemi (AML) adlı bir kan kanseri türüyle yaşayan birçok kişi için yeni hedefe yönelik ilaçlar umut getirdi—ancak herkes fayda görmüyor ve yanıtlar sıklıkla zamanla zayıflıyor. Bu çalışma basit ama kritik bir soruyu soruyor: neden bazı lösemi hücreleri yaygın kullanılan midostaurin ilacını görmezden gelir ve bu inatçı hücreleri öldürmeye zorlayacak akıllı bir kombinasyon bulabilir miyiz?
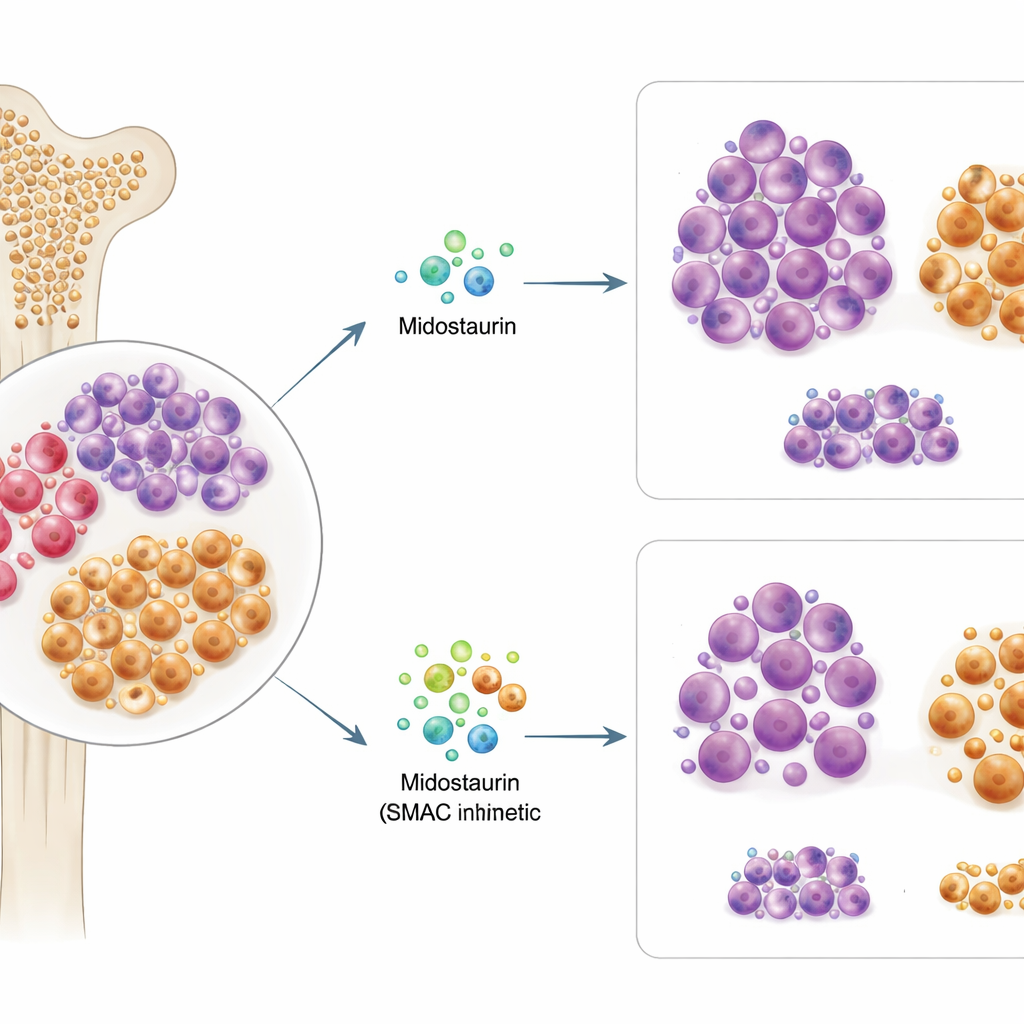
Ana mutasyonun ötesine bakmak
Yaklaşık her üç AML hastasından biri, löseminin büyümesini yönlendiren ve midostaurin reçete edilme nedenlerinden biri olan FLT3 adlı genin bir değişikliğini taşır. Araştırmacılar, FLT3‑mutasyonlu 63 hastadan alınan kemik iliği ve kan örneklerini laboratuvarda midostaurin ve 500’den fazla diğer kanser ilacına maruz bıraktı. Bir hastanın hücrelerinin ex vivo midostaurine ne kadar duyarlı olduğu, o hastanın daha sonra klinikte nasıl yanıt verdiğiyle yakından eşleşti. Sürpriz olarak, FLT3 mutasyonunun tam türü veya bolluğu midostaurin başarısını güvenilir biçimde öngörmedi; bu da yalnızca genetiğin kimin fayda göreceğini açıklamakta yetersiz olduğunu gösteriyor.
Gizli, inatçı bir “tohum” havuzu
Daha derine indiklerinde, ekip midostaurin‑duyarlı olanlarla olmayanlar arasındaki protein ve gen etkinliği desenlerini karşılaştırdı. Yanıt vermeyen örnekler, kan oluşumunun köküne daha yakın ve löseminin yeniden başlamasına neden olabilecek “tohum” görevi gören olgunlaşmamış, kök‑benzeri progenitör hücre özellikleri bakımından zengindi. Buna karşın yanıt veren örnekler kısmen olgunlaşmış bağışıklık ve myeloid hücrelere daha çok benziyordu. İleri tek hücre yöntemleri kullanarak, bilim insanları yüzey proteinleri CD38 ve CD45RA ile işaretlenmiş ve bu progenitör‑benzeri tohumlar gibi davranan belirli bir lösemi hücresi popülasyonunu tanımladı. Bu hücreler dış zarlarının sıra dışı bir örgülenmesini gösteriyordu; bu da hayatta kalmayı destekleyen anahtar sinyal moleküllerinin belirli şekillerde düzenlenmiş olabileceğine işaret ediyordu.
Hayatta kalma devresi: sinyal yollarında bir anahtar değişimi
Midostaurin, normalde STAT5 adlı bir molekülü de içeren ve hücre büyümesini teşvik eden bir sinyal zincirini besleyen FLT3 sinyalini bloke edecek şekilde tasarlanmıştır. Ekip, hücre hatlarında ve hasta örneklerinde midostaurin tedavisinden sonra sinyallemeyi incelediğinde iki farklı desen gördü. Midostaurin‑duyarlı hücrelerde STAT5 aktivitesi hızla düştü; bu, etkili bir FLT3 kapanışına uygundu. Ancak dirençli hücrelerde baskın olan başka bir yol vardı: PI3K/AKT, hücrelerin öldürülmeye direnmelerine yardımcı olan klasik bir hayatta kalma rotası. Bu dirençli hücreler tedaviden sonra AKT aktivitesini korudu veya artırdı ve apoptozu (programlı hücre ölümü) engelleyen protein düzeyleri daha yüksekti. Başka bir deyişle, bu progenitör‑benzeri hücrelerin içindeki devreler, FLT3 engellendiğinde bile hayatta kalmayı destekleyecek şekilde yeniden yönlendirilmiş görünüyordu.
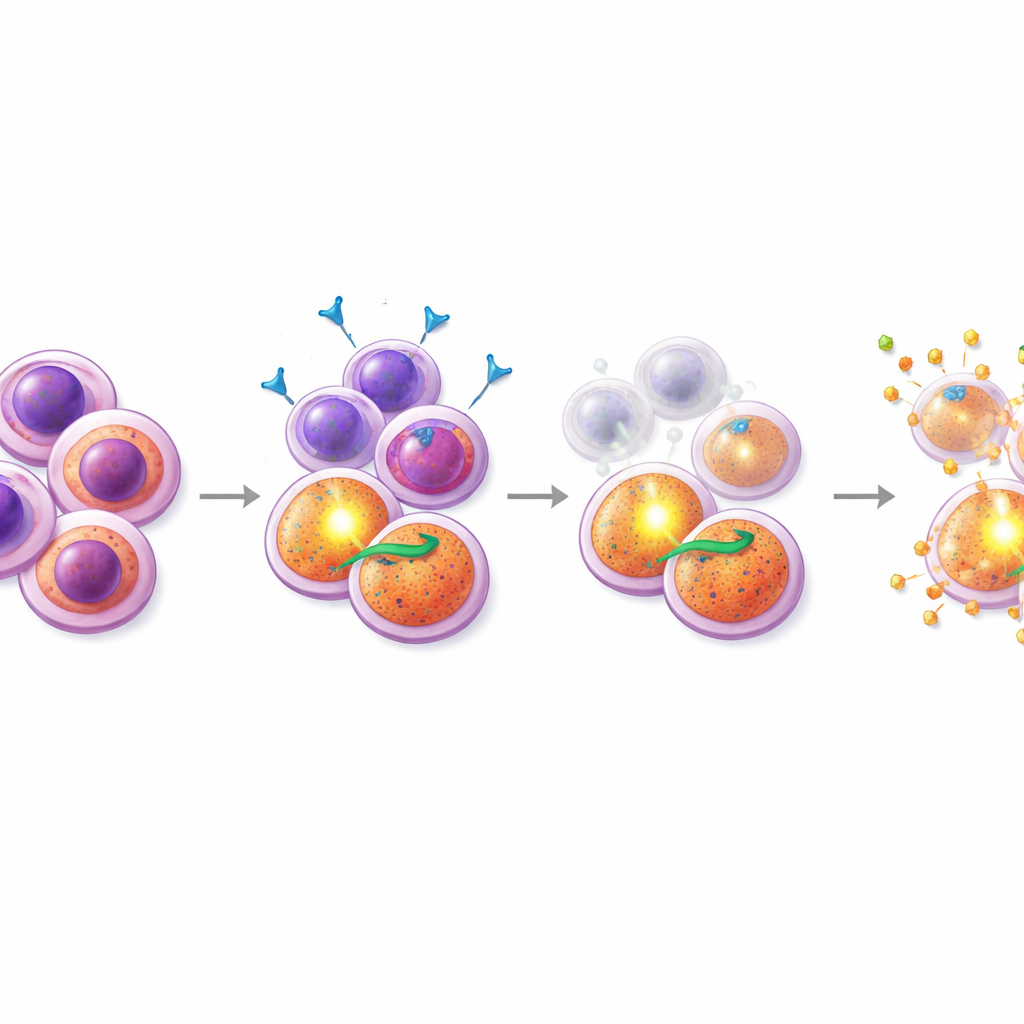
Zayıf noktayı hedefleyen eşlikçi ilaç bulmak
Bu içgörüyle donanmış olarak, araştırmacılar midostaurini yüzlerce diğer bileşikle kombinasyon halinde taradı; odak noktası hücre ölümü üzerinde etkili ilaçlardı. Öne çıkan bir grup SMAC taklitçileri oldu; bu ilaçlar PI3K/AKT‑yönlendirmeli hücrelerin dayandığı “apoptozu inhibe eden” proteinleri devre dışı bırakıyor. Dirençli hasta örneklerinde ve dirençli bir FLT3‑Mutant hücre hattında, birinapant gibi SMAC taklitçilerinin midostaurine eklenmesi güçlü bir sinerji üretti: birlikte, ilaçlar tek başlarına olduğundan çok daha fazla hücreyi öldürdü. Kritik olarak, ayrıntılı akış sitometri deneyleri midostaurin–SMAC taklitçi kombinasyonunun CD38+CD45RA+ progenitör‑benzeri popülasyonu seçici olarak azalttığını ve karakteristik yüzey belirteç düzeylerini düşürdüğünü gösterdi; bu, bu tedavinin zor öldürülen tohumları özgül olarak hedeflediğini düşündürüyor. Buna karşılık onaylı BCL‑2 inhibitörü venetoklaks ile yapılan kombinasyonlar farklı, CD34‑yüksek bir alt kümeye karşı daha etkiliydi ve dirençli hücreler üzerinde aynı odaklanmış etkiyi göstermedi.
Hastalar için ne anlama geliyor?
Bu çalışma, midostaurin direncinin yalnızca FLT3 mutasyonuyla ilgili olmadığını, aynı zamanda lösemi hücrelerinin “durumu”—olgunluk düzeyleri, zar organizasyonu ve tercih ettikleri hayatta kalma yolları—ile de bağlantılı olduğunu öne sürüyor. Progenitör‑benzeri CD38+CD45RA+ alt kümesi, direncin önemli bir rezervuarı gibi görünüyor; sinyalleşmesini sıradan STAT5 rotasından hayatta kalmayı kolaylaştıran PI3K/AKT programına kaydırıyor. Midostaurini SMAC taklitçileriyle eşleştirerek, araştırmacılar bu hücreleri yeniden duyarlı hale getirebildi ve laboratuvarda hücre ölümü yönünde ilerlettiler. Daha büyük klinik çalışmalar hâlâ gerekli olmakla birlikte, bulgular doktorların yalnızca DNA dizilemesi değil, aynı zamanda fonksiyonel testler ve hücre‑durumu profillemesi kullanarak hem kütle lösemiyi hem de en dayanıklı tohumları kesen FLT3‑hedefli kombinasyonları seçebileceği bir geleceğe işaret ediyor.
Atıf: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
Anahtar kelimeler: akut myeloid lösemi, FLT3 inhibitörleri, ilaç direnci, lösemik kök hücreler, SMAC taklitçileri