Clear Sky Science · tr
Bilgisayarlı tomografi tabanlı bir temel model kullanarak homolog rekombinasyon yetmezliğini ve tedavi yanıtlarını tahmin etmek: preklinik bir çalışma
Hastalar ve hekimler için neden önemli
Bazı kemoterapiler ve yeni hedefe yönelik ilaçlar gibi DNA’ya zarar veren kanser tedavileri, onarım sistemleri zaten bozuk olan tümörlerde olağanüstü etkili olabilir. Zorluk, hangi tümörlerin bu gizli zayıflıklara sahip olduğunu, tekrarlayan invaziv biyopsilere başvurmadan saptamaktır. Bu çalışma, farelerde rutinde kullanılan tıbbi taramaların güçlü bir yapay zeka modeli tarafından yorumlanmasının tümörün ne kadar savunmasız olduğunu ve deneysel bir ilaca nasıl yanıt vereceğini ortaya koyup koymayacağını araştırıyor.
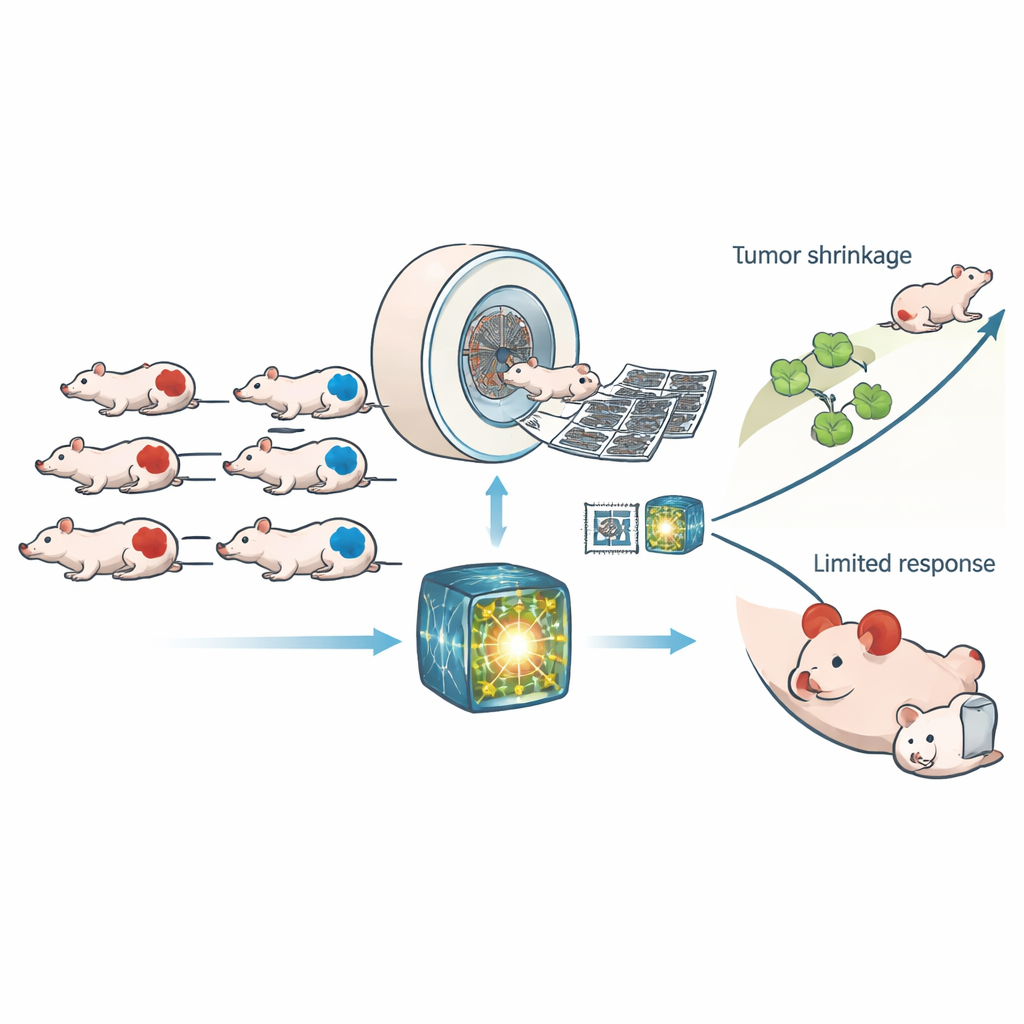
Kanser hücrelerindeki gizli bir zaaf
Birçok tümörde homolog rekombinasyon adı verilen önemli bir DNA onarım yolunda kusurlar bulunur. Bu yol başarısız olduğunda hücreler genetik materyallerinde hasar biriktirir; bu duruma homolog rekombinasyon yetmezliği (HRD) denir. HRD kanserlerin oluşma olasılığını artırabilir, ancak aynı zamanda bir Achilles topuğu haline gelir: DNA’ya daha fazla zarar veren ilaçlar, zaten baskı altında olan bu hücreleri sağlıklı hücrelerden daha etkili biçimde öldürebilir. Günümüzde HRD’yi belirlemek genellikle pahalı, zaman alan ve sıklıkla tümörden doku alınmasını gerektiren genetik testlere veya özel laboratuvar testlerine dayanıyor. Yazarlar, üç boyutlu X‑ray taramaları olan görüntülemenin kliniklerde yaygın kullanılan bu tip taramalarının HRD hakkında hızlı ve invazif olmayan bir pencere sunup sunmayacağını sordular.
Daha fazla biyopsi yerine akıllı taramalar kullanmak
Araştırmacılar, onarım yeteneği ya HRD olan ya da normal olan insan tümör greftleri taşıyan 307 fareyle çalıştı. Tüm hayvanlar kontrol tedavisinden veya tümörlerin düşük oksijenli bölgelerinde aktive olan ve DNA zincirlerini çapraz bağlayan deneysel bir ilaç olan CP‑506’dan birini almadan önce ve sonra yüksek çözünürlüklü bilgisayarlı tomografi (BT) taramalarından geçti. Bir avuç el yapımı görüntü ölçümüne dayanmak yerine ekip, her taramadan binlerce ince deseni çıkarmak için büyük insan BT veri kümeleri üzerinde eğitilmiş modern bir “temel model” kullandı. Basit bir sınıflandırıcı daha sonra bu desenler üzerinde tümörün HRD olup olmadığına karar vermek üzere eğitildi ve aynı öğrenilmiş özellikler CP‑506’nın ne kadar DNA hasarı ve büyüme gecikmesi oluşturacağını tahmin etmek için yeniden kullanıldı.
Görüntüleme modelinin performansı
Temel model, geleneksel radyomik ve sıfırdan eğitilmiş standart bir derin öğrenme ağından açıkça daha iyi performans gösterdi. Yeni test taramalarında HRD’yi HRD olmayan tümörlerden yaklaşık 0,88 civarında bir eğri altı alan (AUC) ile ayırt etti; bu doğruluk seviyesi farklı BT enerji ayarlarında da korunuyordu. Yapay zekâ yaklaşımlarının her ikisi de tümör tipinde aynı görüşe vardığında performans daha da yükseldi. Modelin görüntü tabanlı HRD skoru, birkaç prostat ve kolorektal tümör hattında gerçek genetik durumla yakından uyuştu; ancak olağandışı onarım davranışı gösteren bir hat sınıflandırılması daha zor kaldı. Önemli olarak, HRD ile bağlantılı BT özellikleri yalnızca istatistiksel artefaktlar değildi: tedaviden 48 saat sonra CP‑506’nın oluşturduğu kalıcı DNA hasarının miktarını ve paralel bir deneyde tümörlerin dört katına ulaşmasının ne kadar sürdüğünü de öngördüler.
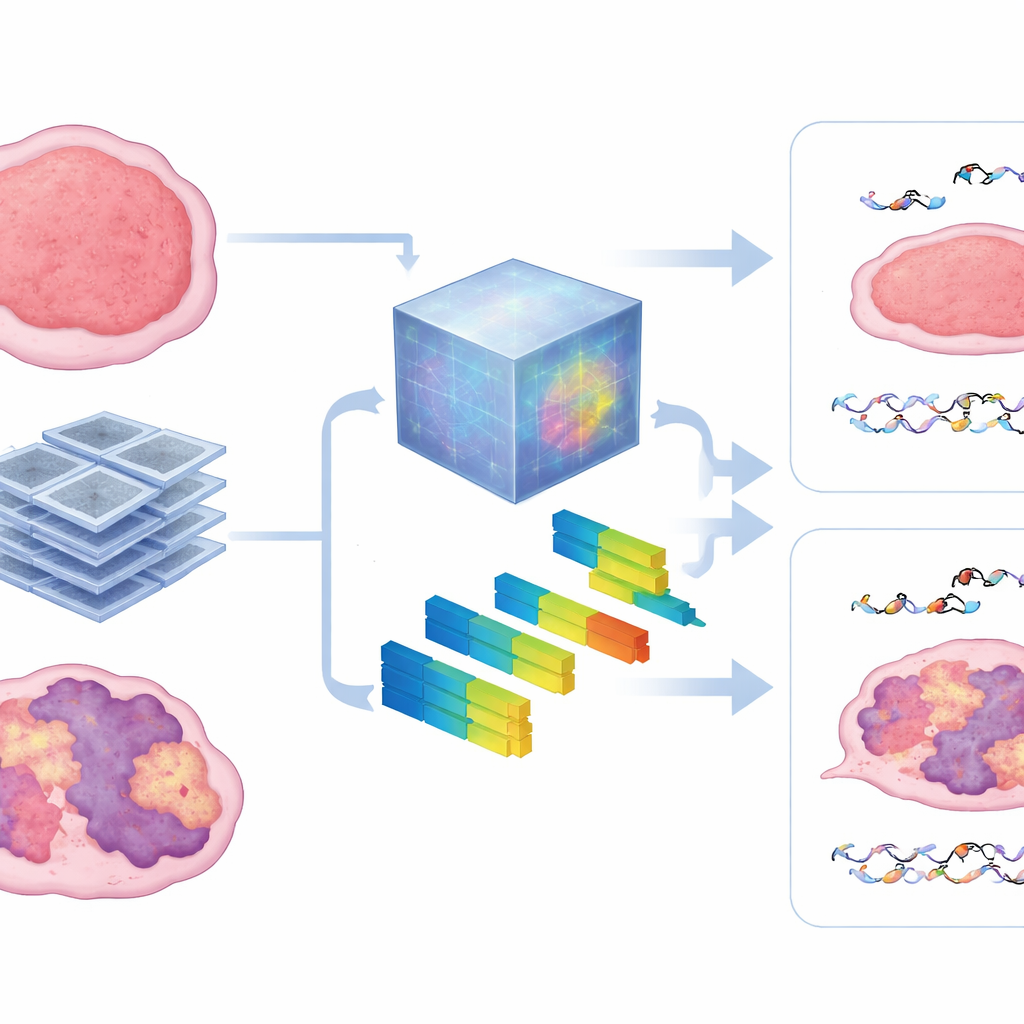
Taramalar tümörün içinde neyi açığa çıkarıyor
Siyah kutuya bakmak için yazarlar, temel model tarafından öğrenilen desenleri görüntü doku ve yoğunluğunu tanımlayan standart radyomik özelliklerle karşılaştırdı. Modelin büyük ölçüde heterojenlik ölçümlerine — tümörün BT’de ne kadar yamalı, kaba veya düzensiz göründüğüne — güvendiğini buldular. Daha güçlü HRD imzalarına sahip tümörler genellikle daha düzensiz dokular sergiledi ve bu aynı özellikler hem mikroskobik DNA hasarını hem de makroskobik tümör kontrolünü öngörmeye yardımcı oldu. Yaklaşım, daha az eğitim verisi bulunduğunda da sağlam kaldı; bu, önceden eğitilmiş modellerin büyük görüntüleme veri setlerinin toplanmasının zor olduğu hayvan çalışmalarındaki önemli bir engeli aşabileceğine işaret ediyor.
Fare deneylerinden gelecekteki hasta bakımına
Bu preklinik çalışma, güçlü, önceden eğitilmiş bir yapay zekâ ile yorumlanan tek bir BT taramasının hatalı DNA onarımının sinyallerini yakalayabileceğini ve bir tümörün DNA’ya zarar veren bir ilaca ne kadar güçlü yanıt vereceğini tahmin edebileceğini gösteriyor. Bir uzman olmayan için çıkarım şudur: standart görünen taramalar yakında ekstra prosedürlere gerek kalmadan hem tümörün yerini belirleyebilir hem de ne kadar kırılgan olduğunu açığa çıkarabilir. Bunun rutin bakımın bir parçası haline gelmeden önce yöntem, insan hastalarda test edilmeli ve doğrulanmalıdır. Bu çabalar başarılı olursa, BT tabanlı yapay zekâ HRD parmak izleri doktorların kişileri CP‑506 ve benzeri tedavilere daha doğru eşleştirmesine yardımcı olabilir; bu da etkileri iyileştirirken diğerlerini etkisiz ve toksik ilaçlardan koruyabilir.
Atıf: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
Anahtar kelimeler: homolog rekombinasyon yetmezliği, kanser görüntüleme, radyomik, temel modeller, DNA'ya zarar veren tedavi