Clear Sky Science · tr
Birçok kanser türünde histopatolojik tam slayt görüntülerinde otomatik tümör segmentasyonunun genelleştirilmesi
Kanser bakımında bunun önemi nedir
Kanser teşhisi hâlâ uzmanların boyanmış doku cam lamlarını mikroskop altında dikkatle incelemesine dayanıyor—bu, vaka sayılarının artması ve patolog eksikliği nedeniyle zaman alıcı bir iş. Bu çalışma basit ama etkili bir soruyu gündeme getiriyor: ayrı kanser türleri için ayrı bir araç geliştirmek yerine tek bir yapay zeka sistemi, dijital mikroskop görüntülerinde birçok farklı tümör tipindeki kanserli bölgeleri güvenilir şekilde bulabilir mi? Eğer yapabilirse, iş yüklerini hafifletebilir, tanıyı hızlandırabilir ve veri kıtlığı olan daha nadir kanserler için bile gelişmiş analizleri erişilebilir kılabilir.
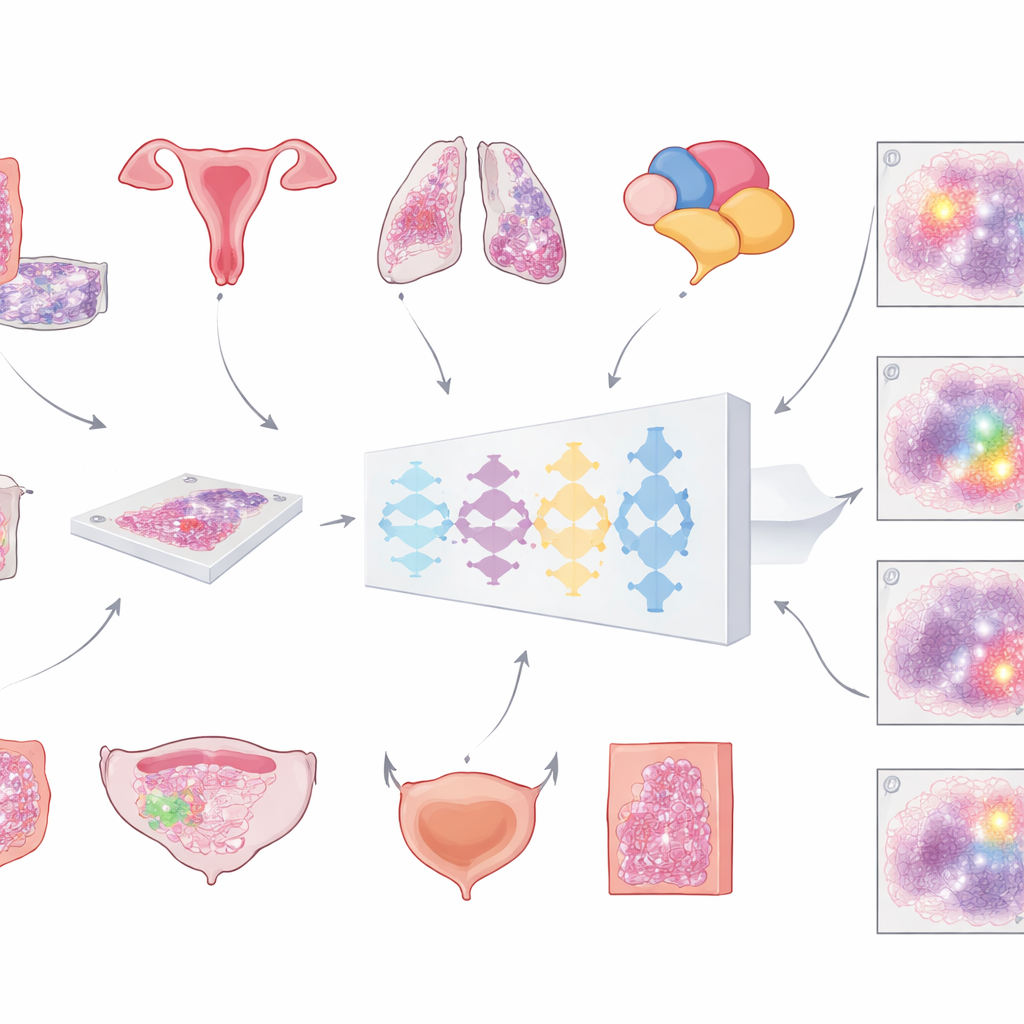
Cam lamlardan dijital yardımcı uygulamalara
Modern hastaneler giderek daha fazla mikroskop lamlarını tarayarak tümörlerin büyük, ayrıntılı “tam‑slayt görüntülerini” oluşturuyor. Bilgisayar destekli herhangi bir analizin ilk kritik adımı, kanserli dokuyu her şeyden ayırmaktır—normal hücreler, yağ, boş cam ve artefaktler. Bugüne kadar çoğu otomatik araç yalnızca tek bir kanser türü üzerinde eğitildi, bu da kullanım alanlarını sınırladı. Bu çalışmanın ekibi, sıradan hematoksilin ve eozin boyamalarıyla hazırlanmış lamlarda birden fazla yaygın kanser türünde tümör bölgelerini tespit edebilecek tek, evrensel bir model oluşturmaya karar verdi. Amaçları, her seferinde yeniden tasarım gerektirmeden birçok tanısal iş akışına entegre edilebilecek genel bir araç geliştirmekti.
Çok sayıda kanseri görmek için tek model eğitmek
Modeli oluşturmak için araştırmacılar alışılmadık derecede büyük ve çeşitli bir dijital lam koleksiyonu bir araya getirdiler: kolorektal, endometrial, akciğer ve prostat kanserli 4.000’den fazla hastaya ait 20.000’den fazla tam‑slayt görüntüsü. Tüm örnekler standart formalin fikse, parafin gömülü dokulardan geldi ve iki farklı yüksek çözünürlüklü lam tarayıcısında tarandı. Bir patolog her lamda tümör alanlarını dikkatle çizerek bilgisayarın öğreneceği “gerçek zemin”i sağladı. Model çok adımlı bir boru hattı izledi: her devasa görüntü büyük üst üste binen parçalara bölündü, her piksel için tümör olma olasılığını tahmin eden derin bir sinir ağından geçirildi ve ardından pürüzsüz bir haritaya yeniden birleştirilerek nihayetinde temiz bir tümör‑ve‑tümör olmayan maskesine dönüştürüldü.
Sistemi teste sokmak
Önemli olarak, ekip yalnızca eğitim performansında kalmadı. Aynı modeli eğitimde hiç kullanılmamış meme ve mesane kanserleri de dahil olmak üzere altı kanser türünden 3.000’den fazla ek hasta üzerinde ve birden çok hastaneden ve tarayıcıdan gelen lamlarda test ettiler. Doğruluk esas olarak bilgisayarın tümör sınırının patologunkilerle mükemmel örtüştüğü durumda %100’e ulaşan standart bir örtüşme skoru (Dice katsayısı) ile ölçüldü. Kolorektal, endometrial, akciğer, prostat ve meme kanserindeki büyük, bütün tümör örnekleri için ortalama örtüşme %80’in üzerinde ve sıklıkla %90’ı aştı. Dünya çapında birçok laboratuvardan ve tarayıcıdan derlenen The Cancer Genome Atlas’ın büyük dış koleksiyonlarında performans yine %80’in üzerinde kaldı; bu, modelin kendi kurumunun dışına iyi şekilde genelleyebildiğini gösteriyor.
Zorlandığı alanlar ve kıyaslama
En büyük zayıflık, doku parçalarını küçük ve parçalanmış hale getiren bir prosedürle alınan erken evre mesane kanserlerinde ortaya çıktı. Bu durumlarda model sıklıkla hiç tümör işaretlemiyordu, özellikle tümör alanı çok küçük olduğunda. Yine de tümörü tespit ettiğinde patologun çizimleriyle örtüşme yüksekti ve son eşik değerlerinde yapılan basit ayarlamalar sonuçları iyileştirdi—bu da temel ağın deseni tanıdığını ancak son işlem adımının fazla katı olduğunu düşündürüyor. Araştırmacılar ayrıca her biri tek bir kanser türü üzerinde eğitilmiş dört “uzman” model de geliştirdiler ve hiçbirinin kendi alanında genel modele anlamlı bir üstünlük sağlamadığını buldular. Buna karşın, bu uzman sistemler diğer kanser türlerine uygulandığında büyük ölçüde başarısız olurken genel model sağlam kaldı. Kullanıcı ipuçları gerektiren popüler, daha genel bir tıbbi segmentasyon aracıyla karşılaştırıldığında, yeni model genelde en az onun kadar iyi veya daha iyi performans gösterdi ve tamamen otomatik kaldı.
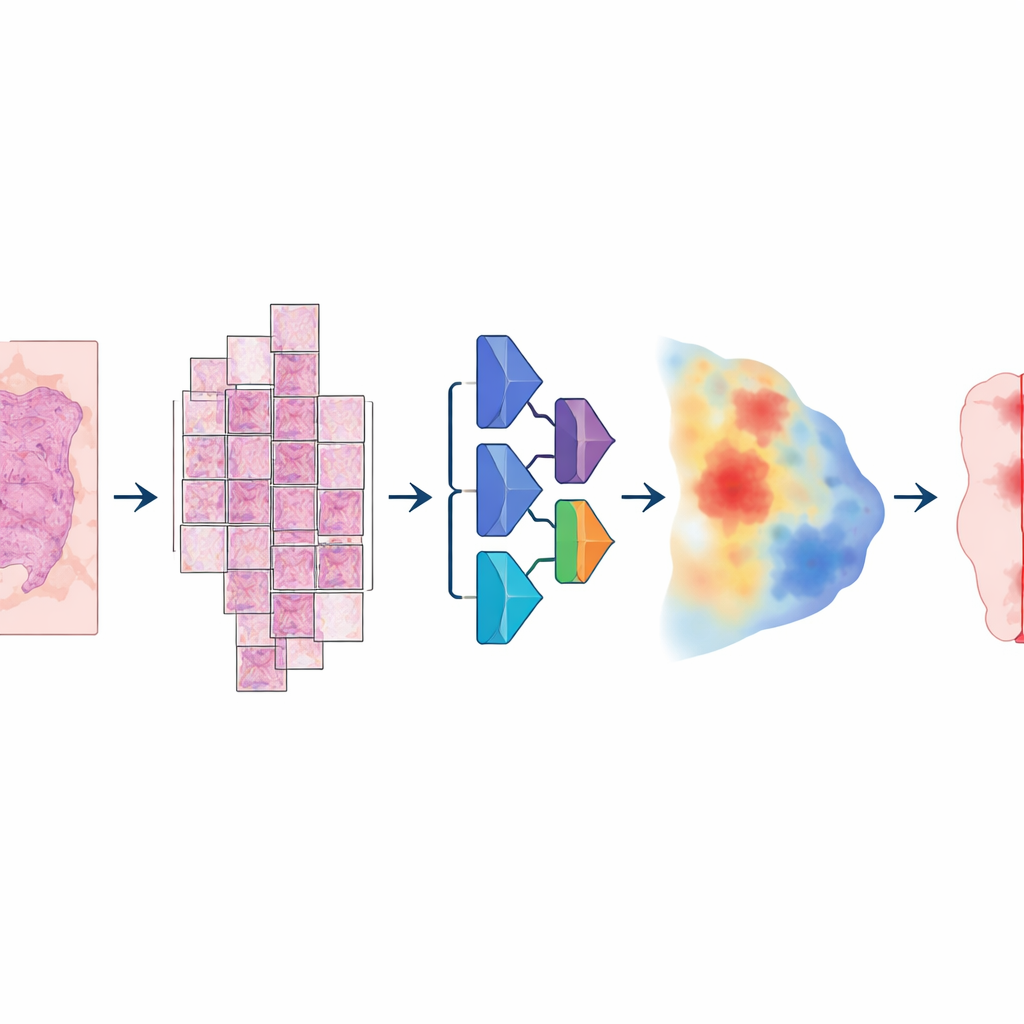
Hastalar ve doktorlar için anlamı
Uzman olmayanlar için çıkarılacak ana mesaj şudur: iyi tasarlanmış tek bir yapay zeka sistemi, her hastalık veya tarayıcı için özel sürümlere gerek kalmadan dijital lamlarda birkaç büyük tümör türü boyunca kanserli dokuyu güvenilir şekilde öne çıkarabilir. Patoloğu yerine geçmez, ancak muhtemel tümör bölgelerini önceden işaretleyebilir, tutarlı ölçümlere yardımcı olabilir ve uzmanların en zor vakalara odaklanmasını sağlayabilir. Mevcut sürüm hâlâ çok küçük veya erken evre bazı tümörleri—özellikle parçalanmış mesane örnekleri ve muhtemelen biyopsiye benzer diğer dokuları—kaçırıyor, bu nedenle en soluk kanser izlerini tespit etmeye henüz uygun değil. Yine de çalışma, geniş kapsamlı “pan‑kanser” tümör segmentasyonunun gerçek dünya koşullarında uygulanabilir olduğunu ve kanser derecesini değerlendiren, tedavi yanıtını tahmin eden veya kişiselleştirilmiş tedavileri yönlendiren gelecekteki otomatik araçlar için sağlam bir ilk adım oluşturabileceğini gösteriyor.
Atıf: Skrede, OJ., Pradhan, M., Isaksen, M.X. et al. Generalisation of automatic tumour segmentation in histopathological whole-slide images across multiple cancer types. npj Precis. Onc. 10, 107 (2026). https://doi.org/10.1038/s41698-026-01311-6
Anahtar kelimeler: dijital patoloji, derin öğrenme, tümör segmentasyonu, tam‑slayt görüntüleme, pan‑kanser model