Clear Sky Science · tr
Büyük ölçekli tek hücre analizi ve in siliko perturbasyon HCC'nin dinamik evrimini ortaya koydu: baştan tedavi hedeflemeye
Karaciğer kanserinin iç yaşamı neden önemli
Hepatosellüler karsinom, karaciğer kanserinin en yaygın biçimi, tedavisi özellikle zor bir hastalıktır. Pek çok hasta mevcut ilaçlara iyi yanıt vermez ve tümörler sık sık nükseder veya yayılır. Bunun büyük bir nedeni, her tümörün zaman içinde evrimleşen ve çevresiyle sürekli iletişim halinde olan farklı hücrelerin kaotik bir karışımı olmasıdır. Bu çalışma, güçlü tek hücre ve uzamsal gen okuma teknolojilerini kullanarak o evrimi hücre hücre izliyor — erken tümör büyümesinden ileri, tedaviye dirençli hastalığa kadar — ve yeni tedavilerin hedefleyebileceği zaafları belirliyor.
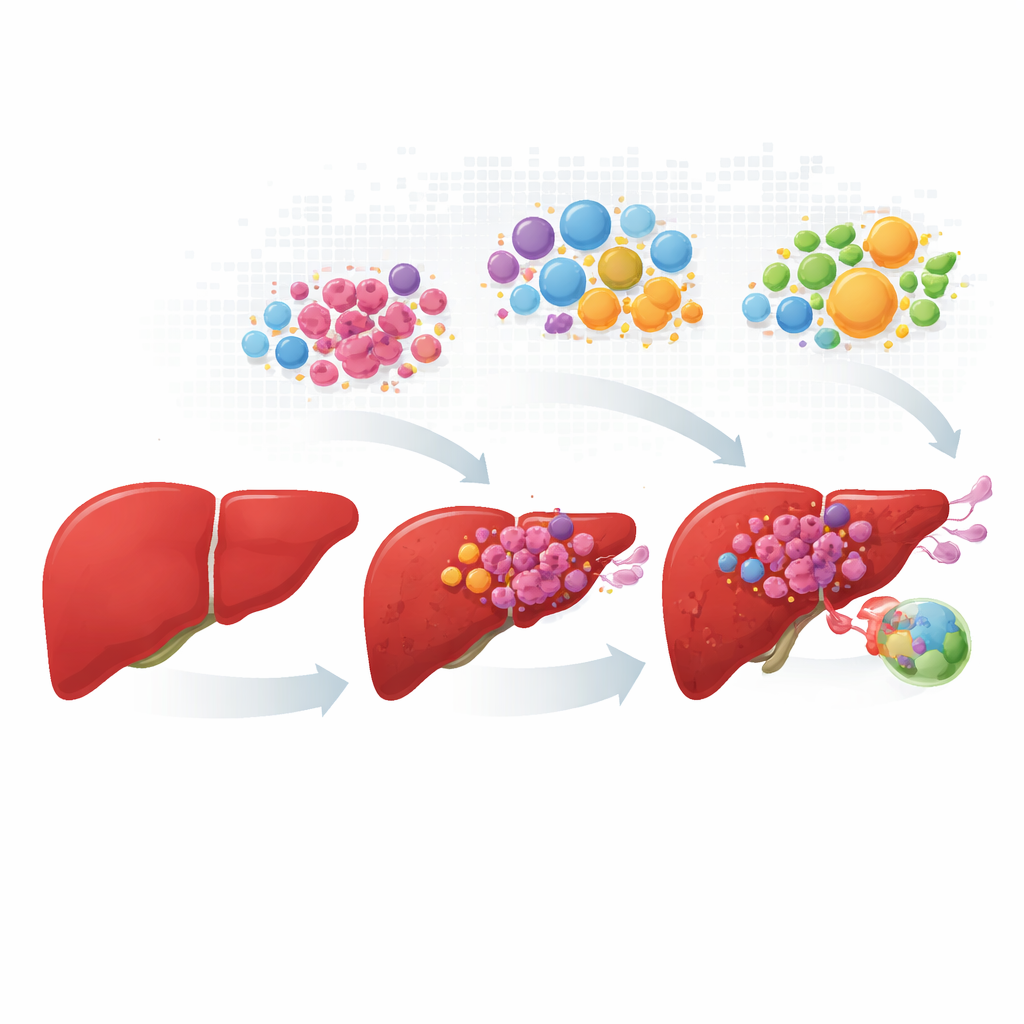
Kanser hücrelerini erken değişimden yayılmaya kadar izlemek
Araştırmacılar, normal karaciğer dokusunu, primer tümörleri, damar içi büyümeleri ve lenf nodu metastazlarını kapsayan yüzün üzerinde hastadan veri toplayıp uyumladılar. Her tümörü tek tip bir kitle olarak ele almak yerine yüzbinlerce bireysel hücreyi profillediler ve ardından bu hücrelerin gerçek doku kesitlerindeki yerlerini haritaladılar. Kanserli karaciğer hücreleri dört yineleyen “kişilik”e ayrıldı. Bir grup birçok normal karaciğer işlevini ve metabolik görevi korurken; diğer üçü stres kaynaklı büyüme, MYC büyüme yolunun yüksek aktivitesi veya invaziv, iltihap ilişkili davranış gösteriyordu. Bu dört durum, hastalık ilerledikçe farklı oranlarda ortaya çıktı; hızlı çoğalan ve invaziv hücreler damar ve lenf nodu lezyonlarında baskın oldu.
Farklı gelecekleri olan dört tümör kişiliği
Dört kanser hücresi durumu sadece akademik bir sınıflandırma değildi; hastaların gidişatıyla bağlantılıydı. Karaciğer benzeri, metabolik olarak aktif durum bakımından zengin tümörler daha iyi sağkalımla ilişkilendirilirken, diğer üç agresif durumla baskınlaşan tümörler genellikle daha kötü sonuçlara sahipti. Yine de “iyi” durumun da bir tuzağı vardı: bu durum, muhtemelen ilaçları inaktive edebilen detoks mekanizmalarını koruduğundan, karaciğer kanseri ilacı sorafenib’den fayda görmeyen hastalarda güçlü biçimde zenginleşmişti. Hücrelerin gelişimsel patikalar boyunca nasıl ilerlediğini tekrar oynatarak ekip, invaziv, iltihaplı hücrelerin daha farklılaşmış veya daha yüksek proliferatif duruma dallanabileceğini gösterdi; bu da tümör hücrelerinin kimlik değiştirebileceğini ve tek bir durumu hedefleyen tedavilerden kaçabileceğini düşündürüyor.
Destekleyici kadro: bağışıklık ve stromal işbirlikçiler
Kanser hücreleri tek başına hareket etmez. Çalışma, tümörlerle savaşan ya da sessizce yardımcı olan özelleşmiş bağışıklık hücreleri ve destek hücrelerini ortaya çıkardı. Doku içindeki çöpçüler ve bekçiler olan makrofajlar arasında bazı tipler anti‑tümör bağışıklığı destekleyebilecek iltihap sinyalleri üretirken, diğerleri metabolik olarak yeniden düzenlenmiş, yararlı sinyalleri baskılamış ve kan damar oluşumunu ile invazyonu teşvik etmişti. Bu “kötü oyuncu” makrofajlar ileri örneklerde genişledi. Benzer şekilde, damarları döşeyen belirli endotel hücreleri ve bağ dokusunu oluşturan fibroblastlar kötü prognozla ilişkili ayrı alt gruplar oluşturdular. İleri hastalıkta belirli bir endotel alt tipi ve iki fibroblast tipi, ekstraselüler iskeleti yeniden şekillendiren, yeni damar oluşumunu destekleyen ve en agresif kanser hücresi durumlarıyla korele olan sıkı bağlantılı merkezler yarattı.
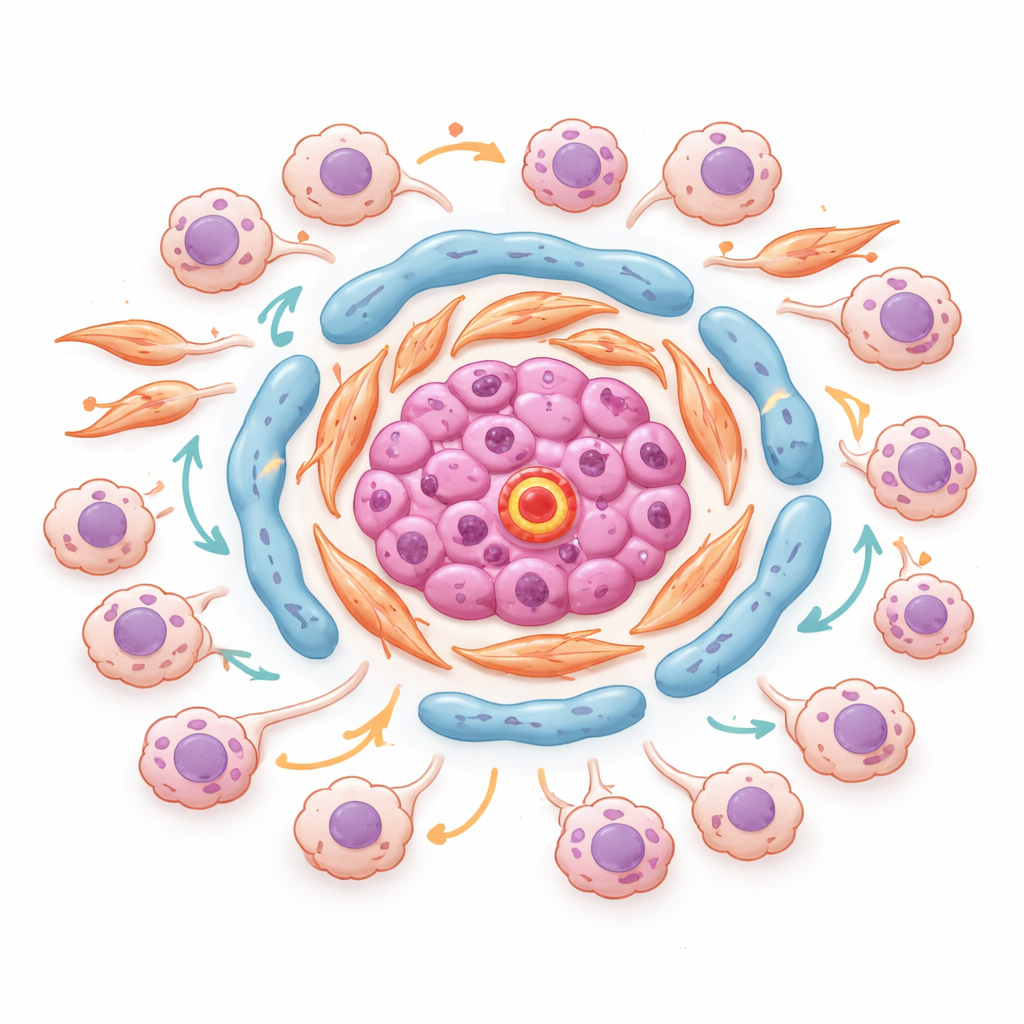
Tümör içindeki tehlikeli mahalleleri görmek
Her noktanın doku içindeki yerini kaybetmeden gen aktivitesini ölçen uzamsal transkriptomik kullanılarak yazarlar, tümörlerin içinde organize “mahalleler” belirlediler. Temsili bir tümörde ESM1 adlı molekülden zengin endotel hücreleri, lipid‑aç ve matris üreten fibroblastlarla stromal adacıkların çekirdeğinde kümelenmişti. Bu çekirdeklerin çevresinde güçlü TGF‑beta ve düşük oksijen sinyallerinin olduğu bölgelerde stres kaynaklı ve invaziv kanser hücreleri birikti. Hücrelerin stres ve iltihaba nasıl yanıt vereceğini kontrol eden önemli transkripsiyon faktörleri bu kanser durumları arasında paylaşılıyordu ve tam olarak tümör hücrelerinin bu stromal merkezlere dokunduğu yerlerde en aktifti. Bu, tümör–stroma sınırlarındaki belirli mikro‑nişlerin kanser hücrelerini durum değiştirmeye, daha agresif hale gelmeye ve tedaviye direnç kazanmaya aktif olarak teşvik ettiğini düşündürüyor.
Yeni tedaviler için ortak bir zayıf nokta bulmak
Açıklamadan müdahaleye geçmek için ekip, milyonlarca hücre üzerinde eğitilmiş bir makine öğrenmesi modeli kullanarak genlerin “sanal yok edilmesini” simüle etti ve hangi değişikliklerin zararlı hücreleri daha sağlıklı durumlara itebileceğini tahmin etti. Makrofajları, endotel hücrelerini ve kanser hücrelerini karşılaştırarak üçünü de normalize etmeye yardımcı olan küçük bir gen seti buldular. Bunların arasında HSP90B1 öne çıktı: kanser hücre hatları buna büyük ölçüde bağımlı, karaciğer tümörlerinde aşırı üretimi var, özellikle hedefe yönelik ilaçlara ve immünoterapiye dirençli olanlarda yüksek düzeyde ve yüksek seviyeler daha kötü sağkalımı öngörüyor. HSP90B1, hücrenin protein katlanma fabrikasındaki stresle başa çıkan bir kılıf proteini kodlar; birçok yüzey reseptörünü ve sinyal yolunu destekler. Bu kılıf proteine karşı seçici ilaçlar zaten mevcut olduğu ve bağışıklık ortamını da yeniden şekillendirebildiği için çalışma, HSP90B1’i özellikle mevcut karaciğer kanseri tedavileriyle kombinasyon halinde direnci aşmak için umut verici bir hedef olarak öneriyor.
Bu hastalar ve tedaviler için ne anlama geliyor
Bir araya getirildiğinde, bu çalışma karaciğer kanserinin tek bir hastalık olmadığını, tümör büyüdükçe ve yayıldıkça değişen bir hücre durumu ve nişler ekosistemi olduğunu gösteriyor. Belirli kanser hücresi kişiliklerini, destek hücrelerini ve uzamsal mahalleleri hasta sonucu ve ilaç yanıtıyla ilişkilendirerek çalışma daha hassas tedavi için bir yol haritası sunuyor: baskın hücre durumlarına uygun tedaviler eşleştirmek, agresif davranışı besleyen stromal merkezleri bozmak ve birçok tümör ile mikroçevre hücresinin dayandığı HSP90B1 gibi ortak bağımlılıkları hedeflemek. Daha fazla laboratuvar ve klinik test gerekli olmakla birlikte, ekip tarafından oluşturulan atlas, tümörün içsel karmaşıklığını engel olmaktan çıkarıp daha akıllı, daha kalıcı karaciğer kanseri tedavilerine dönüştürmek için ayrıntılı bir plan sunuyor.
Atıf: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
Anahtar kelimeler: hepatosellüler karsinom, tek hücre analizi, tümör mikroçevresi, uzamsal transkriptomik, HSP90B1