Clear Sky Science · tr
Entegre edilmiş tek hücre akciğer kanseri atlası, adenokarsinom ile skuamöz hücreli karsinomlar arasında belirgin fibroblast fenotiplerini ortaya koyuyor
Tümörün Çevresi Neden Önemli?
Akciğer kanseri yalnızca kanser hücrelerinden oluşmaz. Daha çok, kanser hücrelerinin kan damarları, bağışıklık hücreleri ve destek hücreleriyle birlikte yaşadığı kalabalık bir şehre benzer. Bu çalışma, büyük çıkarımları olan şaşırtıcı derecede basit bir soruyu soruyor: iki ana tip küçük hücre dışı akciğer kanseri—adenokarsinom ve skuamöz hücreli karsinom—akciğer içinde farklı “mahalleler” mi inşa ediyor ve bu farklılıklar hastaların daha iyi ya da daha kötü olma nedenlerini açıklamaya yardımcı olabilir mi? Güçlü tek hücreli gen okuma araçlarını kullanarak, araştırmacılar yüz binlerce bireysel hücreyi haritalandırıp destek hücrelerden biri olan fibroblastların bu iki kanserde çok farklı davrandığını ortaya koyuyor.
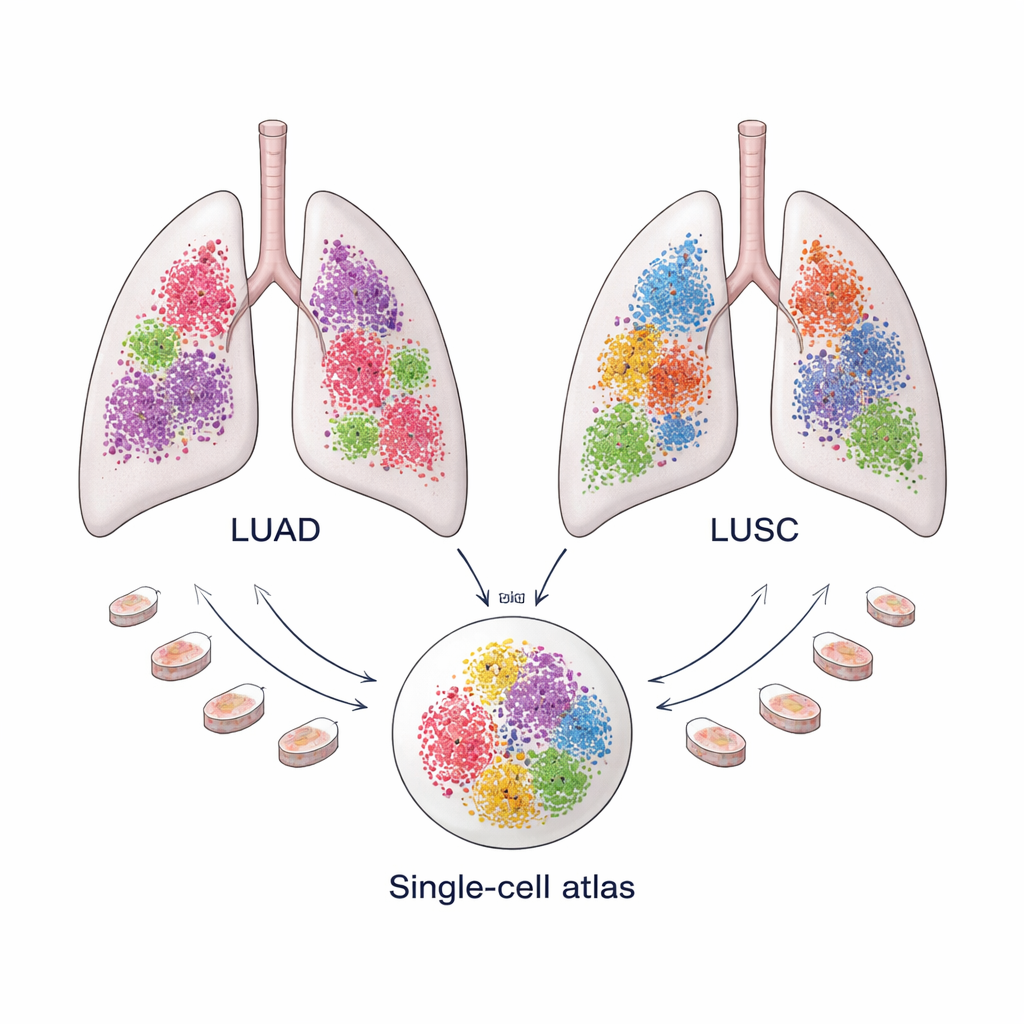
İki Yaygın Akciğer Kanseri, İki Ayrı Ekosistem
Küçük hücre dışı akciğer kanseri, akciğer kanserlerinin yaklaşık yüzde 85’ini oluşturur ve iki tip tarafından domine edilir: genellikle akciğerin dış kısımlarında ortaya çıkan akciğer adenokarsinomu (LUAD) ve daha merkezi bölgelerde görülen akciğer skuamöz hücreli karsinomu (LUSC). Her ikisi de bugün aynı geniş etiket altında tedavi edilse de, tedaviye farklı yanıt verir ve uzun dönemde farklı sonuçlar gösterir. Artan kanıtlar, bu farklılıkların yalnızca kanser hücrelerinin kendisinden kaynaklanmadığını, aynı zamanda tümörü çevreleyen ve onunla etkileşen bağışıklık hücreleri, kan damarları ve yapısal hücrelerden oluşan “tümör mikroçevresi” nedeniyle de ortaya çıktığını gösteriyor.
Tek Hücreli Akciğer Kanseri Atlası Oluşturmak
Bu mikroçevreleri ayrıntılı biçimde anlamak için ekip geniş bir tek hücre RNA dizilemesi veri “atlası” bir araya getirdi: on kamu veri setinden alınan 175 LUAD örneğinden 366.652 hücre ve 74 LUSC örneğinden 125.238 hücre. Her hücrenin gen aktivite deseni, araştırmacıların hücreleri bağışıklık hücreleri, damar hücreleri, kanser hücreleri ve yapısal veya “stromal” hücreler gibi ana gruplara ayırmasına olanak veren bir parmak izi işlevi gördü. Gelişmiş hesaplama yöntemleri teknik gürültüyü giderdi ve farklı hastalardan alınan örnekleri hizalayarak hücrelerin doğrudan karşılaştırılmasını sağladı. Bu ölçek kritik önem taşıyor; çünkü bazı hücre tipleri—özellikle fibroblastlar—nadir ve tek bir çalışmada yeterli sayıda izole edilmesi zor olabiliyor.
Fibroblastlar: Tümör Peyzajının Şekillendiricileri
Fibroblastlar, bağ dokusunu inşa eden ve yeniden düzenleyen destek hücreleridir. Tümörlerde kanser ilişkili fibroblastlar (CAF’ler) haline gelirler ve durumlarına bağlı olarak tümör büyümesini ya engelleyebilir ya da destekleyebilirler. 8.700’den fazla fibroblasta odaklanarak yazarlar beş ana CAF alt tipini tanımladı: miyofibroblastik CAF’ler (mCAF’ler), inflamatuar CAF’ler (iCAF’ler), damar ilişkili CAF’ler (vCAF’ler), döngüsel CAF’ler (cCAF’ler) ve antijen sunan CAF’ler (apCAF’ler). Bu alt tiplerin dengesi LUAD ile LUSC arasında çarpıcı biçimde farklıydı. LUAD tümörleri yüksek düzeyde inflamatuar moleküller salgılayan iCAF’leri daha çok barındırma eğilimindeyken, LUSC tümörleri sert, lifli doku üreten ve tümörün fiziksel iskeletini şekillendirmeye yardımcı olan mCAF’ler açısından daha zengindi.
Kanser Hücreleri Fibroblastlara Rollerini Öğretiyor
Kanser hücrelerinin fibroblastları bu kimlikleri benimsemeye yönlendirip yönlendirmediğini test etmek için araştırmacılar, normal akciğer fibroblastlarını bir dizi LUAD veya LUSC hücre hattıyla aynı kaplarda büyüttüler. LUAD hücrelerine maruz kalan fibroblastlar, IL-6 ve belirli kemokinler gibi iyi bilinen inflamatuar sinyalleri içeren iCAF’lere özgü genleri açtı. LUSC hücreleriyle eşleştirildiklerinde aynı fibroblastlar bunun yerine kas benzeri kasılma ve kollajen üretimiyle ilişkili mCAF genlerini etkinleştirdi. Hücreler arası iletişim analizleri, LUAD hücrelerinin inflamatuar iCAF durumunu tetiklemek için IL-1, LIF ve OSM gibi sitokinleri kullandığını; LUSC hücrelerinin ise fibroblastları matris inşa eden mCAF durumuna itmek için daha çok mekanik ipuçlarına ve kanonik olmayan WNT sinyaline dayandığını öne sürdü.
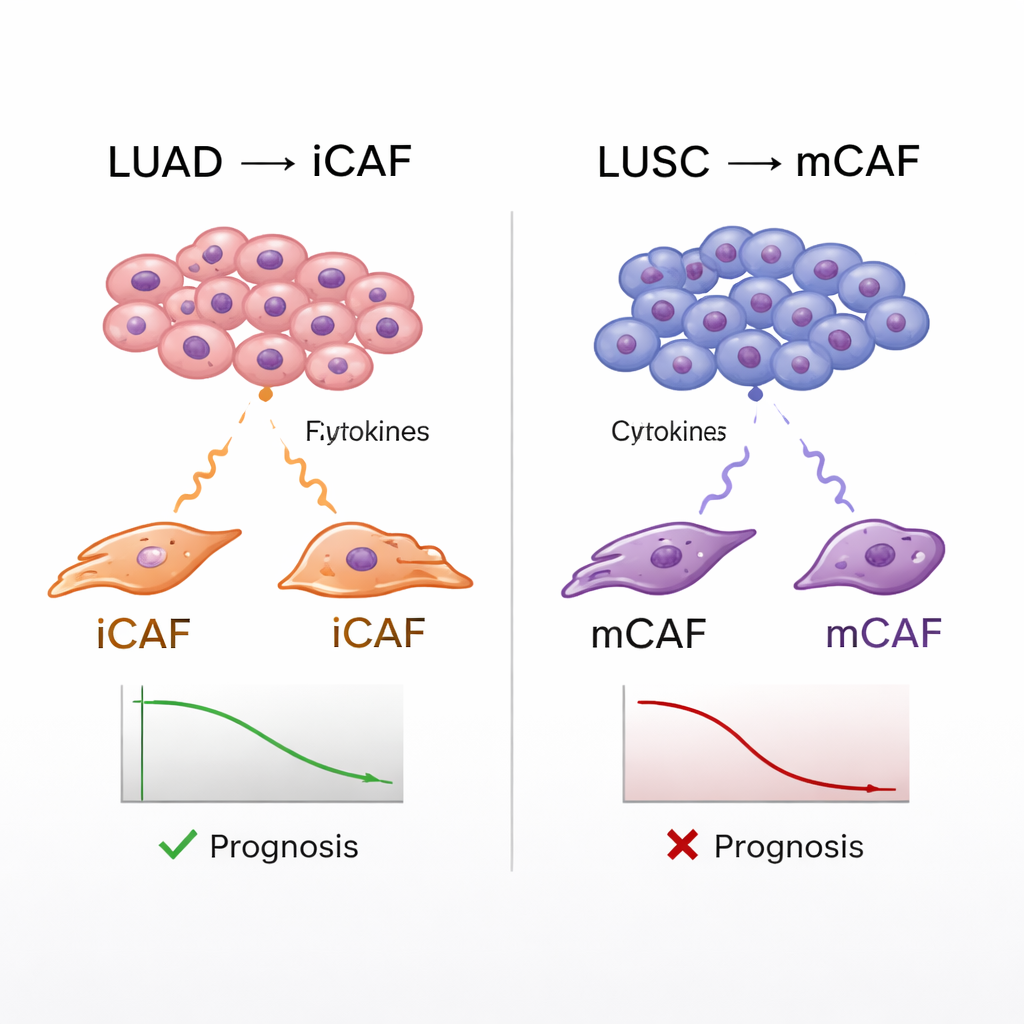
Fibroblast Türlerini Hasta Sonuçlarıyla Bağlamak
Atlas, ekiplerin CAF alt tiplerini gerçek dünyadaki hasta verilerine bağlamasına da izin verdi. Büyük kanser veri tabanlarını kullanarak her hastanın tümörünün farklı fibroblast tiplerine ait gen imzalarını ne ölçüde ifade ettiğini tahmin ettiler ve bu skorları sağkalımla karşılaştırdılar. Hem LUAD hem de LUSC genelinde mCAF’lerle zenginleşmiş tümörler daha kötü sonuçlarla ilişkilendirildi; bu da tümörlerin etrafındaki yoğun, lifli kapsülün kanser ilerlemesine yardımcı olabileceği ve bağışıklık saldırısını engelleyebileceği fikriyle tutarlı. Ancak iCAF’ler ayrık bir kişilik sergiledi: LUSC’de yüksek iCAF imzaları da daha kötü sağkalımı öngörürken, LUAD’da daha iyi sonuçlarla ilişkilendirildi. Daha ileri analizler, LUSC’de iCAF’lerin nötrofilleri çekmeye yardımcı olduğunu; bu bağlamda nötrofillerin yararlı T hücrelerini baskıladığı görülerek etkili bağışıklık yanıtları için özellikle düşmanca bir ortam yarattığını düşündürdü.
Gelecekteki Akciğer Kanseri Bakımı İçin Anlamı
Uzman olmayan bir okuyucu için temel mesaj şudur: akciğer tümörlerindeki tüm destek hücreleri aynı değildir ve aynı fibroblast alt tipi kanser bağlamına bağlı olarak zıt anlamlar taşıyabilir. LUAD ve LUSC sadece kanser hücrelerinin DNA’sında farklılık göstermiyor; tümörlerin nasıl büyüdüğünü ve hastaların nasıl sonuçlandığını şekillendiren farklı mikroskobik ekosistemler inşa ediyorlar. Bu çalışmanın hücre hücre haritalaması, prognoz göstergesi veya gelecekteki tedaviler için hedef olabilecek belirli fibroblast popülasyonlarını tanımlıyor—ideal olarak tedavilerin yalnızca kanser tipine değil, aynı zamanda onu çevreleyen ve sürdüren hücre karışımına da göre uyarlanmasına izin verebilir.
Atıf: Hirano, Y., Suzuki, H., Nakayama, J. et al. An integrated single-cell lung cancer atlas reveals distinct fibroblast phenotypes between adenocarcinoma and squamous cell carcinomas. npj Precis. Onc. 10, 72 (2026). https://doi.org/10.1038/s41698-026-01279-3
Anahtar kelimeler: akciğer kanseri, tümör mikroçevresi, fibroblastlar, tek hücre RNA dizilemesi, kanser prognozu