Clear Sky Science · tr
TheraMind: olgu raporu madenciliği ile akciğer kanserinde ilaç yeniden kullanımı hızlandırmak için çoklu-LLM topluluğu
Hastalar ve doktorlar için neden önemli
İleri evre akciğer kanseri olan insanlar için zaman çok kıymetlidir ve tedavi seçenekleri genellikle hızla tükenir. Yepyeni ilaçlar geliştirmek on yıldan uzun sürebilir, oysa yararlı tedavilere dair dağınık ipuçları hâlihazırda yayımlanmış hasta öykülerinde —olgu raporlarında— saklı olabilir. Bu makale, binlerce olgu raporunu tarayarak zor tedavi edilen akciğer kanseri olan insanlara güvenle yeniden uygulanabilecek mevcut ilaçları ortaya çıkaran bir yapay zeka sistemi olan TheraMind’i tanıtıyor.
Eski ilaçlara yeni kullanım bulmanın zorluğu
Hücresel olmayan küçük hücreli olmayan akciğer kanseri (non-small cell lung cancer), hastalığın yayıldığı aşamada sağkalım oranlarının hâlâ çok düşük olduğu dünyanın en ölümcül kanseridir. Baştan yeni ilaç keşfetmek ve test etmek yavaş, maliyetli ve risklidir. Buna karşılık "yeniden kullanılan" ilaçlar başka durumlar için zaten onaylıdır, bu yüzden güvenlikleri hakkında çok daha fazla bilgi vardır. Onkologlar, standart tedavileri tükenmiş hastalar için bu tür ilaçlara ilgi duyarlar, ancak bir ilacın gerçekten akciğer kanserli birine yardımcı olduğuna dair laboratuvar verilerinden öte gerçek dünya kanıtına ihtiyaç duyarlar. Bu klinik ipuçları genellikle tıp literatürünün derinliklerinde gömülü bireysel olgu raporlarında ortaya çıkar ve elle bulmak zor ve zaman alıcıdır.
Binlerce hasta öyküsünü okuyan dijital bir okuyucu
Araştırmacılar, olgu raporlarının yorulmak bilmez ve dikkatli bir okuyucusu olarak hareket etmesi için TheraMind’i oluşturdu. Önceki genomik ve laboratuvar çalışmaları tarafından önerilen 18 ilaç adayından yola çıkarak sistem otomatik olarak PubMed’den, en büyük tıbbi makale veritabanından, 10.023 olgu raporu çekti. Daha sonra her raporun metnini tıbbi yazıyı anlamak üzere eğitilmiş üç ayrı dil modeline —farklı yapay zeka "okuyucularına"— verdi. Her rapor için bu modeller aynı dört basit soruyu yanıtladı: Hastanın tanımı küçük hücreli olmayan akciğer kanseri miydi? Çalışma ilacı özellikle bunun için mi verildi? Tedavi erken mi sonlandırıldı? Ve hasta iyi bir klinik sonuç mu yaşadı?
Yapay zeka ekibinin ortak karara nasıl vardığı
TheraMind her raporu evet-hayır cevapları setine dönüştürdüğünde, birkaç karar katmanı devreye girer. Bir yöntem, bir olgunun ilaç yeniden kullanımı için ilgili sayılmadan önce bu dört koşulun tamamının sağlanmasını gerektiren el yapımı bir karar ağacı kullanır. Başka bir yöntem, tek bir modelin hem evet-hayır cevaplarını hem de ürettiği kısa açıklamaları dikkate alarak kanıtı daha esnek biçimde tartmasına izin verir. En güçlü yöntem ise farklı bir modele dayanan üç ayrı sınıflandırıcıyı birleştirir ve üçten en az iki model bir raporun ilgili olduğunu onayladığında kabul eder. Bu "çoğunluk oyu" yaklaşımı, birkaç bağımsız doktorun aynı dosyayı gözden geçirmesine benzer şekilde bireysel hataları iptal etmeye yardımcı olur.
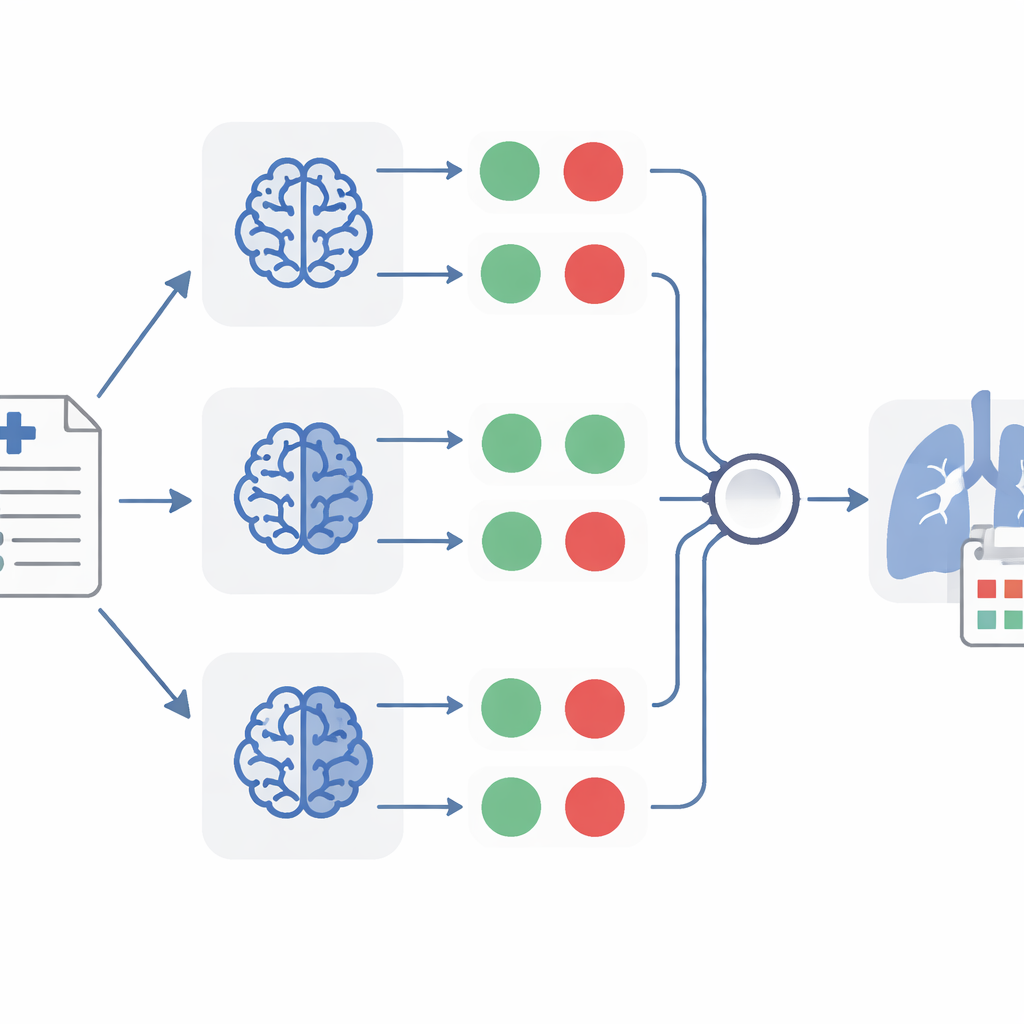
TheraMind’in akciğer kanseri raporlarında keşfettiği şeyler
Geniş olgu raporu koleksiyonuna uygulandığında TheraMind, küçük hücreli olmayan akciğer kanserinde on farklı ilacın kullanımını güçlü biçimde destekleyen 26 raporu işaretledi. Topluluk yöntemi yaklaşık %92 civarında bir geri çağırma (recall) sağladı; bu, gerçekten ilgili olan raporların neredeyse tamamını yakaladığı anlamına gelirken, %99,7 gibi çok yüksek bir özgüllük (specificity) korunarak çok az ilgisiz raporun sızmasına izin verdi. Seçilen her rapor için sistem ayrıca yaş, cinsiyet, tıbbi öykü, durum ve şüphelenilen ilaç gibi temel hasta bilgilerini tutarlı bir veri formatına çıkardı ve olgunun kısa, sade bir özetini oluşturdu. Biyoloji ve bilgisayar bilimi geçmişine sahip insan gözden geçiriciler bu çıktıları kontrol etti ve özellikle bir modelin çok doğru ve eksiksiz çıkarımlar ürettiğini doğruladı.
Akciğer kanserinin ötesine ve kliniğe
Sistemin ne kadar esnek olduğunu test etmek için ekip TheraMind’i meme kanserine ve kendi araştırmalarıyla önceden tanımlanmış birkaç aday ilaca da yöneltti. Bu durumda sistem eşleşen olgu raporları bildirmedi ve bu, kanıt icat etmek yerine mevcut bilimsel kaydı doğru şekilde yansıttı. Yazarlar, kural tabanlı mantığı birden çok yapay zeka okuyucusuyla birleştiren bu tür yapılandırılmış, şeffaf boru hattının laboratuvar keşifleri ile klinik denemelere hazır tedaviler arasındaki boşluğu kapatmaya yardımcı olabileceğini savunuyor. Benzer yöntemlerin diğer kanserlere uygulanmasının vaadini vurgularken, gelecekteki sürümler doğrudan elektronik sağlık kayıtlarına bağlanırsa hasta gizliliğinin dikkatle ele alınması gerektiğine dikkat çekiyorlar.
Gelecek tedaviler için bunun anlamı
Açıkça söylemek gerekirse, TheraMind dağınık, yapılandırılmamış hasta öykülerini doktorlar ve araştırmacıların harekete geçebileceği düzenli kanıtlara dönüştürüyor. Mevcut ilaçların akciğer kanserli insanlara yardımcı olduğu görülen raporları hızla gün yüzüne çıkararak, hangi yeniden kullanılan ilaçların klinik denemelerde daha yakından incelenmeyi hak ettiğine rehberlik edebilir. Tıbbi yargının yerini almasa da, bu çoklu model yapay zeka okuyucusu tıbbi metin dağlarını elemek ve acil yeni seçeneklere ihtiyaç duyan hastalar için güvenilir, kısa bir umut verici seçenek listesi sunmak için bir yol sağlar.
Atıf: More, V., Lu, L., Ding, Z. et al. TheraMind: a multi-LLM ensemble for accelerating drug repurposing in lung cancer via case report mining. npj Precis. Onc. 10, 95 (2026). https://doi.org/10.1038/s41698-025-01265-1
Anahtar kelimeler: ilaç yeniden kullanımı, akciğer kanseri, olgu raporları, büyük dil modelleri, klinik kanıt madenciliği