Clear Sky Science · tr
Neoadjuvan sintilimab, albümin bağlı paklitaksel ve karboplatin için lokal ileri, rezektabl özofagus skuamöz hücreli karsinom: klinik çalışma ve mekanistik keşif
Ölümlü Bir Boğaz Kanserine Karşı Seyri Değiştirmek
Özofagus kanseri, dünya çapında en ölümcül kanserlerden biridir ve genellikle göğüs derinliklerine ilerledikten sonra keşfedilir. Birçok hasta hâlâ ameliyat edilebilir olsa da, günümüzün en iyi kemoterapi ve radyoterapisinde bile hastalığın nüksetme riski yüksektir. Bu çalışma, ameliyattan önce vücudun kendi savunmasını güçlendirmeyi deneyen yeni bir yaklaşımı test ediyor ve tümörlerin ile çevrelerindeki hücrelerin tedaviye nasıl yanıt verdiğini mikroskop altına alarak inceliyor. Bulgular, daha etkili bir tedaviye işaret ediyor ve gerçekten kişiselleştirilmiş bakım için bir yol sunuyor.
Ameliyattan Önce Yeni Bir Üçlü İlaç Planı
Araştırmacılar Çin’de skuamöz hücreli karsinom adı verilen yaygın ve agresif bir özofagus kanseri biçimine sahip 24 kişiyi çalışmaya kaydetti. Hepsinin tümörleri ileri evredeydi ancak hâlâ cerrahiyle çıkarılabiliyordu. Ameliyata gitmeden önce her hasta üç döngüden oluşan bir kombinasyon tedavisi aldı: sintilimab, T hücrelerinin kanseri tanımasına yardımcı olan bağışıklık etkinleştirici bir antikor; artı iki standart kemoterapi ilacı, albümin bağlı paklitaksel ve karboplatin. Bu “neoadjuvan” fazın ardından hastalar özofagus tümörünü çıkarmak için ameliyat edildi ve çoğu hasta sonrasında sintilimaba devam etti.
Daha Güçlü Tümör Küçülmesi ve Ümit Veren Sağkalım
Cerrahlar ve patologlar çıkarılan tümörleri incelediklerinde, bu ameliyat öncesi rejimin birçok hastada derin küçülme sağladığını buldular. Yaklaşık %42’sinde doktorların “major patolojik yanıt” dediği durum gözlendi; yani canlı kanser hücrelerinin yalnızca küçük bir kısmı kaldı. Her üç hastadan biri ana tümör bölgesinde hiç tespit edilebilir kanser hücresi taşımıyordu. Görüntüleme ve klinik izlemde de sonuçlar ümit vericiydi: tedaviden üç yıl sonra yaklaşık dörtte üç hasta hastalığın tekrar etmediği bir durumda hayattaydı ve neredeyse beşte dördü hâlâ hayattaydı. Önemli olarak, bu yoğunlaştırılmış planın yan etkileri yönetilebilir düzeydeydi; tedaviye bağlı ölüm görülmedi ve cerrahi çıkarma güvenli ve uygulanabilir kaldı.
Tümörün Çevresinin Yanıtı Nasıl Şekillendirdiği
Her hasta eşit düzeyde fayda görmedi; bu yüzden ekip nedenini sorguladı. Odaklandıkları şey tümör mikroçevresiydi—kanser hücreleri, bağışıklık hücreleri ve sinyal moleküllerinden oluşan karmaşık komşuluk. Özenle ayrılmış tümör örnekleri üzerinde hedefe yönelik protein ölçümleri kullanarak iyi yanıt verenlerle vermeyenleri karşılaştırdılar. Tedavi öncesinde bu iki grup arasında farklılaşan 14 protein buldular. Bir yüzey proteini olan CD44 öne çıktı: daha yüksek CD44 düzeylerine sahip tümörler sintilimab bazlı tedaviye daha iyi yanıt eğilimindeydi. Tedaviden sonra, bağışıklık aktivitesi ve DNA onarımıyla ilişkili pek çok protein yanıt verenlerde azalmıştı; bu da kombinasyon tedavisinin kanserin destek sistemlerini başarılı bir şekilde bozduğunu ve yerel bağışıklık manzarasını yeniden şekillendirdiğini düşündürüyor.
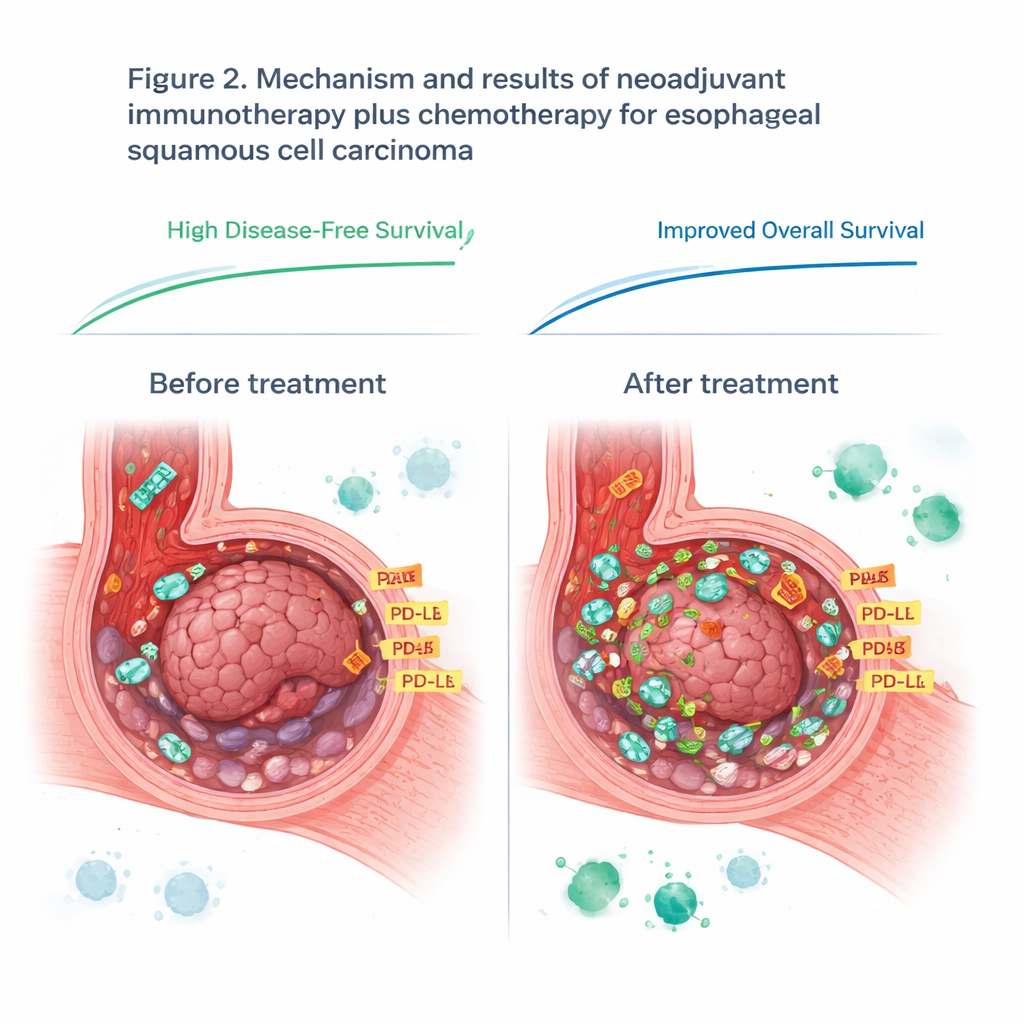
Popüler Bir Bağışıklık İşaretçisini Yeniden Düşünmek
Çalışma ayrıca PD-L1’i, yani hangi hastaların immün kontrol noktası ilaçlarından fayda görebileceğini belirlemede sıklıkla kullanılan bir proteini de inceledi. Tedavi öncesi, PD-L1 düzeyleri hangi hastanın iyi gideceğini tahmin etmedi; bu, bu kanser türünde mevcut uygulamaya meydan okuyor. Bununla birlikte, tedavi sırasında her hastada PD-L1 düzeyleri yükseldi; muhtemelen aktive olmuş bağışıklık sistemi tümörü inflamatuar sinyallerle doldurduğu için. Tedavi sonrası, kalan tümör dokusundaki daha yüksek PD-L1 düzeyleri immünoterapinin ne kadar etkili olduğuyla daha yakından ilişkiliydi. Bu durum, zamanlamanın önemli olduğunu öne sürüyor: tedavi öncesi tek bir PD-L1 ölçümü, bağışıklık sistemi devreye girdiğinde ortaya çıkan kritik değişiklikleri kaçırabilir.
Bu Hastalar ve Gelecek İçin Ne Anlama Geliyor
İleri özofagus kanseri nedeniyle ameliyatla karşı karşıya olan insanlar için bu çalışma iki ümit verici mesaj sunuyor. Birincisi, ameliyattan önce sintilimab ile kemoterapinin birleştirilmesi tümörleri daha derin şekilde küçültüyor ve tehlikeli yan etkiler eklemeden uzun vadeli sağkalım şansını artırabilir. İkincisi, çalışma tümörün ve mikroçevresinin sabit olmadığını; tedaviyle takip edilebilecek şekilde yeniden şekillendiğini gösteriyor; PD-L1 ve CD44 gibi proteinler bu değişikliklerin izlenmesine olanak tanıyabilir. Gelecekte, bu tür moleküler parmak izleri doktorların terapileri gerçek zamanlı seçmesine ve ayarlamasına yardımcı olabilir; bağışıklık sistemini görmezden gelen daha fazla “soğuk” tümörü güçlü, kalıcı bir bağışıklık saldırısına davet eden “sıcak” tümörlere çevirmek mümkün olabilir.
Atıf: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
Anahtar kelimeler: özofagus kanseri, immünoterapi, neoadjuvan tedavi, PD-1 inhibitörleri, tümör mikroçevresi