Clear Sky Science · tr
Algoritma destekli bireyselleştirilmiş tedavi tasarımı, üçlü negatif meme kanseri fare modelinde sağkalımı iyileştiriyor
Daha Akıllı Kemoterapinin Önemi
Kemoterapi yaşam kurtarıyor, ancak hâlâ çoğunlukla “tek beden herkese uyar” yaklaşımıyla uygulanıyor: benzer kanseri olan herkes genellikle aynı ilaç dozunu aynı takvimle alıyor. Bu bazı kişiler için ağır yan etkilere, bazıları içinse yetersiz faydaya yol açabiliyor. Burada anlatılan çalışma basit ama güçlü bir soruyu gündeme getiriyor: ya bir termostatın evi ısıtırken yaptığı gibi, kemoterapiyi her bireye gerçek zamanlı olarak ayarlayan bilgisayar algoritmaları kullanabilseydik? Agresif bir meme kanserinin gelişmiş bir fare modelini kullanarak araştırmacılar, böyle uyarlanmış dozlamanın sağkalımı uzatabileceğini ve ilaç direncinin gelişimini sınırlayabileceğini gösteriyor.
Rutin Kanser İlaç Takvimlerinin Sorunu
Bugün birçok hasta, tolere edebilecekleri en yüksek kemoterapi dozunu sabit aralıklarla alıyor. Bu sözde maksimum tolere edilebilir doz protokolü, belirli bir tümörün ne kadar hızlı büyüdüğünü, bir hastanın ilacı nasıl işlediğini veya o tümörün zaman içindeki tepkisini hesaba katmıyor. Sonuç olarak, tümörler başlangıçta küçülebilir ama daha sonra kendilerinin daha dirençli versiyonları olarak geri dönebilir; hastalar ise güçlü yan etkilerin yükünü çekmek zorunda kalır. Daha küçük, daha sık dozlar kullanan “metronomik” kemoterapi gibi önceki geliştirme çabaları klinik çalışmalarda karışık sonuçlar verdi ve doz ve zamanlamayı nasıl en iyi seçeceğimizi netleştirmedi. Kemoterapiyi daha akılcı, kişiselleştirilmiş bir şekilde planlamaya açık bir ihtiyaç var.
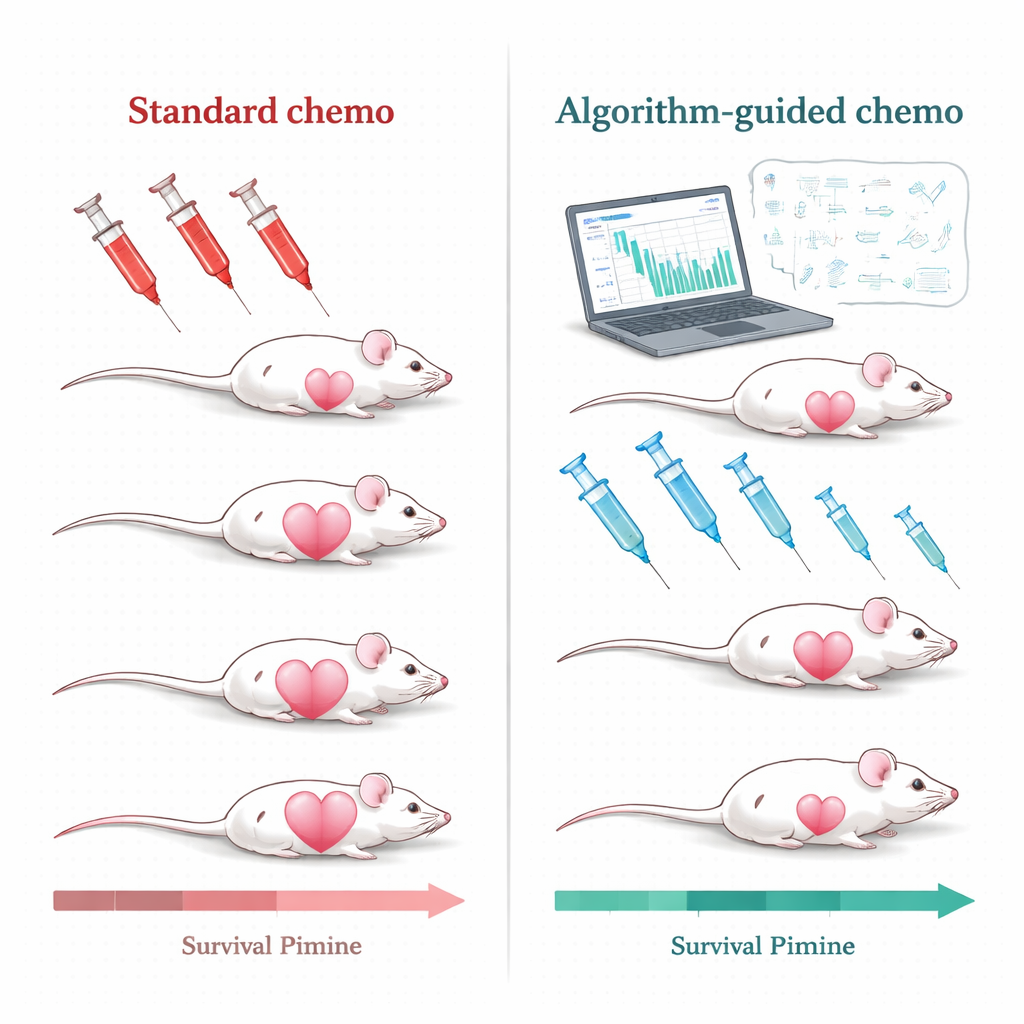
Tedaviyi Uyarlamak İçin Algoritmaların Kullanılması
Araştırma ekibi bu meydan okumayı, insanlarda özellikle tedavisi zor olan ve hâlâ neredeyse tamamen kemoterapiye dayanan üçlü negatif meme tümörleri taşıyan farelerde ele aldı. Farelere yaygın olarak kullanılan bir ilaç formülasyonu olan pegile liposomal doksorubisin verildi. Tümörler belirli bir büyüklüğe geri döndüğünde yalnızca yüksek doz tekrar etmek yerine, bilim insanları tümörün nasıl büyüdüğünü, tedavi altında nasıl gerilediğini ve ilacın kan dolaşımında nasıl hareket ettiğini tanımlayan matematiksel modeller kurdu. Ardından bu modellere basit, klinik olarak gerçekçi ölçümler beslediler: tekrarlanan tümör boyutu okumaları ve kandaki ilaç düzeyleri. Bu girdilerden, bir bilgisayar algoritması her fare için kişiselleştirilmiş tedavi planları üretti.
Bilgisayara Yardım Ettirmenin İki Yolu
Çalışma, algoritma destekli tedavi tasarımının iki çeşidini test etti. Bir yaklaşımdaki PDPK adlı yöntemde, bilgisayar erken verileri kullanarak 30 günlük, nispeten küçük, tekrarlayan dozlardan oluşan bir takvim tasarladı; amaç kanda ilacın düzeyini sabit ama düşük tutmaktı—tümörü kontrol edecek kadar yüksek, ancak toksisiteyi sınırlayacak kadar düşük. İkinci yaklaşımda, model öngörülebilir kontrol (model predictive control) olarak adlandırılan yöntemde algoritma her gün en son tümör ölçümüne göre planı güncelleştirdi ve dozu tümörü sürekli aşağı itmek için ayarladı. Her iki yöntem de aynı temel fikre dayanıyordu: tümör taşıyan farenin gerçekçi bir “dijital ikizini” kullanıp olası birçok dozlama düzenini önden simüle etmek ve güvenlik kısıtları altında en iyi çalışması muhtemel olanları seçmek.
Daha Uzun Sağkalım ve Daha Az İlaç Direnci
Araştırmacılar bu algoritma rehberli rejimleri standart yüksek doz, tümör tetiklemeli protokolle karşılaştırdıklarında farklar çarpıcıydı. Geleneksel tedavi altında tümörler genellikle başlangıçta keskin bir şekilde küçüldü, ancak sonunda geri döndü ve tekrarlanan büyük dozlar ilaç dirençli hastalık gelişimini teşvik etti. Buna karşın, algoritma tarafından tasarlanan tedavilerin çoğu tümörleri çok daha sıkı kontrol altında tuttu, nüks süresini uzattı ve birçok durumda çalışma süresi boyunca belirgin direnç belirtilerini önledi. Düzineleceği kadar farede hem PDPK hem de model öngörüsel kontrol grupları, standart takvimdeki hayvanlardan önemli ölçüde daha uzun yaşadı; birkaç algoritma tabanlı strateji güçlü, istatistiksel olarak anlamlı sağkalım artışları gösterdi.
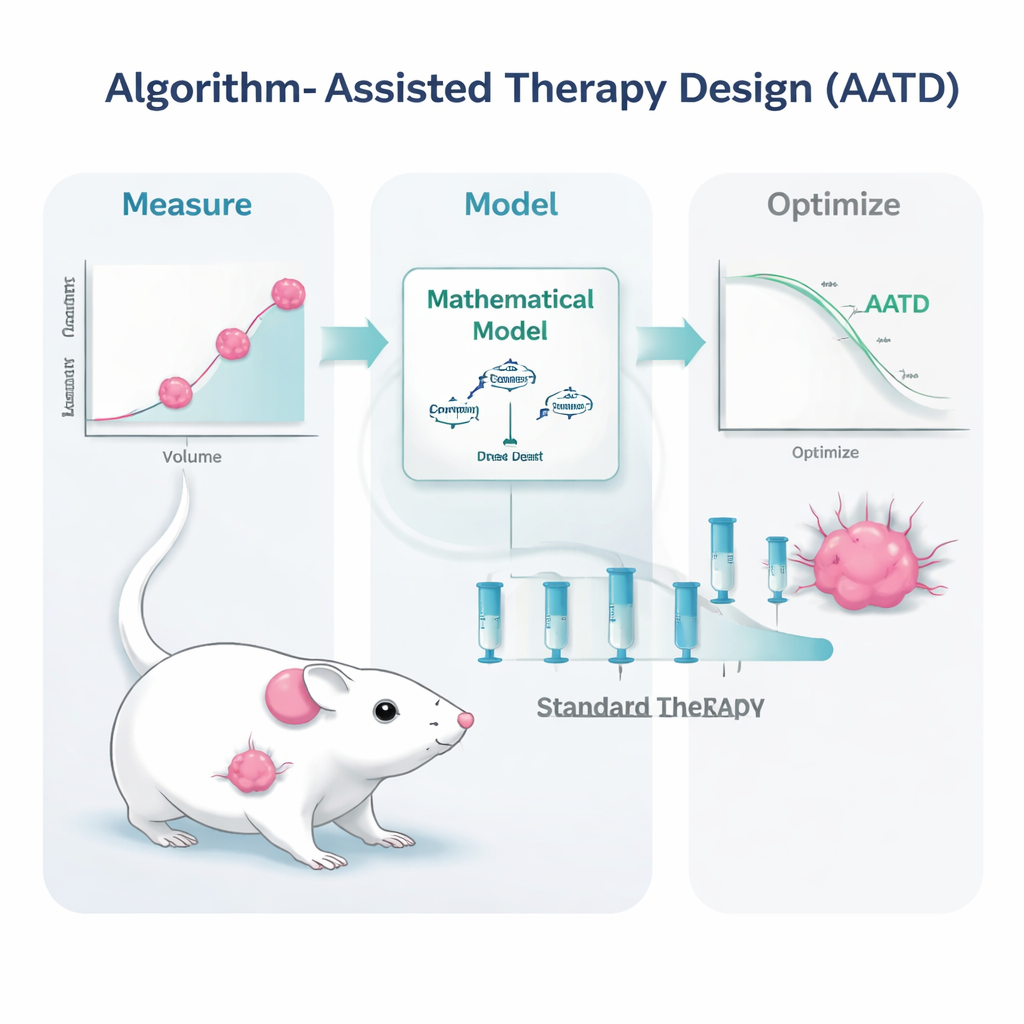
Gelecekteki Hastalar İçin Anlamı Ne Olabilir?
Bu çalışma farelerde yapılmış olsa da kilit bileşenleri—tümör boyutunu ölçmek, kandaki ilaç düzeylerini izlemek ve bilgisayar modelleri çalıştırmak—modern görüntüleme ve laboratuvar araçlarıyla insan hastalarda zaten mümkün. Çalışma, "Standart doz nedir?" yerine doktorların bir gün "Bu hastanın kendi tümör davranışı ve ilacı işleme biçimi göz önüne alındığında şu an için hangi doz ve zamanlama en iyi sonucu verir?" diye sorabileceğini öne sürüyor. Daha sık ölçüm yapılması gerekliliği ve esnek dozlamanın lojistiği gibi pratik engeller devam etse de mesaj açık: kemoterapi kaba ve tek tip olmak zorunda değil. Algoritmaların yardımıyla daha hassas, uyarlanabilir bir araca dönüştürülebilir ve hastalara agresif kanserlerin uzun vadeli kontrolü için daha iyi bir şans sunabilir.
Atıf: Gombos, B., Léner, V., Drexler, D.A. et al. Algorithm-assisted individualized therapy design improves survival in a mouse model of triple-negative breast cancer. npj Precis. Onc. 10, 84 (2026). https://doi.org/10.1038/s41698-025-01245-5
Anahtar kelimeler: kişiselleştirilmiş kemoterapi, üçlü negatif meme kanseri, algoritma destekli tedavi, matematiksel tümör modellemesi, doksorubisin dozlaması