Clear Sky Science · tr
Uzamsal transkriptomik, küçük hücreli akciğer kanserinde moleküler heterojenlik ve alt tipe özgü terapötik hedefleri ortaya koyuyor
Bu akciğer kanseri çalışması neden önemli
Küçük hücreli akciğer kanseri, çoğunlukla sigara öyküsü olan insanları etkileyen ve kemoterapiden sonra sıklıkla hızla nükseden en öldürücü kanser türlerinden biridir. Klinik olarak tüm küçük hücreli akciğer kanserlerinin aynı davranmadığı bilinse de, farklı kanser hücresi tiplerinin ve bağışıklık hücrelerinin her bir tümör içinde nasıl düzenlendiğini görmeye yarayan araçlar eksikti. Bu çalışma, tümör lamı üzerinde binlerce küçük noktada gen etkinliğini okuyan yeni bir teknolojiyi kullandı ve her örneğin “moleküler haritasını” çıkardı. Bunu özel bilgisayar analizleriyle eşleştirerek, daha kesin ve alt tipe özgü tedavilere işaret edebilecek gizli desenleri ortaya koydular.
Tümörleri yerinde haritalamak
Araştırma ekibi, herhangi bir ilaç alımından önce cerrahi uygulanmış, sınırlı evre küçük hücreli akciğer kanseri olan 21 hastanın tümör örneklerini inceledi. Doku öğütülüp tüm mekansal bilgi kaybedilmek yerine, tanımlanmış birçok noktada hangi genlerin aktif olduğunu ölçen uzamsal transkriptomik uygulandı. Her nokta özgün konumunda kaldığı için bilim insanları gen etkinliğini kanser hücrelerinin, normal hücrelerin ve bağışıklık hücrelerinin fiziksel yerleşimi ile ilişkilendirebildi. Buna ek olarak iki önemli araç daha kullandılar: tümör hücrelerinin komşu dokuya ne kadar derinlemesine nüfuz ettiğini nicelleştiren yeni bir “Edgeindex” skoru ve hangi noktaların tümör, hangi noktaların tümör olmayan doku olduğunu otomatik işaretlemek için bir yapay sinir ağı—makine öğrenmesi biçimi.
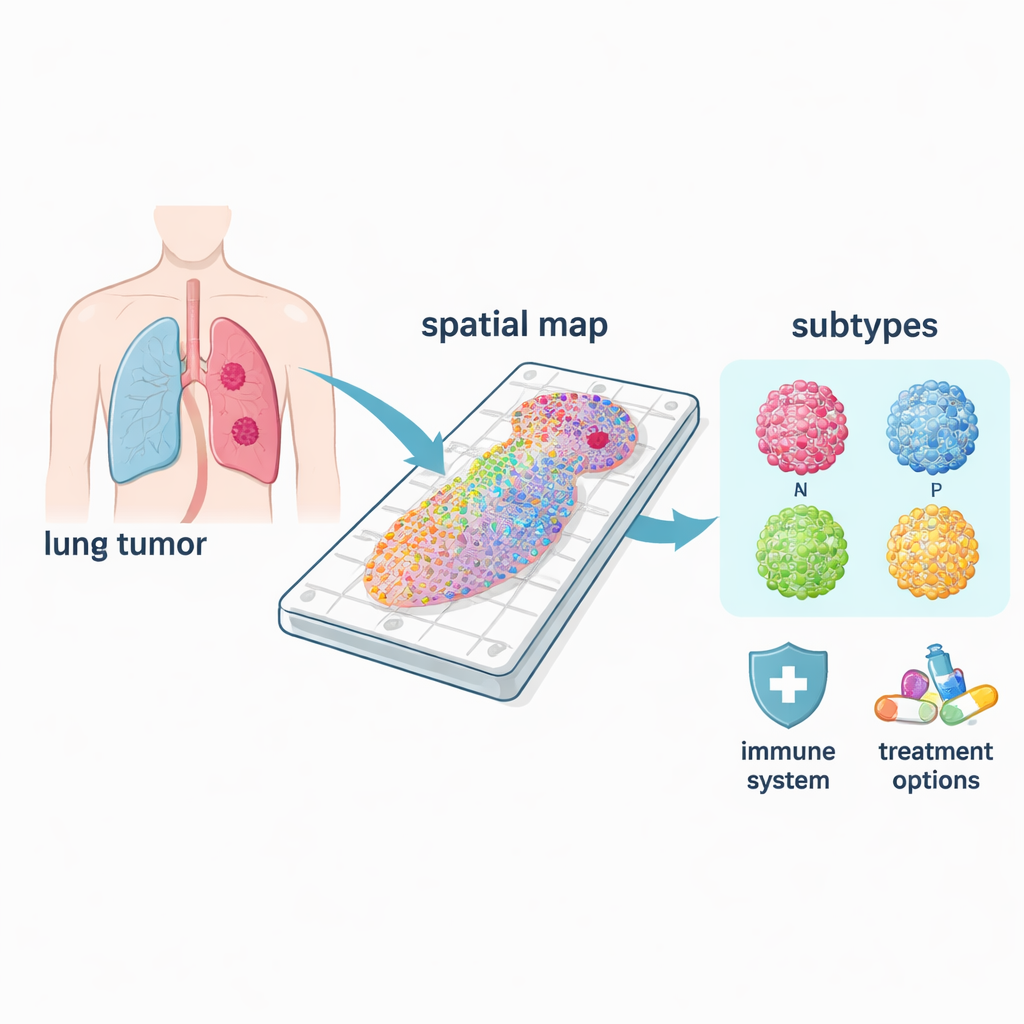
Tek bir hastalık içinde farklı kanser tipleri
Küçük hücreli akciğer kanseri tek bir hastalık değildir; en az dört ana moleküler alt tipi içerir ve bunlar sıklıkla belirleyici kontrol genlerinin adlarıyla ASCL1, NEUROD1, POU2F3 ve YAP1 olarak anılır. Uzamsal haritalarını kullanarak araştırmacılar her alt tipin tümör içinde nerede baskın olduğunu ve biyolojilerinin nasıl farklılaştığını görebildiler. Yaygın olan ASCL1 ve NEUROD1 formları hücre bölünmesi programlarıyla güçlü şekilde ilişkiliydi; bu da onların yüksek proliferatif özellikleriyle uyumludur. Buna karşılık POU2F3 bölgeleri bağışıklık ilişkili yolaklarla bağlantılıydı, YAP1 alanları ise metabolizma ve doku yeniden şekillenmesiyle ilişkili sinyaller gösterdi; bu özellikler yayılma ve tedavi direnciyle bağlantılı olabilir. Bu desenler uzay içinde çözüldüğü için yöntem, karışık bir tümörde gerçek “sürücü” alt tipi belirleyebiliyor; toplu testlerin sıklıkla kaçırdığı bir durum.
Saldıran kenar ve bağışıklık değişimi
Çalışmanın merkezî yeniliklerinden biri olan Edgeindex, tümör hücrelerinin çevreleyen tümör olmayan doku ile ne kadar karıştığını yakalıyor. Düşük skorlar kompakt, iyi sınırlanmış tümörleri yansıtarken yüksek skorlar dağılan adacıklar ve düzensiz, invazif sınırları gösteriyor. Yüksek Edgeindex’e sahip tümörler ekstraselüler matriks, metastaz ve hücre ölümü ile ilgili gen programları açısından zengindi. Ayrıca çarpıcı şekilde değişmiş bir bağışıklık manzarası sergilediler: yardımcı T hücreleri ve diğer adaptif bağışıklık elemanları daha azdı; oysa belirli doğal öldürücü hücreler ve monositler gibi daha fazla innat hücre mevcuttu. Yazarlar bunu tümörün hassas, hedefe yönelik bağışıklık tepkilerini uzaklaştırdığı ve geride daha az etkili, büyük ölçüde innat bir savunma bıraktığı bir “immünolojik niş yeniden yapılanması” olarak yorumluyorlar; bu savunma kanseri tam olarak kontrol edemiyor.
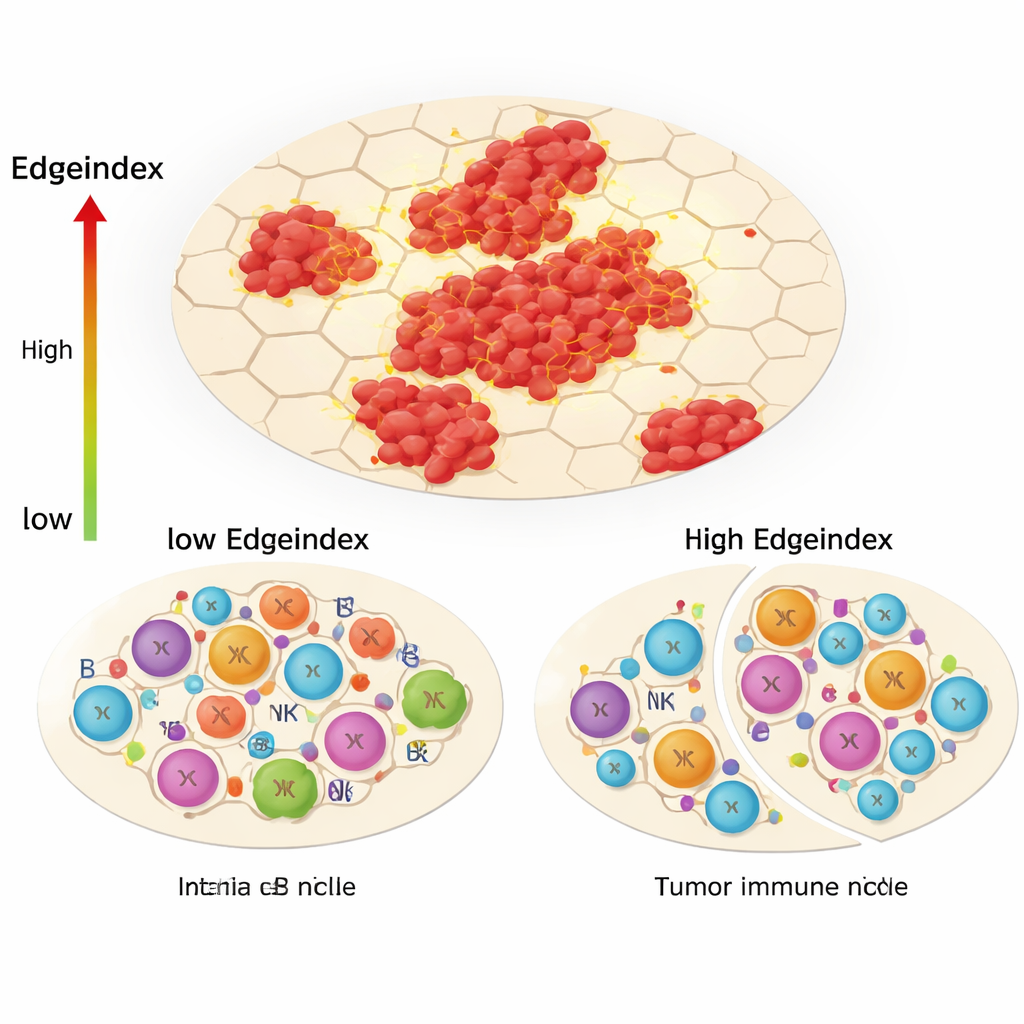
Tümör içinde ve çevresinde gizli çeşitlilik
Alt tip ve invazyon desenlerinin ötesinde, uzamsal veriler hem kanser hücresi popülasyonlarının hem de çevreleyen mikroçevrelerin dahili olarak çeşitli olduğunu ortaya koydu. Her tümör içinde noktaları kümeleyerek ekip, kanser bölgelerinde ve yakınlardaki tümör olmayan dokuda kaç farklı gen‑ekspresyonu mahallesinin bulunduğunu saydı. Tümör içindeki daha yüksek çeşitlilik bağışıklık ilişkili yolaklarla ilişkilendirildi; çevreleyen dokudaki belirli desenler ise hücre döngüsü aktivitesi ve genetik düzenlemeyle bağlantılıydı. Araştırmacılar ayrıca bilinen sinyal moleküllerini kullanarak farklı bölgelerin ne kadar güçlü “iletişim kurduğunu” da incelediler. Bölgeler arasında daha yoğun iletişime sahip tümörler genellikle daha güçlü bağışıklık ilişkili sinyaller gösteriyordu; bu da bağışıklık etkinliği ile tümör büyümesinin uzay içinde sıkı bir şekilde iç içe olduğunu pekiştiriyor.
Tümör gelişimini zaman içinde izlemek
Hastalığın ilerlemesiyle birlikte tümör hücrelerinin nasıl değiştiğini yaklaşık olarak çıkarmak için ekip, gen etkinliğine dayalı olarak hücreleri gelişimsel bir yol boyunca sıralayan bir “pseudotime” analizi gerçekleştirdi. Örnekler arasında tekrar tekrar bu yörüngelerin merkezinde bir gen, UCHL1, öne çıktı. Yüksek UCHL1 seviyeleri tümör noktalarında güçlü hücre döngüsü aktivitesiyle çakışırken, daha düşük seviyeler bağışıklık ve hücre ölümü yolaklarıyla ilişkiliydi. UCHL1 daha önce agresif akciğer kanserleriyle bağlantılı bulunan nöral‑tip bir protein olduğu için, bu bulgular özellikle küçük hücreli akciğer kanserini yönlendiren nöroendokrin‑benzeri hücreler için faydalı bir ilaç hedefi olabileceği şeklindeki olasılığı güçlendiriyor.
Bu hastalar için ne anlama geliyor
Açık ifadeyle, bu çalışma küçük hücreli akciğer kanserinin düz mikroskop lamlarını, farklı kanser alt tiplerinin nerede bulunduğunu, ne kadar agresifçe nüfuz ettiklerini, çevreleriyle nasıl iletişim kurduklarını ve bağışıklık sisteminin nasıl yanıt verdiğini veya neden başarısız olduğunu gösteren zengin, katmanlı haritalara dönüştürüyor. Yeni Edgeindex skoru ve haritalama yaklaşımı hangi tümörlerin özellikle infiltratif olduğunu ve sınırda hangi bağışıklık hücrelerinin mevcut veya eksik olduğunu vurguluyor. Bu uzamsal desenleri DLL3, BCL‑2, AURKA, IGF‑1R/PARP veya immün kontrol noktalarını hedef alan ilaçlar gibi alt tipe özgü zayıflıklarla ilişkilendirerek çalışma, her hastaya uygun bir tedavi stratejisi eşleştirmeye bir adım daha yaklaştırıyor. Bu araçların daha büyük çalışmalarda test edilmesi gerektiği halde, acil olarak daha iyi seçeneklere ihtiyaç duyan bir kanser türünde daha kesin ve potansiyel olarak daha etkili tedavilere yönelik bir plan sunuyorlar.
Atıf: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
Anahtar kelimeler: küçük hücreli akciğer kanseri, uzamsal transkriptomik, tümör heterojenitesi, tümör bağışıklık mikroçevresi, kesin onkoloji