Clear Sky Science · tr
Küçük hücreli akciğer kanserinde (SCLC) bağışıklık mimarisinin hesaplamalı patoloji özellikleri klinik olarak anlamlı sonuçları öngörür
Vücudun savunucuları akciğer kanserinde neden önemli
Küçük hücreli akciğer kanseri, genellikle hızla yayılan ve tedavi sonrasında tekrar eden en agresif akciğer kanserlerinden biridir. Doktorlar tümörleri mikroskop altında görebilir, ancak kanser hücreleri ile bağışıklık hücrelerinin birbirine nasıl konumlandığına dair ince desenler gözle değerlendirmeyle çok karmaşıktır. Bu çalışma, rutin biyopsi lamlarından bu gizli desenleri okuyan ve bunları hastaların ne kadar süre yaşayacağı ile kemoterapiye nasıl yanıt verebileceklerini tahmin etmek için kullanan PhenopyCell adlı bilgisayar destekli bir yöntemi tanıtıyor. Hastalar ve aileleri için bu tür bilgiler, bir kerelik, herkese aynı uygulanan bir plandan ziyade tedaviyi kişiselleştirmeye yardımcı olabilir.
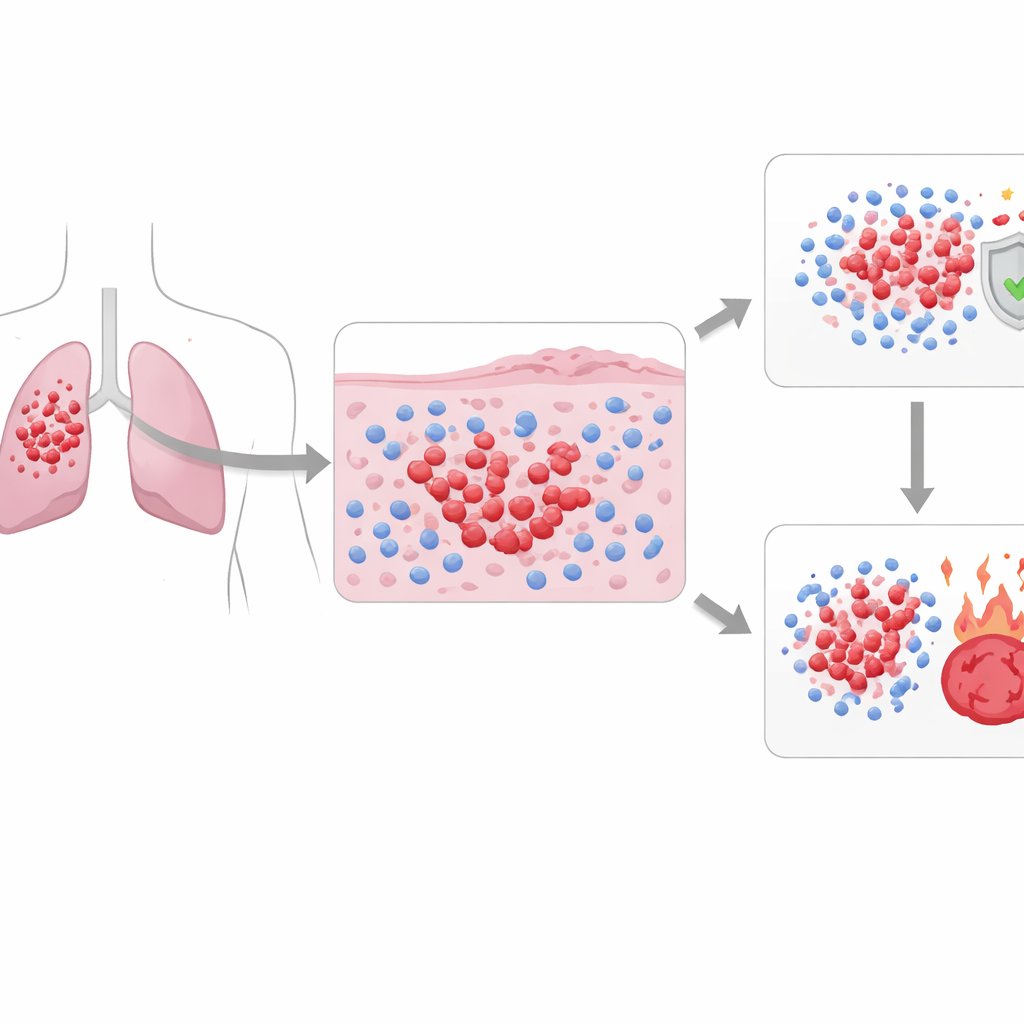
Ölümcül bir akciğer kanserine daha yakından bakmak
Küçük hücreli akciğer kanseri tüm akciğer kanserlerinin yaklaşık %15’ini oluşturur, ancak hızlı büyüme ve yayılma nedeniyle ölümlerde büyük paya sahiptir. Genellikle tek bir ışınlama alanına sığabilecek “sınırlı” hastalık ve daha geniş yayılan “yaygın” hastalık olarak sınıflandırılır. Standart ilk tedavi güçlü platin bazlı kemoterapiyi, bazen immünoterapi ile kombinasyonunu içerir. Birçok tümör başlangıçta kaybolur gibi görünse de kanser sık sık bir yıl içinde geri döner ve uzun dönemde hayatta kalan hasta sayısı onda birden azdır. Tümör büyüklüğü, yayılma ve temel mikroskopik görünüm gibi mevcut testler aynı ilaçlarla bazı hastaların neden daha iyi sonuç aldığını açıklayamıyor.
Bilgisayarları tümör mahallelerini okumaya öğretmek
Araştırmacılar, standart boyanmış doku lamlarını hücre “mahallelerinin” ayrıntılı bir haritasına dönüştürmek için PhenopyCell’i geliştirdi. Mevcut derin öğrenme araçlarını kullanarak, önce bir bilgisayara üç ABD merkezinde tedavi edilen 281 hastanın dijital biyopsi görüntülerinde bireysel tümör hücrelerini ve bağışıklık hücrelerini bulmayı ve işaretlemeyi öğrettiler. Ardından her lamı tümör, yakın doku ve uzak olmayan tümör bölgelerine böldüler ve yüzün üzerinde sayısal özellik hesapladılar. Bu özellikler, örneğin bağışıklık hücrelerinin tümör kümelerinin etrafında ne kadar yoğunlaştığını, bağışıklık hücrelerinin kanser hücrelerinden ne kadar uzakta olduğunu, hücre karışımının ne kadar çeşitli olduğunu ve hücrelerin lam boyunca ne kadar düzenli dizildiğini tanımlar.
Hayatta kalma ve ilaç yanıtıyla ilişkilendirilen gizli desenler
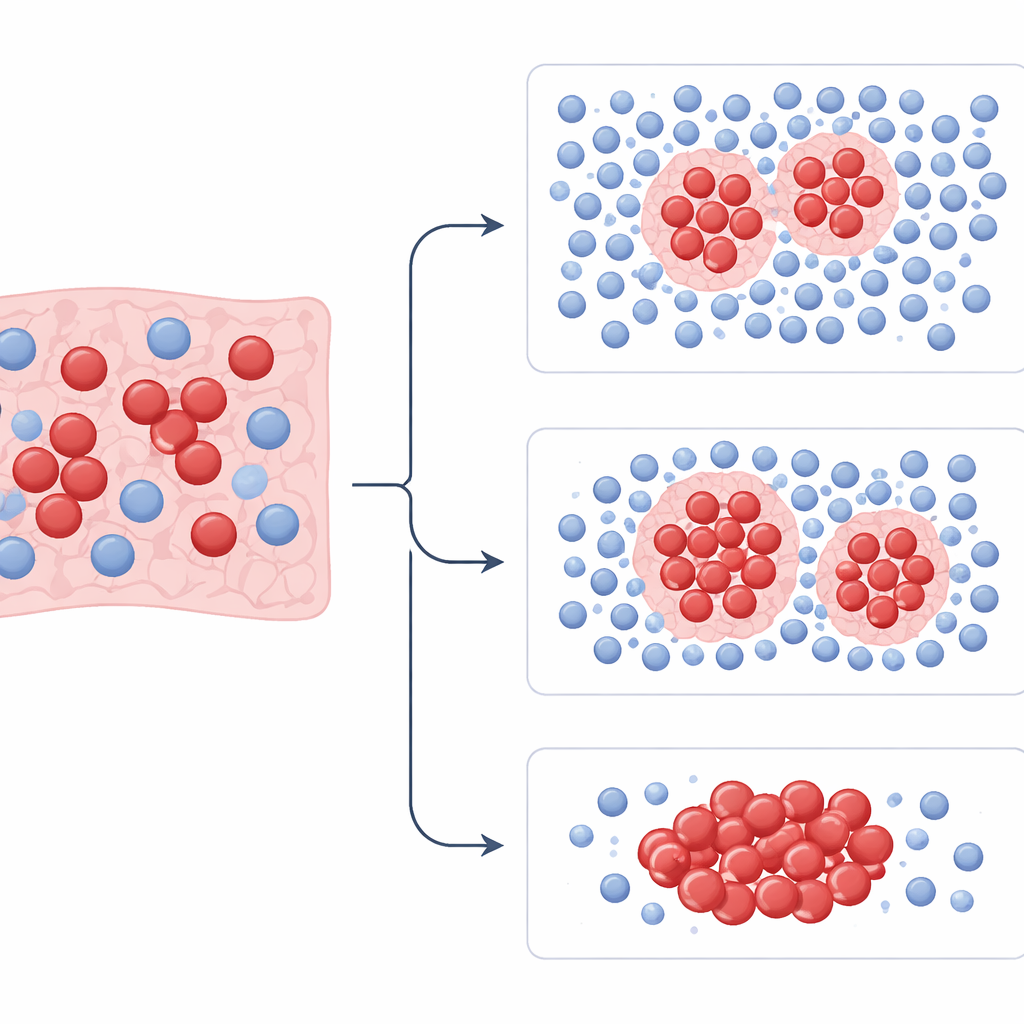
Bu ölçümlerle ekip, hastaları daha yüksek ve daha düşük riskli gruplara ayırmak ve kimin platin kemoterapiye yanıt vereceğini tahmin etmek için modeller eğitti. Modelleri bir hastanenin vakaları üzerinde eğitip ardından diğer iki hastanenin hastalarında test ettiler. Tüm veri setlerinde PhenopyCell tarafından yakalanan desenler genel sağkalım ve kemoterapinin işe yarayıp yaramadığı ile güçlü bir şekilde ilişkilendirildi. Tümör kümelerini sıkı bir şekilde çevreleyen çok sayıda düzenli bağışıklık hücresi cebine sahip hastalar genellikle daha uzun yaşadı. Dağınık veya seyrek bağışıklık hücrelerine ve çok düzensiz tümör hücresi dağılımına sahip olanlar ise daha agresif hastalık ve kötü sonuçlarla daha fazla karşılaştı. Bu bağlantılar yaş, cinsiyet ve diğer klinik faktörler dikkate alındığında bile geçerliydi ve hem sınırlı hem de yaygın evrelerde gözlendi.
Siyah kutuların ve rutin mikroskop kontrollerinin ötesinde
Çalışma ayrıca PhenopyCell’i daha yeni “foundation” yapay zeka modelleri ve tümör içine sızan lenfositler olarak adlandırılan geleneksel bağışıklık hücresi ölçümleriyle karşılaştırdı. Bazı büyük derin öğrenme modelleri orijinal eğitim grubunda yüksek doğruluk gösterse de dışarıdaki hastalarda tutarsız performans sergiledi; bu da kararlılık hakkında endişe uyandırdı. Bilgisayar tarafından tahmin edilen veya bir patolog tarafından değerlendirilen basit bağışıklık hücresi sayımları da güvenilir şekilde sağkalımı öngörmedi. Buna karşılık, PhenopyCell’in bağışıklık ve tümör hücrelerinin mekânda nasıl düzenlendiğine, sadece sayısına değil de odaklanması daha güvenilir ve yorumlaması daha kolay sinyaller sağladı. Kullandığı özellikler, bağışıklığın dışlanması, doku ölümü bölgeleri ve değişken tümör şekilleri gibi biyolojik fikirlerle doğrudan ilişkilendirilebilir.
Bu hastalar için ne anlama gelebilir
Uzman olmayan bir kişi için ana mesaj, tümörün “mimarisi”—kanser hücrelerinin ve vücudun savunucularının savaş alanını nasıl paylaştığı—hastalığın nasıl davranacağı ve tedaviye nasıl yanıt vereceği hakkında önemli ipuçları içerir. PhenopyCell, bu ipuçlarının standart bakım sırasında zaten alınan rutin biyopsi lamlarından, ekstra prosedür gerektirmeden çıkarılabileceğini gösteriyor. Çalışma retrospektif ve ağırlıklı olarak yalnızca kemoterapi alan hastalara dayansa da, gelecekteki araçların hangi hastaların en yüksek riske sahip olduğunu, kimlerin daha agresif veya yeni tedavilerden yarar görebileceğini ve kimlerin gereksiz yan etkilerden kaçınabileceğini belirlemeye yardımcı olabileceğini öne sürüyor. Böyle bir sistemin günlük kararları yönlendirebilmesi için özellikle modern immünoterapi alan hastalarda daha büyük, ileriye dönük çalışmalara ihtiyaç olacak, ancak bu çalışma küçük hücreli akciğer kanserinde daha kişiselleştirilmiş bakıma doğru açık bir yol çiziyor.
Atıf: Barrera, C., Jain, P., Corredor, G. et al. Computational pathology features of immune architecture predict clinically relevant outcomes in small-cell lung cancer (SCLC). npj Precis. Onc. 10, 119 (2026). https://doi.org/10.1038/s41698-025-01225-9
Anahtar kelimeler: küçük hücreli akciğer kanseri, hesaplamalı patoloji, tümör mikroçevresi, bağışıklık hücresi mimarisi, tedavi yanıtı tahmini