Clear Sky Science · tr
Kansere özgü olarak eksprese edilen EGFR'yi humanize edilmiş monoklonal antikorla hedeflemek
Kanserin Gizli İşaretlerini Bulmak
Kanser tedavileri genellikle tümör hücrelerine saldırmak ile sağlıklı dokuları korumak arasında bir denge kurmakta zorlanır. Bu makale, A10 adında, belirli bir biçimdeki büyüme sinyali reseptörünü taşıyan kanser hücrelerini normal hücrelerden ayırt edebilen yeni bir laboratuvar yapımı antikoru tanımlıyor. Bu reseptörün değiştiği veya tümör hücrelerinde aşırı bulunduğu durumda ortaya çıkan bir şekle yönelerek, A10 birçok mevcut seçenekten daha güçlü ve daha seçici olabilecek terapilere kapı aralıyor.
Bu Büyüme Anahtarının Önemi
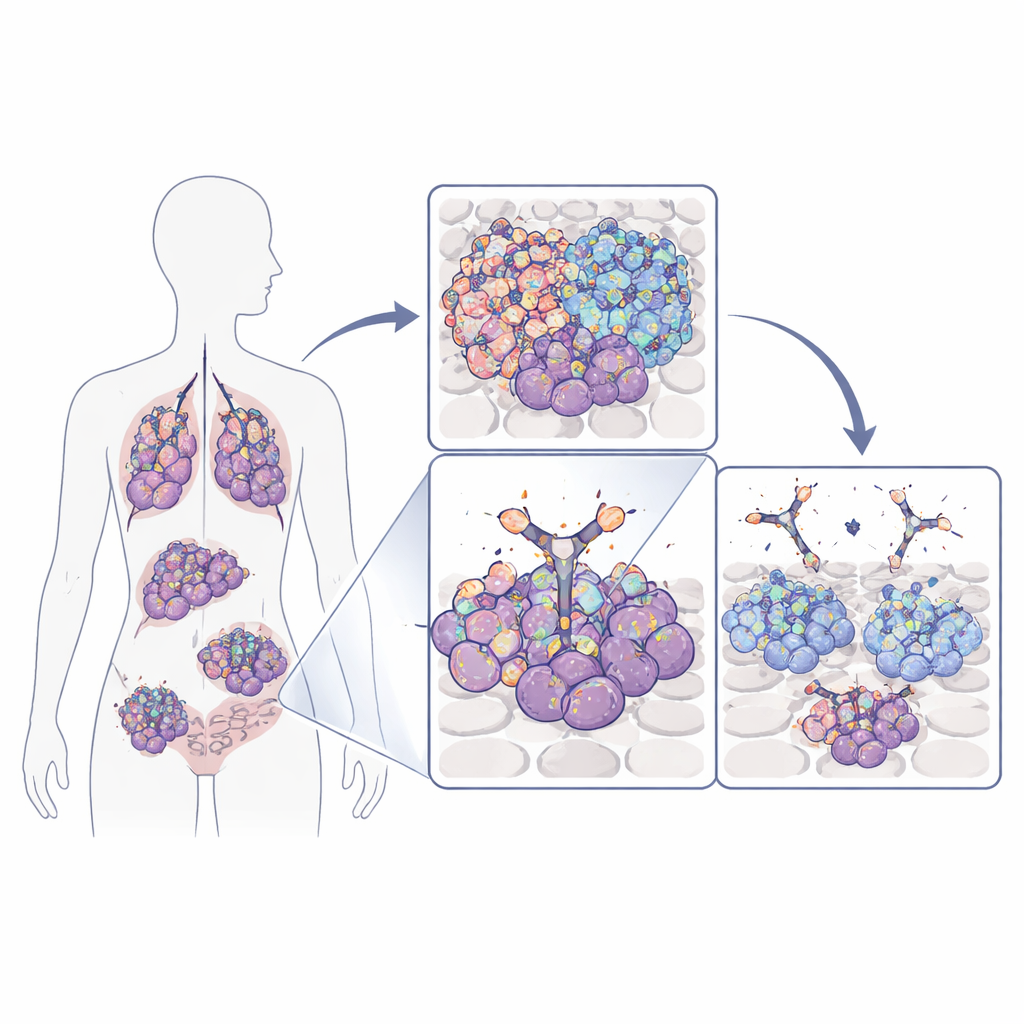
Agresif beyin, akciğer, meme ve kolorektal kanserler dahil birçok tümör, büyümek ve hayatta kalmak için epidermal büyüme faktörü reseptörü (EGFR) adlı yüzey proteinine bağımlıdır. Tümör hücreleri bu reseptörü genini çoğaltarak, mutasyona uğratarak veya sürekli aktif, kısaltılmış bir versiyon olan EGFRvIII'ü üreterek artırabilir. EGFR'yi bloke eden standart ilaçlar sıklıkla reseptörün her yerde bulunan kısımlarını tanıdıkları için hem kanser hücrelerini hem de normal dokuları etkiler. Bu çalışmanın ekibi bunun yerine, EGFR'nin yalnızca kanser hücrelerinde—ya reseptörün anormal derecede fazla bulunması ya da EGFRvIII’de reseptörün kısalması nedeniyle—açıkça ortaya çıkan küçük bir döngüsüne odaklandı. Bu döngü, ilke olarak çok daha güvenli bir şekilde hedeflenebilecek kanser‑özgü bir “bayrak” gibi davranır.
Fare Antikorunu İnsan İlacına Dönüştürmek
Araştırmacılar önceden, kanser eksprese edilen EGFR üzerindeki bu açık döngüyü tanıyan 40H3 adlı bir fare antikoru keşfetmişlerdi. Ancak fare antikorları hastalara tekrar tekrar verildiğinde bağışıklık reaksiyonları tetikleyebilir. Bunu aşmak için ekip, 40H3'ün bağlanmada kritik segmentlerini insan antikor çerçevelerine aşılamak üzere protein mühendisliği yöntemleri kullandı ve on dört “humanize” aday ile bir kimerik referans molekül üretti. Bu varyantları EGFR’yi aşırı üreten kanser hücrelerinde test ettiklerinde üç versiyon özellikle iyi bağlandı ve A10, normal hücrelerdeki ılımlı EGFR seviyelerini göz ardı ederken en güçlü bağlanıcı olarak öne çıktı. Farklı EGFR mutasyonlarına ve kopya sayılarına sahip geniş bir tümör hücre hattı panelinde, A10 orijinal fare antikorundan daha yüksek bağlanma gösterdi ve malign hücrelere karşı güçlü bir tercihini korudu.
Antikorun Hedefini Nasıl Tuttuğunu Görmek
A10'ın neden bu kadar seçici olduğunu anlamak için ekip, antikorun aktif kısmının EGFR döngüsüne bağlı hâlinin yüksek çözünürlüklü 3B yapısını çözdü. Döngü, bir disülfid bağı tarafından stabilize edilen sıkı bir saç tokası (hairpin) şeklinde katlanır ve A10 bu şekli kolları arasındaki bir olukta kavrar; çok sayıda yüklü temas onu sabitlemektedir. Bu yapıyı tam EGFR molekülünün bilinen şekilleriyle karşılaştırmak, önemli bir içgörü sağladı: normal EGFR'nin hem inaktif “bağlanmış” (tethered) hem de aktif dimer formlarında döngü büyük ölçüde gömülü veya komşu domainler tarafından kısmen korunmuştur. Bu, A10'ın tipik, ılımlı düzeyde eksprese edilen reseptörlerde bağlanma bölgesine kolayca erişemeyeceği anlamına gelir. Buna karşın kanser‑özgü EGFRvIII varyantında reseptörün ön kısmı eksiktir ve döngü yüksek oranda açığa çıkarak erişilebilir olur. Veriler A10'ın başlıca belirli geçiş şekillerindeki ve tümör hücrelerinde tercihli olarak ortaya çıkan aşırı kalabalık veya kısaltılmış formlardaki EGFR'yi tanıdığını düşündürmektedir.
Tümör Hücrelerini Öldürmek İçin Antikoru Silahlandırmak
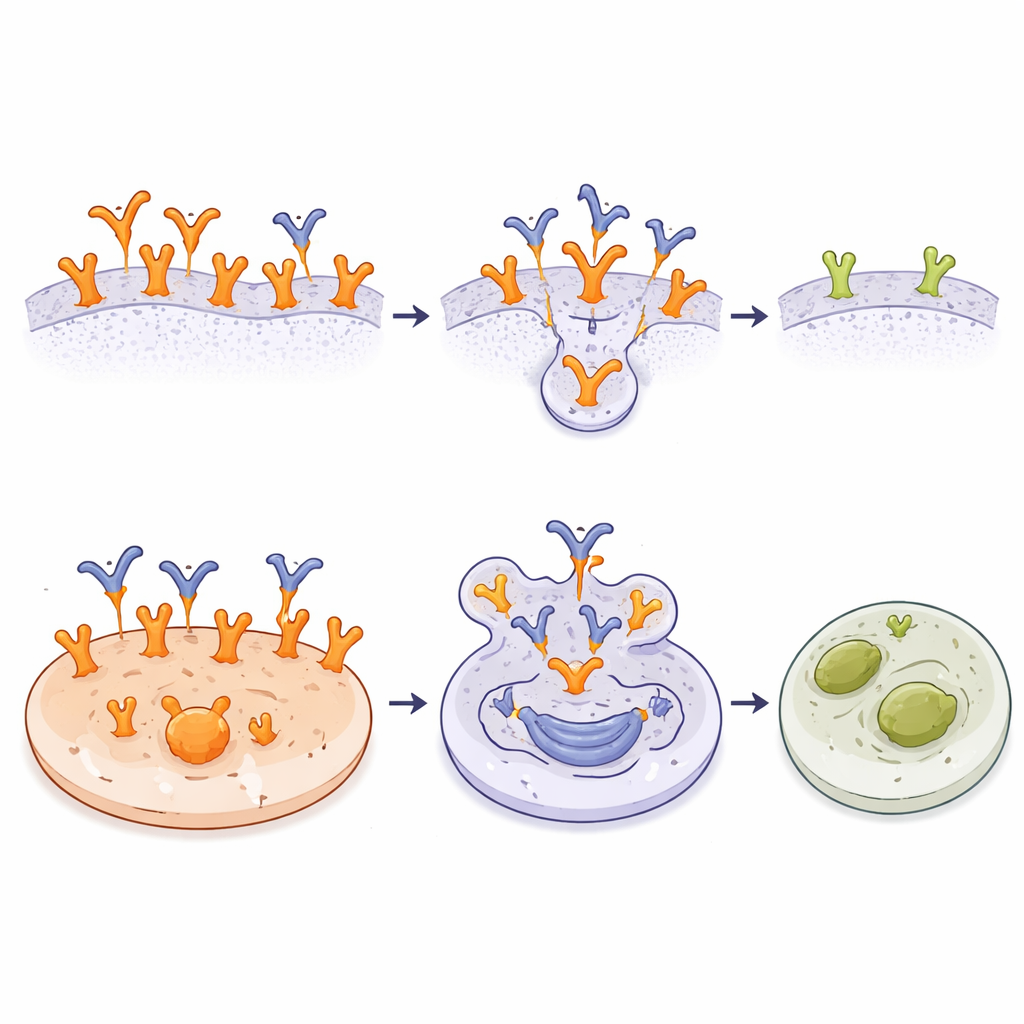
Bir tümör‑özgü bayrağı tanımak kendi başına faydalı olmakla birlikte, araştırmacılar A10'u bir antikor‑ilaç konjugatına (ADC) dönüştürerek daha ileri gittiler. Hücre öldürücü güçlü bir bileşik olan monometil auristatin E (MMAE) kimyasal olarak A10'a, hücre içinde kesilebilen bir bağlayıcı kullanılarak eklendi. Bu A10‑MMAE ADC, konjugatsız antikorla olduğu kadar iyi kanser hücrelerine bağlandı. Çok sayıda hücre hattında yapılan laboratuvar testlerinde, ADC en etkili olduğu durumlar A10 bağlanma bölgelerinin bol olduğu çok yüksek EGFR seviyeli veya EGFRvIII taşıyan tümörlerdi. Bu hücrelerde çok küçük miktarlarda konjugat bile hücre ölümünü tetiklemeye yetti. Daha az A10 hedefi olan veya MMAE'ye karşı doğuştan dirençli tümör hatları daha az etkilendi ve vahşi tip EGFR taşıyan normal fibroblast hücreleri serbest MMAE'ye hassas olmalarına rağmen zarar görmedi. Sonuçlar, seçici bağlanma ile içsel ilaç salınımının toksisitenin keskin bir şekilde kanser hücrelerine odaklanmasını sağlayabileceğini gösteriyor.
Geleceğin Kanser Bakımı İçin Anlamı
Basitçe söylemek gerekirse, bu çalışma EGFR yalnızca kanser‑sürücü bir reseptör gibi görünüp davrandığında “gören” ve sağlıklı dokulardaki gündelik formunu büyük ölçüde görmezden gelen bir antikor inşa etmenin mümkün olduğunu gösteriyor. A10'ın EGFR üzerindeki gizli bir döngüyü tam olarak nasıl tuttuğunu haritalandırarak ve A10 tabanlı bir ilaç konjugatının reseptör‑zengini tümör hücrelerini verimli şekilde öldürebildiğini ancak normal hücreleri koruyabildiğini göstererek, çalışma daha güvenli, yüksek derecede hedefe yönelik terapiler geliştirmek için sağlam bir temel sunuyor. Bu bulgular hastalara da yansırsa, A10'a dayalı gelecekteki tedaviler güçlü ilaçları doğrudan EGFR'ye bağımlı kanserlere taşıyabilir ve geri kalan vücudu büyük ölçüde dokunulmamış bırakabilir.
Atıf: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
Anahtar kelimeler: EGFR, antikor ilaç konjugatı, hedefe yönelik kanser tedavisi, glioblastom, EGFRvIII