Clear Sky Science · tr
Escherichia coli Colicin E9 bağışıklık proteininin Pseudomonas aeruginosa DNA girazı ile etkileşimlerinin incelenmesi: yeni antimikrobiyal stratejiler geliştirmek için ileri hesaplamalı yaklaşım
Bakteriyel Silahları Yeni İlaçlara Dönüştürmek
Antibiyotik direnci yayıldıkça, doktorların tehlikeli enfeksiyonları durdurma seçenekleri azalıyor. Pseudomonas aeruginosa gibi en inatçı suçlular birçok ilaca karşı direnç gösterebiliyor. Bu çalışma, taze fikirler için bakterilerin kendisine bakıyor; bir mikroorganizmanın yerleşik koruyucu proteininin başka bir mikroorganizmadaki hayati bir enzimi devre dışı bırakmak üzere yeniden kullanılmasını araştırıyor. İleri düzey bilgisayar simülasyonları kullanarak, araştırmacılar küçük bir “bağışıklık” proteininin önemli bir bakteri enzimine sıkı şekilde tutunabileceğini gösteriyor ve bu da gelecekteki antimikrobiyaller için yeni bir yolun işaretçisi oluyor.
Ölümcül Bir Toksine Karşı Minik Bir Kalkan
Belirli Escherichia coli suşları, komşu bakterileri öldürebilen güçlü protein toksinleri olan kolisinleri üretir. Kendilerini zehirlenmeden korumak için bu bakteriler aynı zamanda eşleşen bağışıklık proteinleri de üretir. Colicin E9 bağışıklık proteini (genellikle Im9 olarak anılır) gibi bir koruyucu, toksinin kesici domenine kilitlenir ve bunun konağın DNA’sına zarar vermesini engeller. Bu ortaklık çok özgül ve güçlü olduğundan, bilim insanları uzun süredir bunu ayrıntılı biçimde anlamanın zararlı bakterileri kontrol etmenin yeni yollarını ortaya çıkarabileceğini düşünüyor. Bu çalışmada yazarlar, Im9’un ayrıca DNA’sının nasıl büküldüğünü ve kopyalandığını yöneten Pseudomonas aeruginosa’nın hayati bir enzimi olan DNA girazına da tutunup tutunmayacağını araştırıyorlar.
Zor Tedavi Edilen Bir Mikropta Savunmasız Bir Enzimi Hedeflemek
Pseudomonas aeruginosa, zorlu ortamlarda hayatta kalabilen ve birçok ilaca dirençli olan önemli bir hastane patojenidir. DNA girazı, bakterinin uzun DNA zincirlerini düzgün şekilde bükülmüş tutmaktan sorumlu en önemli enzimlerinden biridir, böylece bunlar kopyalanabilir. Bu enzimi bloke etmek bakteriyel büyümeyi durdurabildiği için bazı antibiyotiklerin kanıtlanmış bir hedefidir. Yazarlar, Pseudomonas DNA girazının üç boyutlu yapısını taramak ve bağlanma ortakları için en önemli yüzeydeki amino asit kümeleri olan muhtemel “sıcak noktaları” işaretlemek için bir derin öğrenme aracı kullandılar. Bu bölgeler, normal DNA işleme işleminin gerçekleştiği ve potansiyel bir inhibitörün ideal olarak tutunacağı enzimin aktif ceplerini oluşturur.
Moleküler Bir Tokalaşmanın Simülasyonu
Im9’un bu sıcak noktalara tutunup tutunamayacağını görmek için araştırmacılar, proteinleri 3B yapbozlar gibi sanal olarak “uyduran” moleküler dock programlarına başvurdular. Önce, hem Im9 hem de DNA girazının mevcut yapılarını temizlediler ve tamamladılar; enzimdeki eksik bir döngüyü onardılar ve gerilimli bölgeleri rahatlatmak için kısa simülasyonlar çalıştırdılar. Ardından ClusPro ve LightDock olmak üzere tamamlayıcı iki docking aracı kullanarak çok sayıda aday kompleks ürettiler. Bunlardan en umut verici düzenlemeleri seçip yüzlerce nanosaniye süren uzun moleküler dinamikler simülasyonlarına tabi tuttular. Bu zamana bağlı filmler, iki proteinin bağlandıklarında nasıl ayarladığını, esnediğini ve daha kararlı şekillere nasıl yerleştiğini izlemelerine olanak verdi.
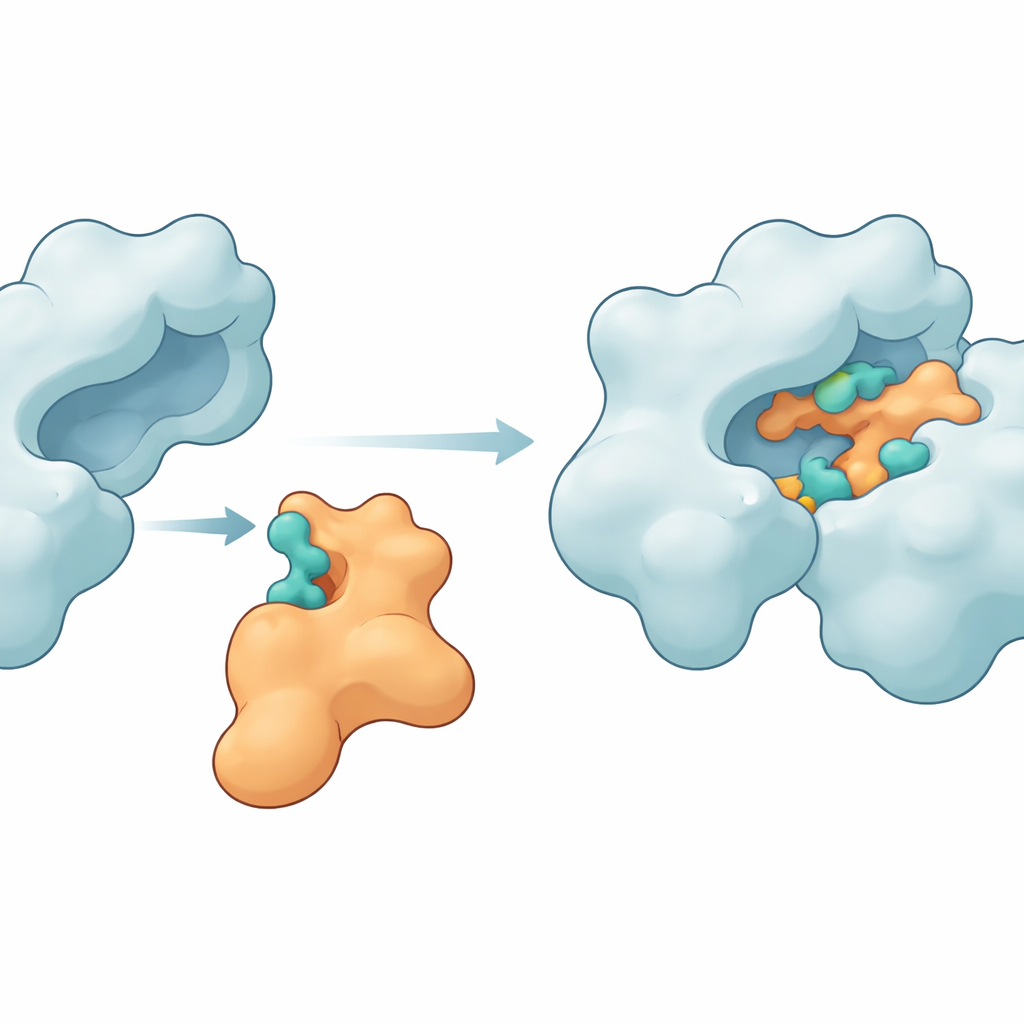
Proteinleri Bir Arada Tutankilit Temas Noktaları
Simülasyonlar, Im9’un gerçekten de DNA giraz ile sıkı ve kalıcı bir kompleks oluşturabileceğini ortaya koydu. Enzim üzerinde MET27, ASP47, LYS105, LEU198, ASN199, ARG191 ve GLU194 gibi birkaç amino asit, Im9’daki eşleşen bölgelerle tekrarlayan hidrojen bağları ve diğer çekici etkileşimler oluşturdu. Önde gelen bir modelde, iki ortak simülasyonun çoğunda altı ile on arasında hidrojen bağı sürdürdü; bu, güçlü ve iyi düzenlenmiş bir arayüzün göstergesiydi. Proteinlerin ne kadar kompakt kaldığı ve şekillerinin ne kadar dalgalandığı gibi diğer yapısal ölçümler, enzimin bütün kaldığını ve bağışıklık proteininin gyraz yüzeyine uyum sağlamak için yeterince esnediğini gösterdi. MM-GBSA yöntemiyle yapılan enerji hesaplamaları da bu temasların elektrostatik ve van der Waals katkılarının hakim olduğu, mütevazı fakat olumlu bir bağlanma serbest enerjisi oluşturduğunu destekledi.
Bilgisayar Modellerinden Geleceğin Antimikrobiyallerine
Genel olarak sonuçlar, Colicin E9 bağışıklık proteininin Pseudomonas DNA girazının aktif bölgesine kararlı şekilde bağlanabileceğini, uzun ömürlü bir kompleks oluşturabileceğini ve prensipte enzimin DNA işlemedeki normal rolünü engelleyebileceğini öne sürüyor. Bu bulgular tamamen bilgisayar modellerine dayandığı ve hala deneysel testlere ihtiyaç duyduğu halde, bir protein-temelli inhibitörün nerede ve nasıl tutunabileceğine dair ayrıntılı bir plan sunuyorlar. Uzman olmayanlar için ana mesaj, doğanın kendi bakteriyel silahlarının ve kalkanlarının zor tedavi edilen enfeksiyonlara karşı yeni stratejilere ilham verebileceğidir. Bu mikroskobik tokalaşmayı atomik ayrıntıda anlayarak, bilim insanları insan hücrelerine zarar vermeden önemli bakteri enzimlerini kapatacak yeni antimikrobiyaller tasarlamaya bir adım daha yaklaşmış oluyor.
Atıf: Alfaraj, R., Alkathiri, F. & Chikhale, R. Investigating Escherichia coli Colicin E9 immunity protein interactions with DNA gyrase of Pseudomonas aeruginosa: advanced computational approach for developing novel antimicrobial strategies. Sci Rep 16, 10786 (2026). https://doi.org/10.1038/s41598-026-44427-2
Anahtar kelimeler: antibiyotik direnci, DNA girazı, protein–protein etkileşimleri, hesaplamalı ilaç tasarımı, Pseudomonas aeruginosa