Clear Sky Science · tr
Pyrococcus furiosus dolichylfosfat mannoz sentetazı için kristalografik veriler enzimin glikolipid ürününü ters çevirebileceğini öne sürüyor
Sıcak seven mikroplar hücre örtülerini nasıl koruyor
Kaynama sıcaklıklarına dayanabilen birçok mikroorganizma, hücre yüzeyinde bulunan koruyucu bir şeker örtüsüne borçludur. Bu örtüyü inşa etmek, hücre zarının bir tarafında üretilip diğer tarafa taşınması gereken özel yağ–şeker moleküllerini gerektirir. Bu çalışma, sıcak seven bir mikroorganizmadan bir böyle molekül üreten enzimi ayrıntılı olarak inceliyor ve dikkat çekici biçimde aynı proteinin ürününü zar boyunca çevirmeye de yardımcı olabileceğini—yani aynı anda iki işi yapabileceğini—öneriyor.
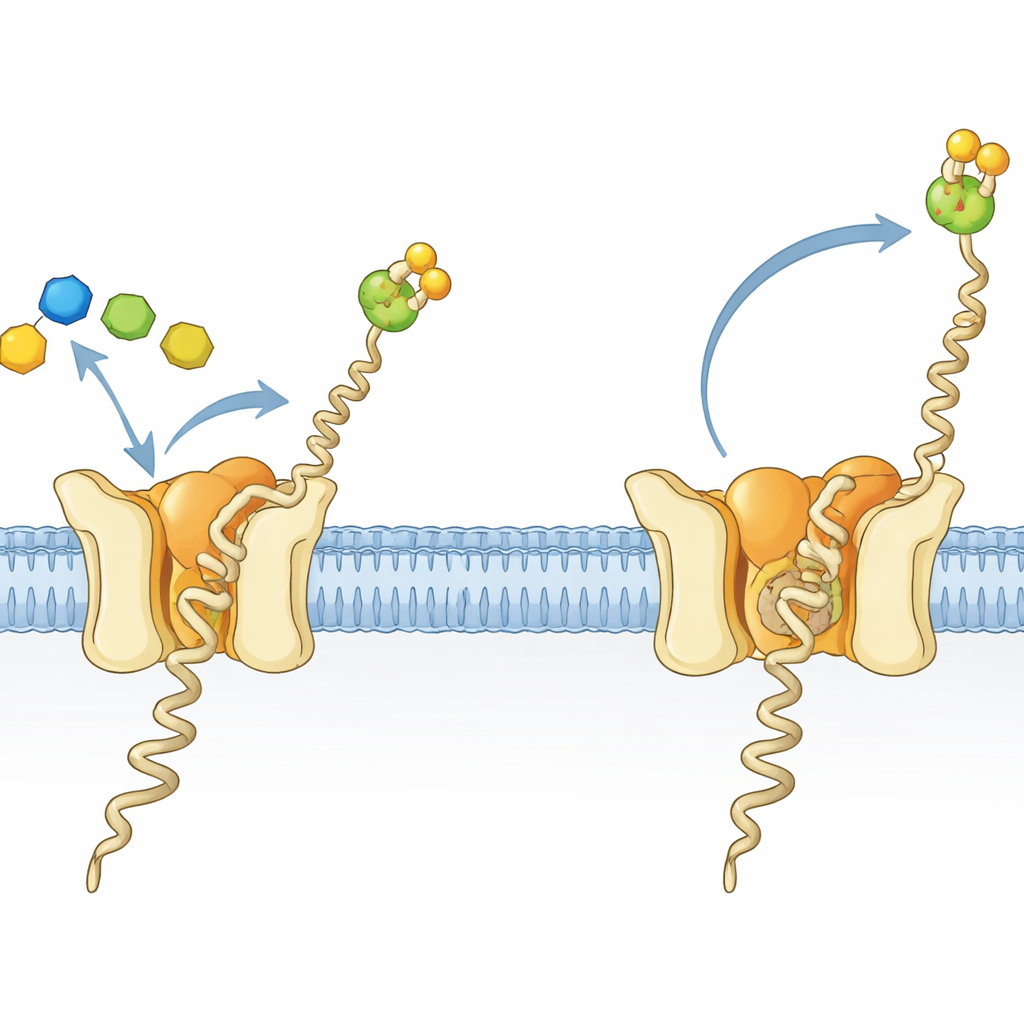
Hayati bir şeker–yağ molekülü için küçük bir fabrika
Tüm yaşam alanlarındaki hücreler birçok proteini şeker zincirleriyle süsler; bu süreç doğru katlanma, kararlılık ve hücreler arası iletişim için elzemdir. Arkealar ve ökaryotlarda bu süslemelerin ana yapı taşlarından biri dolichylfosfat mannoz (Dol-P-Man) adı verilen bir şeker–yağ molekülüdür. Bu molekül, zar içinde tutunan uzun yağlı bir kuyruğa ve sulu ortamın dışına bakan bir şeker–fosfat başına sahiptir. Dol-P-Man, çözünebilir bir vericiden membrana bağlı bir lipide mannoz şekerini aktaran dolichylfosfat mannoz sentetazı (DPMS) enzimi tarafından üretilir. Hipertermofilik arkeon Pyrococcus furiosus’ta DPMS tek zincirli bir protein olup, tip-III DPMS olarak adlandırılır; çözünür katalitik bölgeye bağlı, rolü belirsiz olan dört sarmallı bir membran geçişli bölüme sahiptir.
Enzimi iş başındayken yakalamak
Araştırmacılar P. furiosus DPMS'i substratlarıyla birlikte kristalize edip reaksiyonu X-ışını kristalografisiyle izlediler. Yeni yapıları ve önceki üç yapı, şeker aktarımının gerçekleştiği anın çevresine ait bir dizi fotoğraf yakalıyor. Bir durumda, verici molekül (GDP-mannoz) ve Dol-P benzeri bir alıcı, mannozun reaksiyona giren karbonunu Dol-P üzerindeki fosfat grubunun tam karşısına yerleştiren hassas bir geometride bağlanmış durumda—ideal bir “aktarmadan önce” düzenlenişi. Enzimdeki döngüler ön ve arka kapılar gibi davranır: vericiyi ve metal iyonunu yerinde tutmak için kapanır, sonra Dol-P’nin girişi ve şeker aktarıldıktan sonra harcanmış GDP’nin çıkışı için yolu açacak şekilde yeniden düzenlenir. Bu ayrıntılar, enzimin zar yüzeyindeki etkili ve doğru şeker aktarımını nasıl sağladığını netleştirir.
Zarın içinde ters çevrilmiş bir ürün
Daha şaşırtıcı olarak aynı kristallerde görülen ikinci, farklı bir durum vardı. Burada bitmiş Dol-P-Man molekülü aktif bölgede değil, proteinin membran geçişli bölümünün daha derininde, “ters” bir yönelimle sıkışmış haldeydi. Şeker–fosfat başı iki çift heliks (TMD1 ve TMD2) arasındaki polar bir cepte otururken, yağlı kuyruğu helikslerin oluşturduğu bir olu boyunca uzanıyordu. Belirgin bir aminoasit olan fenilalanin, bu cebe erişimi engelleyebilen ya da açabilen bir kapı görevi görüyor gibi görünüyordu. Elektron yoğunluğunun kalitesi ve protein paketlenme biçimi, bu ters çevrilmiş Dol-P-Man’in kristal temaslarına bağlı bir artefakt değil, enzimin benimseyebileceği gerçek ve iyi dolu bir durum olduğunu düşündürüyor.
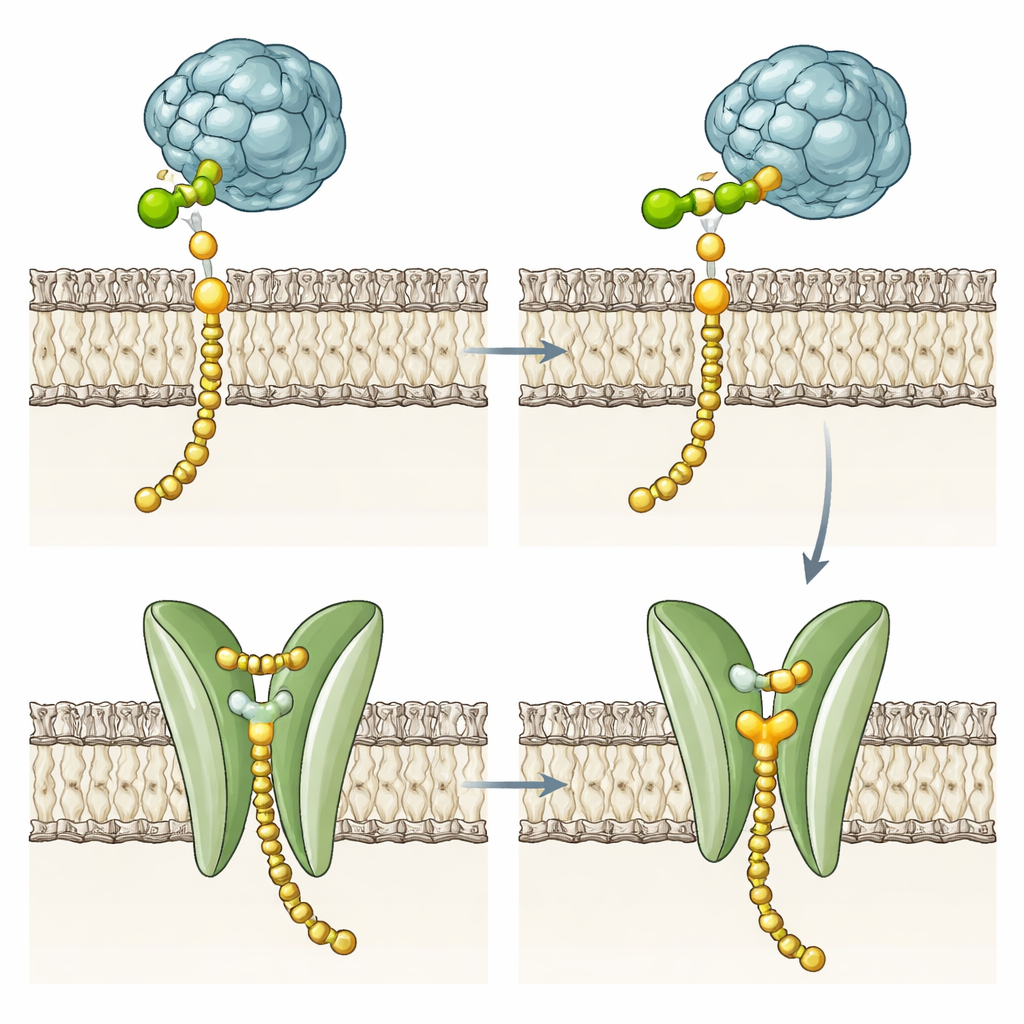
Mutant enzimler ikinci bir işe işaret ediyor
Membran geçişli bölgenin şeker aktarım kimyası için gerekli olup olmadığını test etmek üzere ekip bir dizi varyant tasarladı. Helikslerin çoğunu ya da tamamını sildiler, onları maya DPMS’inden alınan farklı bir membran segmentiyle değiştirdiler veya cepteki kritik kalıntıları ve fenilalanin kapıyı değiştirdiler. Dikkat çekici biçimde, bu mutantlar hâlâ sağlam enzimle benzer hızlarda Dol-P-Man ürettiler; bazıları zar içinde biraz daha az kararlıydı. Bu, temel kimyanın çözünür katalitik bölgede yer aldığını ve dört sarmallı demetin mannozu Dol-P’ye bağlamak için gerekli olmadığını gösteriyor. Bunun yerine korunmuş polar cep, olu ve kapılayıcı kalıntı, özellikle sert membranlarının kendiliğinden lipid çevirimini enerji açısından maliyetli kıldığı hipertermofilik arkealarda bitmiş ürünü işleme konusunda özel bir rol olduğunu düşündürüyor.
İki amaçlı bir enzim neden önemli
Yapısal ve mutasyonel kanıtları birleştirerek yazarlar tip-III DPMS’in “ayrık görevli” (moonlighting) bir protein olduğunu öne sürüyorlar. Önce arkeal plazma zarının iç yüzünde Dol-P-Man’i sentezler; ardından transmembran bölgesi şeker–yağ molekülünü çevirerek baş grubunun hücre dışına çıkmasına yardımcı olabilir; böylece hücrenin şeker örtüsünü inşa eden diğer enzimlerin tüketimine hazır hale gelir. Evrim, büyük olasılıkla bu kamçılı tasarımı aşırı ısı seven arkealarda desteklemiş; sentez yerini özel bir çevirme oluğuna yakın tutmak israfı ve ısıl hasarı en aza indirebilir. Bu çalışma doğrudan çevirme aktivitesini henüz kanıtlamasa da, bir enzimin zorlu bir zar bariyeri üzerinden hayati bir lipid ara ürününü hem yaratıp hem de yeniden konumlandırabileceğine dair somut bir yapısal model sunuyor.
Atıf: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
Anahtar kelimeler: dolichylfosfat mannoz, lipid flippaz, arkealar, protein glikozilasyonu, zar enzimleri