Clear Sky Science · tr
Reçete dozu sınıflandırması, lokal olarak ileri evre NSCLC’de derin öğrenme tabanlı VMAT doz tahminini iyileştirir
Neden Daha Akıllı Radyasyon Planları Önemli
İleri evre akciğer kanserini radyasyonla tedavi ederken doktorlar ince bir dengede yürür: tümörü kontrol etmek için yeterli enerji vermek aynı zamanda yakınlardaki hassas organları güvende tutmak. Bu planları tasarlamak yavaş, karmaşık ve planerinin becerisine büyük ölçüde bağlıdır. Bu çalışma, yapay zekanın göğüs bölgesindeki radyasyon yayılımını nasıl tahmin edebileceğini araştırıyor ve özellikle AI’ye özenle gruplanmış doz seviyeleriyle öğretilmesinin tahminlerini daha doğru ve klinik olarak daha kullanışlı hale getirdiğini gösteriyor.
Akciğer Kanseri Nasıl Odaklanmış Işınlarla Tedavi Edilir
Lokal olarak ileri evre küçük hücre dışı olmayan akciğer kanseri olan çoğu kişi tümörü ameliyatla aldırmaya uygun değildir. Bunun yerine genellikle kemoterapiyle birlikte, göğüs çevresinde yayılan ve arklar halinde hareket eden yüksek oranda şekillendirilmiş radyasyon ışınları (VMAT olarak bilinen teknik) uygulanır. Amaç, tümörü yüksek ve homojen bir dozla kaplamak, aynı zamanda akciğerler, kalp, yemek borusu ve omuriliğin maruziyetini sınırlamaktır. Bu dengeye ulaşmak genellikle birden çok deneme‑yanılma ayarı gerektirir; bu işlemler zaman alır ve tedavi kararlarını geciktirebilir. Doktorlar belirli bir hasta için hangi doz deseninin gerçekçi olarak elde edilebileceğini hızlıca tahmin edebilseydi, en iyi tedavi stratejisini daha erken seçebilirlerdi.
Algoritmaya Doz Desenlerini Öğretmek
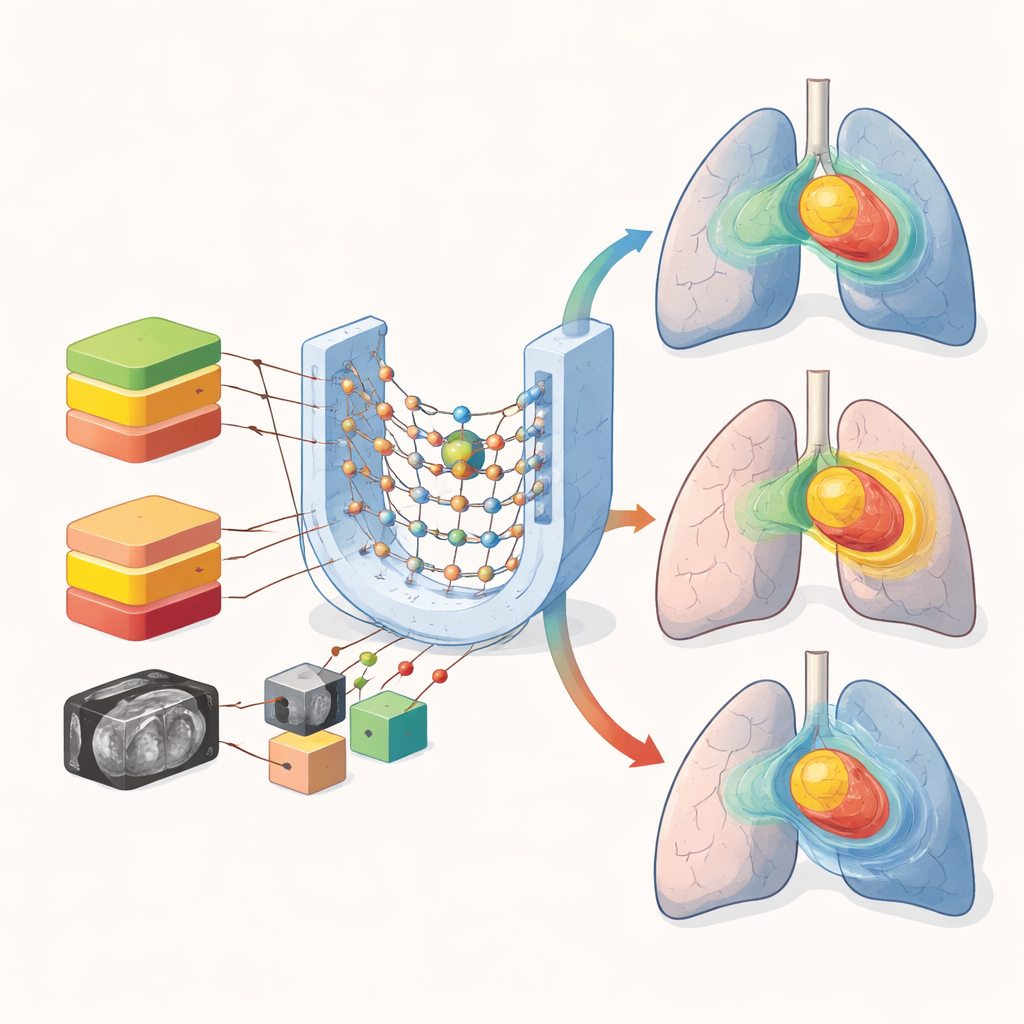
Araştırmacılar, görüntülerden doğrudan desenleri öğrenen bir yapay zeka biçimi olan derin öğrenmeye yöneldi. VMAT ile tedavi edilmiş 72 akciğer kanseri hastasının BT taramalarını ve tamamlanmış tedavi planlarını topladılar. Her hasta için aynı ışın düzeninin üç farklı toplam dozu nasıl vereceğini yeniden hesapladılar: radyasyonda standart birimler olan 50, 54 ve 60 gray (Gy). Her vaka, tümörü, ana organları ve altta yatan BT görüntüsünü işaretleyen üç boyutlu bir ızgaraya dönüştürüldü. Bu dokuz kanallı bilgi, anatomiye göre dozun vücutta nasıl aktığını öğrenebilen yaygın bir sinir ağı tasarımı olan 3B U‑Net’e beslendi.
Reçete Dozuna Göre Gruplamanın Neden Önemli Olduğu
Ana soru, hastalara farklı toplam dozlar reçete edilmesi gerçeğiyle nasıl başa çıkılacağıydı. Ekip, aksi halde özdeş dört AI modeli oluşturdu. Üçü yalnızca bir doz düzeyi (50, 54 veya 60 Gy) içeren planlarla eğitilen “tek reçete” modelleriydi. Dördüncü modelse 50 ve 60 Gy vakalarını karıştırdı ve ağa hangi reçeteyi gördüğünü söylemedi. Yeni hastalar üzerinde test edildiğinde, reçeteye özgü modeller tümörde gerçek dozu daha iyi eşleştirdi; hem kapsama hem de yüksek doz noktalarını klinik planlara yakın tutarak tipik olarak birkaç Gy içinde kaldılar. Buna karşılık, karışık model tümörün en yüksek doz bölgelerinde ve dozun katı güvenlik sınırlarının altında tutulması gereken omuriliğin çevresinde belirgin şekilde daha büyük hatalar yaptı.
Hayati Organları Korurken Planlamayı Hızlandırmak
İlginç bir şekilde, akciğerler, kalp ve yemek borusu gibi birçok organ için karışık ve sınıflandırılmış modeller benzer performans sergiledi. Bu daha büyük yapıların ortalama doz hataları tüm yaklaşımlarda ılımlı kaldı. Reçetelerin karıştırılmasının başlıca zayıflığı, dik doz düşüşünün elzem olduğu omurilik gibi küçük, hassas yapılarda ortaya çıktı. Tahmin edilen doz haritalarının görsel kontrolleri, tümördeki yüksek doz bölgesinin genel şeklini tüm modellerin yakaladığını gösterdi; ancak reçetelerin karıştırılması keskin gradyanlarda ve akciğerlerin düşük doz alanlarında daha fazla bulanıklığa yol açtı. Sayısal olarak ince olan bu farklar, doktorlar daha yüksek bir reçetenin güvenli olup olmadığına karar verirken önemli olabilir.
Bu Hastalar ve Klinikler İçin Ne Anlama Geliyor
Hastalar için bu çalışma, klinik sistemlerin zaten yaptığı dikkatli doz hesaplarını değiştirmez; ancak zaman ve çabanın gerçekten uygulanabilir ve güvenli olan planlara odaklanmasını sağlamaya yardımcı olabilir. Eğitim verilerini reçete dozuna göre gruplamanın—özellikle tümör kapsaması ve omurilik koruması açısından—AI tahminlerini belirgin şekilde keskinleştirdiğini göstererek çalışma, bilgisayar destekli yardımı daha güvenilir kılabilecek pratik bir tasarım seçimini vurguluyor. Daha büyük ve daha çeşitli hasta gruplarında ileri testlerle bu tür modeller, doktorlara muhtemel radyasyon ödünleşmelerinin hızlı, anatomiye dayalı bir önizlemesini sunan günlük araçlar haline gelebilir; böylece daha iyi ve daha tutarlı tedavi planlamasını destekleyebilirler.
Atıf: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
Anahtar kelimeler: akciğer kanseri radyoterapisi, derin öğrenme doz tahmini, VMAT planlaması, tedavi planı optimizasyonu, risk altındaki organlar