Clear Sky Science · tr
Glioblastomada pıhtılaşma ve bağışıklık düzenlenmesinde ekstraselüler veziküllerin ikili rolünü keşfetmek
Beyin kanserinde kan pıhtılarının önemi
En agresif beyin kanseri biçimi olan glioblastoma teşhisi konan kişiler sıklıkla beklenmedik bir tehlikeyle karşılaşır: bacaklarda veya beyinde ortaya çıkan tehlikeli kan pıhtıları. Bu pıhtılar sağkalımı kısaltabilir ve zaten zorlu olan tedavileri daha da karmaşık hale getirebilir. Bu çalışma basit ama kritik bir soruyu soruyor: glioblastoma hücrelerini çevreleyen kanı pıhtılaşmaya neden bu kadar yatkın kılan nedir ve tümör hücrelerinin kana bıraktığı küçük parçacıklar vücudun bağışıklık savunmasını nasıl yeniden şekillendirir?
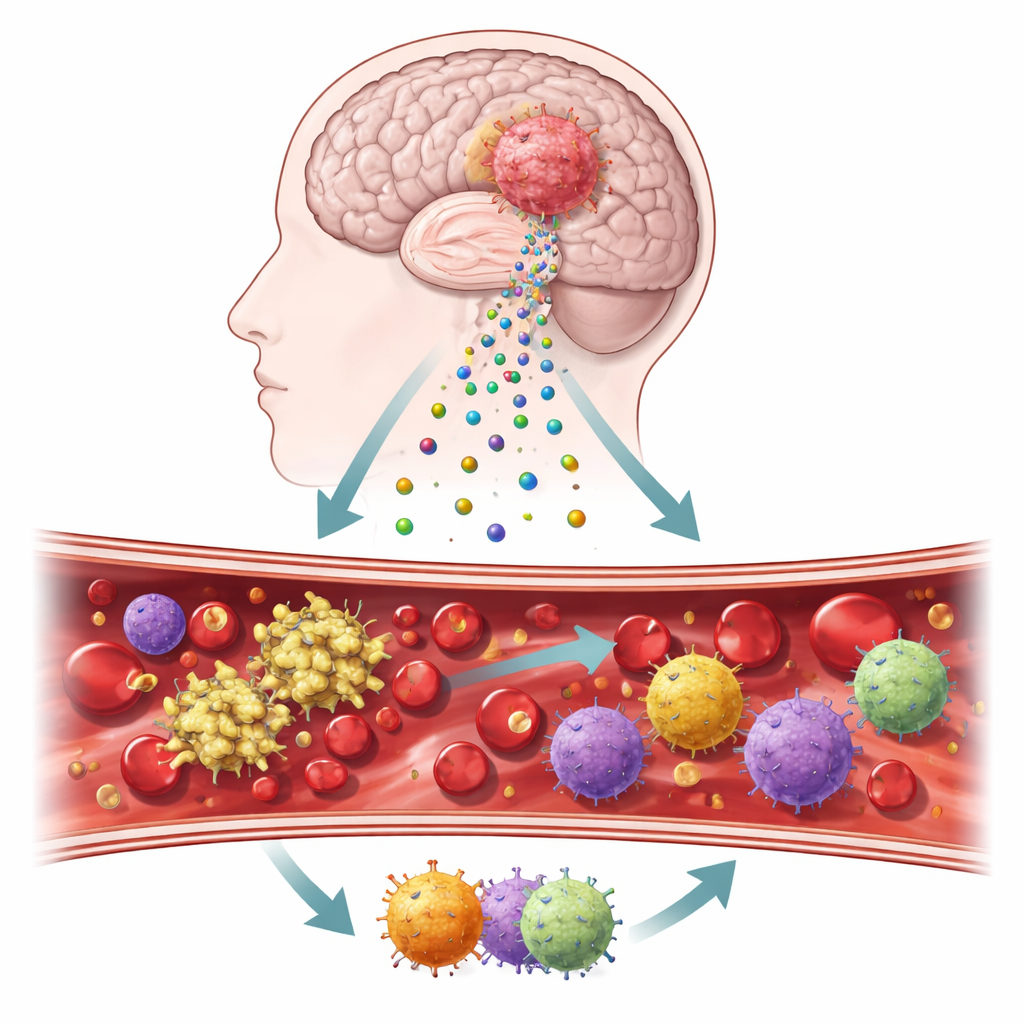
Beyin tümöründen ayrılan küçük haberci parçacıklar
Araştırmacılar, tümör hücrelerinden kopup kan ve beyin dokusu içinde dolaşan ekstraselüler vezikül adı verilen mikroskobik kabarcıklara odaklandılar. Bu veziküller yüzeylerinde pıhtı oluşumunu tetiklediği ve inflamasyonu etkilediği bilinen iki ana protein taşır: doku faktörü ve podoplanin. Araştırma ekibi, gerçek hastalardan alınan tümör örnekleri, ameliyat sırasında toplanan kan ve hastaların tümörlerinden elde edilen hücre kültürlerini kullanarak bu moleküllerin gerçek hastalarda ve kontrollü laboratuvar testlerindeki davranışını takip eden adım adım bir iş akışı oluşturdu. Ayrıca tümör dokusunu normal beyin dokusuyla karşılaştırarak pıhtı ile ilişkili bu sinyallerin ne kadar güçlü biçimde açıldığını incelediler.
Sessiz bir kan dolaşımı ama hazırlıklı bir tümör bölgesi
Standart hastane testleri, ameliyat öncesinde birçok hastanın kanının şaşırtıcı derecede normal göründüğünü gösterdi: yaygın pıhtılaşma zamanları ve pıhtı sertliği değerleri büyük ölçüde referans aralıkları içindeydi. Ancak araştırmacılar tümörleri incelediklerinde farklı bir tablo ortaya çıktı. Glioblastoma dokusu, doku faktörü ve podoplanin düzeylerinin tutarlı biçimde yüksek olduğunu ve doğal bir fren olan doku faktörü yol akışkanı inhibitörünün çok düşük olduğunu gösterdi. Hastadan türetilen tümör hücre hatları da bu deseni kültürde büyük ölçüde koruyarak “pıhtıya yatkın” imzanın kanser hücrelerinin içsel bir özelliği olduğunu doğruladı. Bu hücreler veya salgıladıkları veziküller laboratuvarda plazma ile karıştırıldığında, özellikle doku faktörüne dayanan sözde ekstrinsik yol boyunca pıhtılar daha hızlı oluştu.
Farklı tümör hücreleri, farklı pıhtılaşma stratejileri
Tüm glioblastomalar aynı davranmadı. Bazı hasta kökenli hücre hatlarında çok yüksek doku faktörü vardı, bazılarında daha fazla podoplanin saptandı, bazılarında ise her iki proteinden az bulunuyordu. Doku faktörüne zengin hücreler pıhtılaşma süresini kısaltmada en güçlüydü; podoplanin açısından zengin hücreler ise trombositler üzerindeki etkileriyle orta düzeyde katkı sağladı. Bu hücre hatlarından biri yalnızca doku faktörü, yalnızca podoplanin, her ikisi veya hiçbiri ifadeli alt gruplara ayrıldığında, hücreler uzun süre bu ayrımı korumadı. Üç hafta içinde karışık profillere geri kaydılar ve bu yüksek düzeyde plastisiteyi ortaya koydu. Bu dinamik yeniden şekillenme, hücre içindeki oksidatif stres değişimleriyle birlikteydi; bu da tümördeki kimyasal stresin hücreleri daha pro‑pıhtılaşma eğilimli hâle itebileceğine işaret ediyor.
Veziküller beynin ve kanın bağışıklığını şekillendiriyor
Araştırma ekibi daha sonra tümör kaynaklı veziküllerin beynin kendi bağışıklık hücreleri olan mikroglia ile dolaşımdaki akyuvarlar ve nötrofiller üzerindeki etkilerine odaklandı. Güçlü şekilde pro‑pıhtılaşma yapan tümör hatlarından gelen veziküller mikroglia tarafından kolayca alındı ve mikroglianın göçünü yavaşlatırken onları daha inflamatuar, “M1‑benzeri” bir duruma ve hücresel yaşlanma belirtilerine doğru yönlendirdi. Kandaki bağışıklık hücrelerinde doku faktörü zengini veziküller lökositleri aktive etti, reaktif oksijen türlerinin üretimini artırdı ve nötrofillerden yapışkan ağ benzeri yapılar olan ekstrasellüler tuzakların salınımını teşvik etti. Podoplanin taşıyan veziküller bu patlayıcı bağışıklık reaksiyonlarını tetiklemede daha az güçlüydü ancak bağışıklık hücrelerinde bölünmeyi durduran ve davranışı değiştiren bir senesens programını güçlü biçimde teşvik etti. Her iki ana proteinden yoksun olan veziküller bile belirli düzeylerde senesens provokasyonu yapabiliyordu; bu da başka yüklerin de rol oynadığını düşündürüyor.
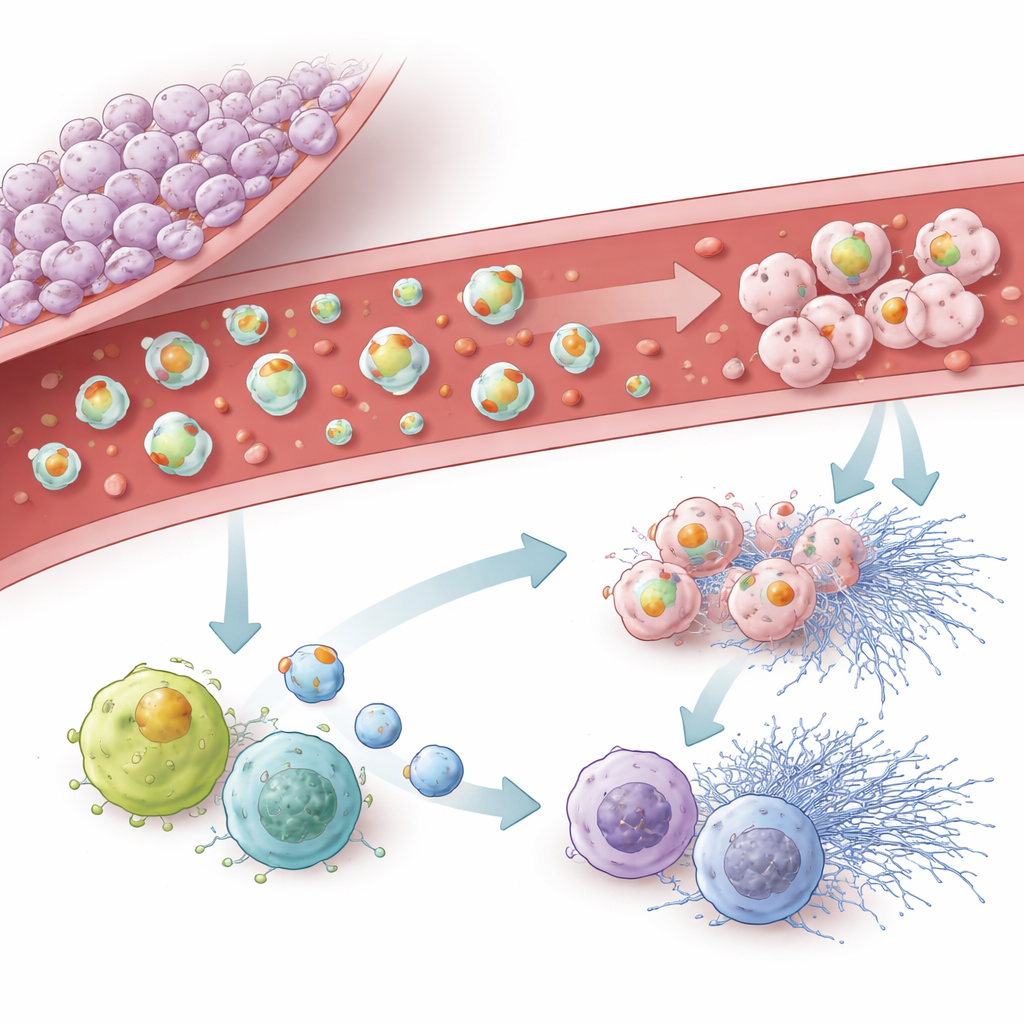
Bu bulguların hastalar ve gelecekteki bakım için anlamı
Bir araya getirildiğinde, bulgular glioblastomanın her yerde kanı kalınlaştırmadığını gösteriyor. Bunun yerine tümör ve saldığı veziküller, pıhtılaşma ve inflamasyonun birbirini beslediği lokalize, son derece karmaşık bir bölge yaratıyor. Doku faktörü pıhtı oluşumunun ve inflamatuar aktivasyonun başlıca motoru olarak öne çıkarken, podoplanin trombositler, bağışıklık yaşlanması ve mikroglial davranış üzerinde kendi etkisini ekliyor. Bu veziküller dolaştıkları ve tümörün durumunu yansıttıkları için, özellikle pıhtı riski yüksek hastaları tanımlamak üzere gelecekte kan bazlı belirteçler olarak kullanılabilirler. Ayrıca kanı geniş çapta inceltmeden tümörün pro‑pıhtı mekanizmasını hedef alan daha kişiselleştirilmiş koruma stratejilerine işaret edebilirler.
Atıf: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
Anahtar kelimeler: glioblastoma, kan pıhtıları, ekstraselüler veziküller, tümör mikroçevresi, bağışıklık yanıtı