Clear Sky Science · tr
Malign ilerlemeyi görselleştirmek: in situ CD109 tabanlı mekansal immünofloresan testi tümör mikroçevresinde papillerden anaplastik tiroid karsinomuna dönüşümü sınırlandırıyor
Bu tiroid kanseri çalışması neden önemli
Anaplastik tiroid karsinomu, genellikle tedavi edilebilir bir tiroid tümörünü hızla ölümcül bir hastalığa dönüştürebilen en öldürücü insan kanserlerinden biridir. Yine de doktorlar yaygın ve yavaş büyüyen bir papiller tiroid kanserinin nasıl aniden bu agresif forma dönüşebildiğini tam olarak anlamış değiller. Bu çalışma, yeni bir görüntüleme tekniği kullanarak kanser hücrelerinin ve çevrelerindeki doku komşuluğunun adım adım nasıl değiştiğini doğrudan hastanın tümörü içinde izliyor. Çalışma, tümörün yerel çevresinin hücreleri daha ölümcül bir duruma itmesinde nasıl bir rol oynayabileceğine dair daha ayrıntılı bir tablo sunuyor ve bu dönüşümü yavaşlatma veya önleme yollarına işaret ediyor.
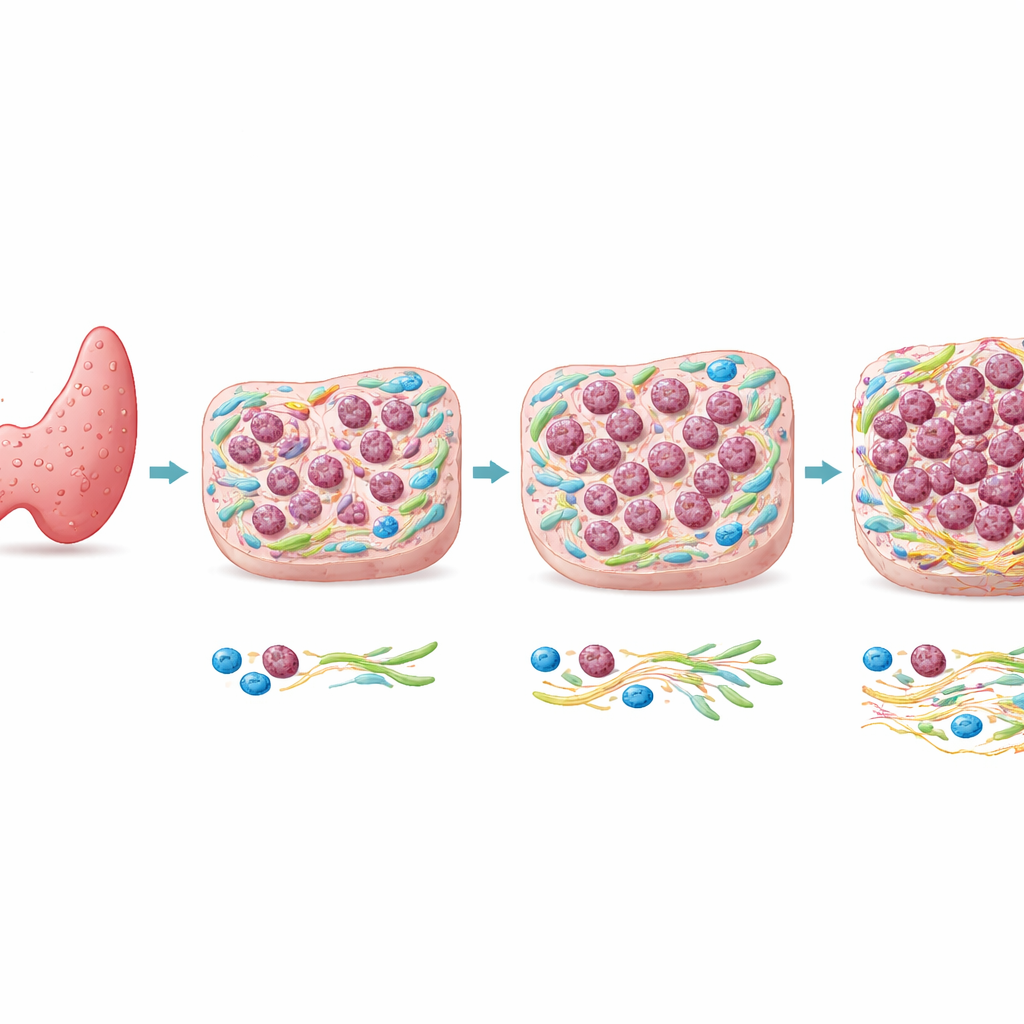
Yaygın bir tümörden nadir bir katile
Çoğu tiroid kanseri papiller tiroid karsinomu (PTC) olup, genellikle yavaş büyür ve iyi prognoza sahiptir. Buna karşılık anaplastik tiroid karsinomu (ATC) nadirdir ancak sıklıkla aylar içinde öldürücüdür. Genetik çalışmalar, aynı hastadaki ATC ve bitişik PTC bölgelerinin sık sık bilinen kanser genlerindeki değişiklikler de dahil olmak üzere aynı DNA mutasyonlarının çoğunu paylaştığını göstermiştir. Bu benzerlik, yalnızca genlerin neden bazı tümör bölgelerinin anaplastik hâle geldiğini açıklamayabileceğini düşündürür. Bu nedenle yazarlar, tehlikeli bu değişimi tetikleyip tetiklemediğini görmek için hücrelerin çevresindeki doku manzarasında—tümör mikroçevresinde—neler olduğunu incelemeye odaklandılar.
Kanseri yerinde haritalamanın yeni bir yolu
Ekip, doku kesitleri boyunca yüzlerce küçük tanımlı karoda belirli proteinlerin parlaklığını ölçen çok renkli mikroskopi türü olan mekansal immünofloresans (SPI) testi geliştirdi. Bu yöntemi tiroid dokusunda malign davranışın bir belirteci olarak tanımladıkları yüzey proteini CD109 ve sıradan papiller tümör hücrelerinin bir özelliği olan CK8/18 üzerine merkezlediler. Yüzlerce küçük bölgedeki CD109 ile CK8/18 oranını hesaplayarak, belirgin PTC alanlarını belirgin ATC alanlarından ayıran ve kritik olarak her iki belirtecin örtüştüğü ara bölgeleri ortaya çıkaran renk kodlu haritalar ürettiler. Keskin bir sınır yerine, papillerden anaplastik kansere geçiş, kademeli ve yamalı bir süreklilik olarak göründü.
Değişim yolunda beş bölge
Bu sürekliliği daha iyi anlamak için araştırmacılar dokuyu saf PTC’den tam gelişmiş ATC’ye kadar beş bölgeye ayırdılar. Ardından hücre kimliği, büyüme, hareket ve destek dokusunu raporlayan birçok ek proteini incelediler. Bu bölgeler boyunca E-kaderin ve CK8/18 gibi klasik epitel özellikleri istikrarlı şekilde azaldı; öte yandan vimentin gibi hücre hareketliliği ve şekil değişikliğiyle ilişkili belirteçler arttı. Daha anaplastik bölgelerde hızlı hücre bölünmesini gösteren proteinler yükseldi. Aynı zamanda çevredeki destek hücreler—kanser ilişkili fibroblastlar—ve belirli makrofajlar başta olmak üzere bağışıklık hücreleri daha fazla sayıda ve daha aktif hale geldi ve ürettikleri proteinler arttı.
Tümör iskelesi düşmanca döndüğünde
Tümörün iskelesi ya da ekstraselüler matrikste çarpıcı bir değişim gözlendi. Anaplastik bölgelerde fibroblast benzeri hücreler daha fazla tip III ve VI kollajen ile TGFBI adlı bir matriks proteini biriktirdiler; bu lifler daha kalın, daha dolaşık ve düzgün, paralel çizgiler halinde değil birçok yönde yönlenmişti. Bu yeniden düzenlenmiş ağ muhtemelen dokuyu mekanik olarak daha sert hale getiriyor. Bu daha sert zonlarda, YAP adlı basınca duyarlı bir sinyal proteini hem kanser hem destek hücrelerinde daha aktifti. Aynı alanlar, DNA hasarı belirtilerinin ve iltihabı andıran bir hücre ölümü türünün daha fazla göstergesini, ayrıca tehlike sinyali olarak hareket edebilen ve çevreyi daha da iltihaplandırabilecek S100 proteinlerinin salınımını gösterdi. Yazarlar, sıkışma, hücre ölümü ve kronik iltihabın kombinasyonunun baskıya dayanabilen ve epitel–mezankimal benzeri bir geçişe uğrayabilen zaten mutasyona uğramış kanser hücrelerinin hayatta kalmasını ve yayılmasını desteklediğini öne sürüyorlar.
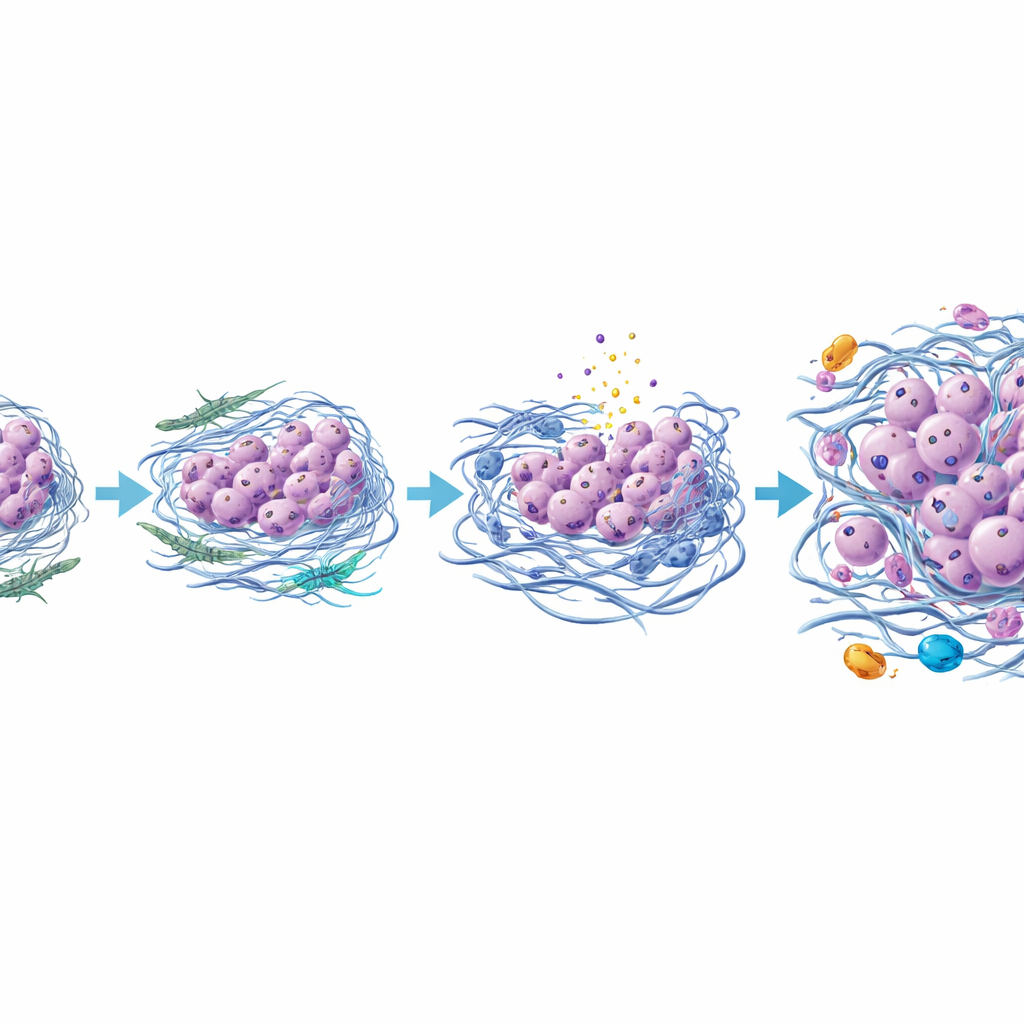
Bir tiroid tümörünün nasıl öldürücü hale geldiğine dair yeni bir resim
Bu bulguları bir araya getiren çalışma, anaplastik tiroid kanserinin yalnızca ek gen mutasyonlarından değil, tümörün etrafındaki komşuluğun yeniden şekillenmesinden de ortaya çıktığını öne sürüyor. Papiller tümör hücreleri ile yakınlarındaki destek hücreleri etkileşime girdikçe, bazı fibroblastlar çevre matriksi kalınlaştıran ve sertleştiren daha agresif bir tipe evriliyor, hassas hücreleri sıkıştırıp ölüme itiyor ve iltihaplı bağışıklık hücrelerini çağırıyor. Hayatta kalan, daha dirençli kanser hücreleri zamanla özgün tiroid özelliklerini kaybedip daha hareketli, invaziv bir kimlik benimsiyor ve sonunda anaplastik bir tümör oluşturuyor. Bu çalışma tek iyi incelenmiş bir olguya dayansa ve daha fazla hastada doğrulama gerektirse de, güçlü bir görüntüleme aracı ve tümörün destek hücrelerini, matriksini veya iltihap sinyallerini hedeflemenin tiroid kanserindeki en korkulan dönüşümlerden birini önlemeye veya geciktirmeye yardımcı olabileceği ayrıntılı bir model sunuyor.
Atıf: Cohen, T., Suzuki, K., Matsuda, K. et al. Visualizing malignant progression: in situ CD109-based spatial immunofluorescence assay delineates papillary to anaplastic thyroid carcinoma transformation within the tumor microenvironment. Sci Rep 16, 8682 (2026). https://doi.org/10.1038/s41598-026-41927-z
Anahtar kelimeler: anaplastik tiroid karsinomu, papiller tiroid karsinomu, tümör mikroçevresi, ekstraselüler matriks sertliği, mekansal immünofloresans