Clear Sky Science · tr
Potansiyel kanser uygulamaları için Mg katkılı CuFe2O4 nanoparçacıklarının sentezi ve karakterizasyonu
Neden küçük mıknatıslar kanser için önemli olabilir
Kemoterapi ve radyasyon gibi kanser tedavileri tümörlerin yanı sıra sağlıklı dokulara da zarar verebilir. Bilim insanları kanser hücrelerine normal hücrelerden daha güçlü şekilde saldıran daha akıllı tedaviler arıyor. Bu çalışma, demir, bakır ve magnezyumdan yapılan ultra-küçük manyetik parçacıkları araştırıyor; amaçları kanser hücrelerine yönelip içten onların kendi kendini yok etme programlarını tetiklemek. Bulgular, bu parçacıkların bileşimini ve boyutunu dikkatle ayarlamanın tümör hücrelerine karşı özellikle öldürücü olurken sağlıklı hücreleri koruyabileceğini gösteriyor.
Akıllı metal parçacıklar inşa etmek
Araştırmacılar bakır ve magnezyumu farklı oranlarda demir ve oksijenle birleştirerek içinde demir içeren “nanogerçek feritler” ailesi yaratıldı. Bu parçacıklar yalnızca yaklaşık 17–30 milyarıncı metrenin genişliğinde olup hücrelere sızacak kadar küçüktür. Ekip, parçacıkların doğru kristal yapıya sahip olduğunu, kimyasal olarak saf olduklarını ve kabaca küresel kümeler oluşturduklarını doğrulamak için çeşitli gelişmiş mikroskoplar ve X-ışını teknikleri kullandı. Eşit miktarda bakır ve magnezyum içeren karışık metal versiyonunun en küçük parçacıkları ürettiği, bunun yüzey alanını artırıp kimyasal reaktiviteyi yükseltebileceği görüldü.
Parçacıkları kanser hücrelerinde teste sokmak
Daha sonra ekip, her parçacık tipinin laboratuvarda yetiştirilen insan kanser hücrelerine olan toksisitesini test etti; bu hücreler arasında prostat (PC‑3), kolon (Caco‑2), meme (MCF‑7) ve karaciğer (HepG‑2) kanser hücreleri ile güvenlik kontrolü için normal bağırsak hücreleri yer aldı. Üç formülasyon da doz-bağımlı olarak kanser hücrelerine zarar verdi, ancak eşit derecede değil. Karışık bakır‑magnezyum parçacıkları genel olarak en güçlüydü; özellikle prostat ve kolon kanser hücrelerine karşı nispeten düşük dozlarda hücrelerin yarısını öldürdüler. Önemli olarak, normal hücreler daha yüksek dozları tolere etti; bu da gelecekteki herhangi bir tedavi için kritik olan bir seçicilik düzeyine işaret ediyor.
Kanser hücrelerini kontrollü kendi kendini yok etmeye zorlamak
Nanoparçacıkların nasıl öldürdüğünü anlamak için araştırmacılar hücrelerin hasarlı hücrelerin patlamaktansa düzgün bir şekilde kendilerini söküp attığı düzenli ölüm biçimi olan apoptoza baktı. Akış sitometrisi kullanarak, tedavi edilen prostat ve kolon kanseri hücrelerinin sağlıklı hâlden güçlü biçimde erken ve geç apoptoz evrelerine kaydığını gösterdiler. Yine, karışık bakır‑magnezyum parçacıkları en güçlü etkiyi gösterdi ve toplam apoptozu tedavi edilmeyen hücrelerin çok katına çıkardı. Ayrıca daha düzensiz bir hücre ölümü formu olan nekrozda da ılımlı bir artış görüldü; bu, birden fazla hasar yolunun devreye girebileceğine işaret ediyor.
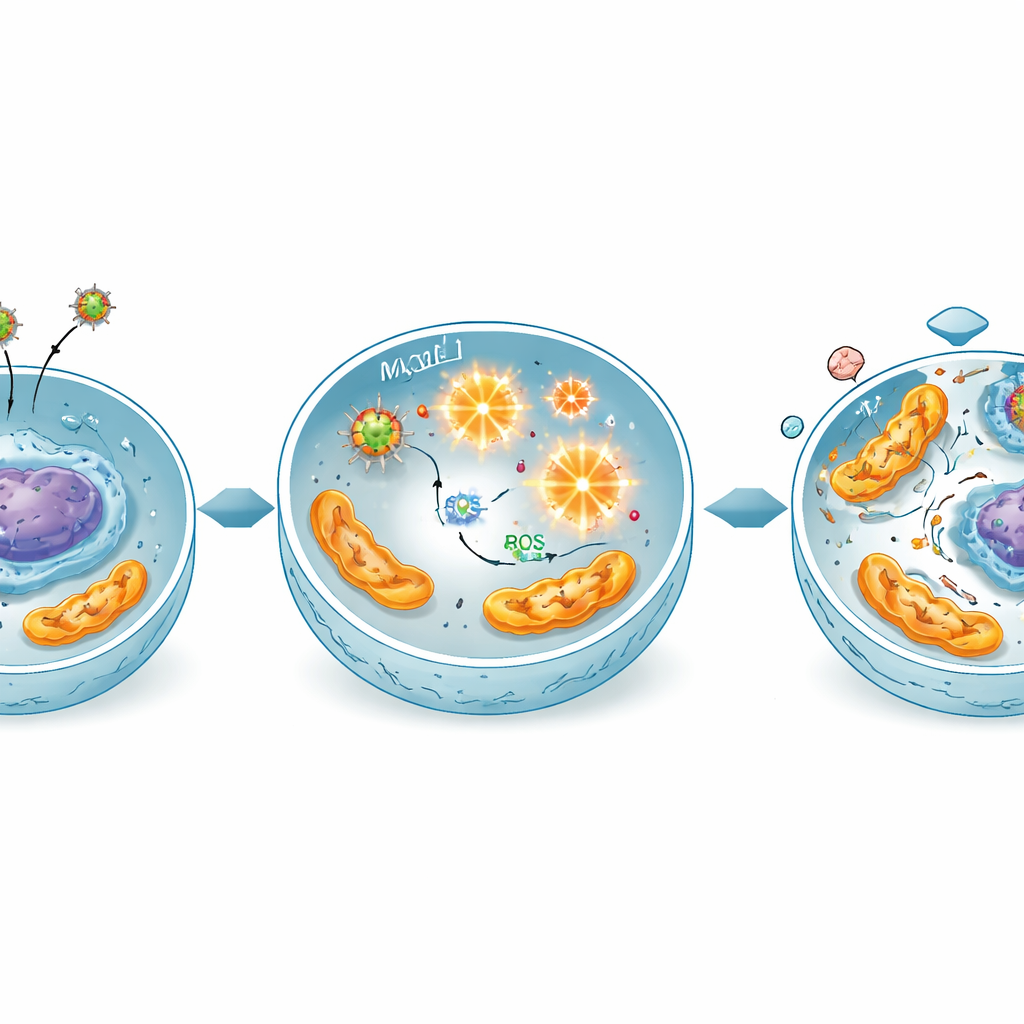
Kanser hücrelerini zararlı oksijen kimyasıyla aşırı yüklemek
Çalışma bu etkinin merkezinde kimyasal bir zincirleme reaksiyon olduğunu gösteriyor. Bu demir bazlı parçacıklar hücre içindeki doğal hidrojen peroksiti yüksek reaktif oksijen formlarına dönüştüren küçük katalizörler gibi davranabilir. Ölçümler, özellikle karışık bakır‑magnezyum parçacıklara maruz kalan tedavi edilmiş kanser hücrelerinin çok daha fazla bu reaktif oksijen türlerini ürettiğini gösterdi. Bu oksidatif saldırı hücre bileşenlerine, özellikle enerji üreten mitokondrilere ve DNA'ya zarar veriyor. Gen ifadeleri testleri, hücre intiharına bağlı ana “koruyucu” ve “idamcı” genlerin açıldığını, hayatta kalma ve hücre döngüsü genlerinin ise kapandığını doğruladı; bu da stres kaynaklı, mitokondri-bağımlı apoptoz manzarasını destekliyor.
Bu, gelecekteki kanser bakımına ne anlama gelebilir
Genel olarak çalışma, metal seçiminde ve nanoferitlerin boyutunu ve yapısını ayarlamakta dikkatli davranarak kanser hücrelerini güçlü biçimde kendi kendini yok etmeye iten, aynı zamanda normal hücrelere daha nazik davranan parçacıklar yaratmanın mümkün olduğunu gösteriyor. Eşit parça bakır‑magnezyum versiyonu en etkili olarak öne çıktı; muhtemelen küçük boyutu ve karışık metal kimyası hücreye girişini ve reaktif oksijen üretme yeteneğini artırıyor. Bu sonuçlar hâlâ hücre kültürleriyle sınırlı ve klinik kullanımdan çok uzak olsa da, tümörü vücudu yaygın şekilde toksik ilaçlarla doldurmak yerine kendi öldürme anahtarlarını tetiklemeye dayalı daha hassas, nanoteknoloji tabanlı kanser tedavilerine umut verici bir yol gösteriyor.
Atıf: Ali, M., Zein, N., Abdo, M.A. et al. Synthesis, characterization of Mg doped CuFe2O4 nanoparticles for potential anticancer applications. Sci Rep 16, 8276 (2026). https://doi.org/10.1038/s41598-026-41540-0
Anahtar kelimeler: nanoparçacıklar, kanser tedavisi, reaktif oksijen türleri, apoptoz, feritler