Clear Sky Science · tr
Simetrik bispesifik antikorların yapısal stabilitesi: bağlantı bölgelerine yakın potansiyel zayıflığı gösteren bir vaka çalışması
Yeni kanser ilaçlarındaki küçük bağlayıcıların önemi
Günümüzün en heyecan verici kanser ilaçlarının birçoğu, aynı anda iki farklı hedefi tutacak şekilde tasarlanmış antikorlardır; bunlar bağışık hücrelerin tümörlere yönelmesine yardımcı olur. Bu "bispesifik" antikorlar tek hedefli eski ilaçlardan daha güçlü olabilir, ancak aynı zamanda daha karmaşık moleküllerdir. Bu çalışma, deneysel bir ilacı yakından inceleyerek basit ama kritik bir soruyu soruyor: parçaları bir arada tutan küçük protein bağlayıcıları gerçek dünyadaki üretim ve depolama koşullarında sağlam kalıyor mu, yoksa zayıf halka mı oluyorlar?
İki elli bir antikor inşa etmek
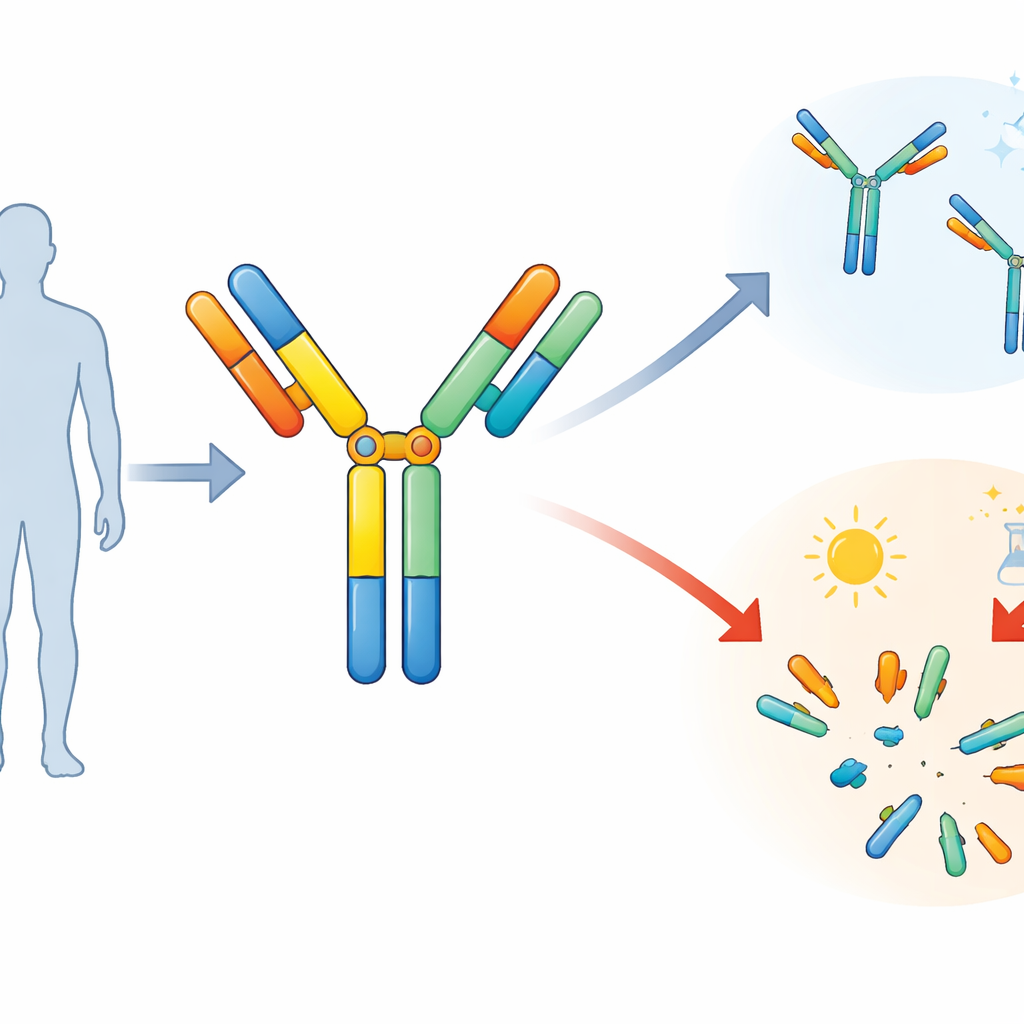
Araştırmacılar, HER2 adlı bir tümör belirteci ve CD3 adlı bir bağışık hücre reseptörüne bağlanacak şekilde tasarlanmış simetrik bir bispesifik antikora odaklandı. Burada simetrik, molekülün dengeli, ayna benzeri bir yapıda inşa edildiği ve olağan iki uç yerine dört tutma ucuna sahip olduğu anlamına geliyor. Bunu başarmak için ekip, tanıdık antikor parçalarını bağlayıcı olarak bilinen kısa, esnek protein uzantılarıyla dikti. Bu bağlayıcılar menteşe ya da mesafe koruyucu gibi davranarak bağlanma bölgelerinin doğru konumları almasına imkan verir, böylece ilaç aynı anda hem kanser hücresini hem de T hücresini yakalayabilir.
Sıcaklık ve zorlu koşullar altındaki zayıf noktalar
Tasarımın gerçekten ne kadar dayanıklı olduğunu test etmek için ekip antikoru kasıtlı olarak zorladı. Haftalarca ısıtıp, molekülün saflaştırma, formülasyon veya uzun süreli depolama sırasında karşılaşabileceği farklı asidite (pH) ve tuz seviyelerindeki sıvılara koydular. Molekülleri boyuta göre ayıran bir teknik kullanarak, sağlam antikor oranının yavaşça düştüğünü ve özellikle yüksek pH’da daha küçük parçaların miktarının arttığını gözlemlediler. Tuz tek başına ancak mütevazı bir etki yaptı, ancak yüksek pH ile yüksek tuz birleştiğinde parçalanma keskin şekilde arttı; bu, molekülün belirli bölgelerinin ayrıldığını gösteriyordu.
Kırılma noktalarına yakından bakmak
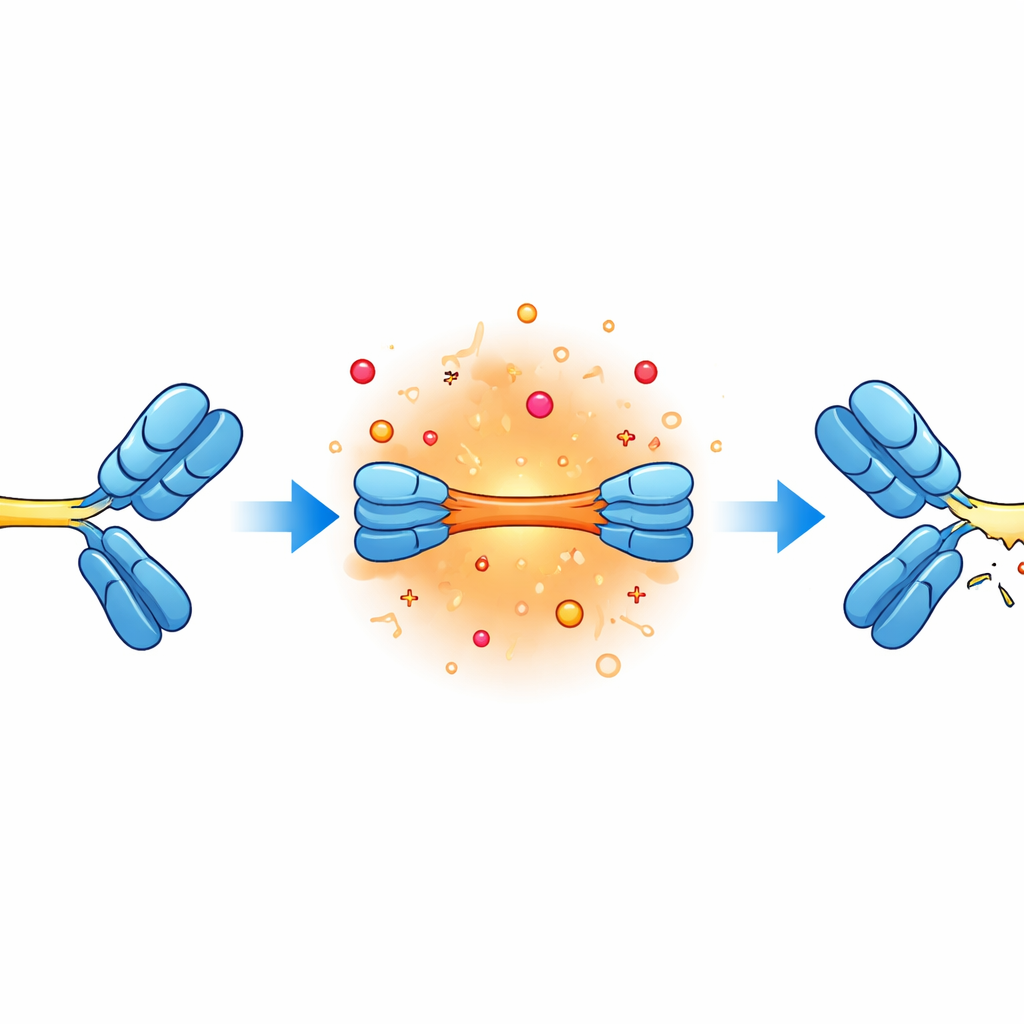
Bir sonraki adım, kırılmaların tam olarak nerede olduğunu belirlemekti. Araştırmacılar çeşitli parçaları topladı ve yüksek çözünürlüklü kütle spektrometrisiyle kütlelerini analiz etti; esasen parçaları moleküler bir yapboz gibi tartıp yeniden inşa ettiler. Bu, özellikle G4S ve G4 olarak adlandırılan iki belirli bağlayıcının kesilmeye yatkın olduğunu ortaya koydu. Bu esnek bağlayıcılar ana antikor kolları ile eklenmiş bağlanma segmentleri arasında yer alıyor. Alkalin, tuzlu ve sıcak koşullar altında bu bölgelerdeki peptit bağları aşama aşama kesiliyor ve bağlayıcı zincirleri boyunca öngörülebilir bir dizi fragment oluşuyordu.
Sadece bağlayıcılar değil: diğer bağlar da riskte
Analiz ayrıca diğer hassas noktalarda da hasar gösterdi. Bazı kırılmalar belirli asparagin yapı taşlarının yakınında oluştu; bu aminoasitlerin yüksek pH’da yavaş kimyasal değişimlere uğrayarak nihayetinde zincir kopmasına yol açabileceği biliniyor. Ayrıca ağırlık ve hafif zincirleri genellikle bir arada tutmaya yardımcı olan kükürt içeren sistein kalıntılarını içeren bağlar da bozuldu. Bu durum, kopmuş hafif zincir parçalarına ve farklı kimyasal olarak modifiye olmuş varyantlara yol açtı. Bu tür değişiklikler standart monoklonal antikor çalışmalarından tanıdık olsa da, bunların bağlayıcı bölgelere yakın ortaya çıkması, bispesifik tasarımın ek esnekliğinin komşu bağları ekstra strese maruz bırakabileceğini düşündürüyor.
Daha güvenli ve dayanıklı ilaçlar için tasarım dersleri
Uzman olmayanlar için temel çıkarım şu: antikorları ek bağlanma kolları ekleyerek daha çok yönlü yapmak sadece zekice genetik mühendisliğiyle ilgili değildir; aynı zamanda her şeyi bir arada tutan küçük bağlayıcı bölgelere dikkat edilmesini de gerektirir. Bu durumda, bispesifik antikorun işlevsel parçalarını birleştiren yaygın kullanılan esnek bağlayıcıların gerçekçi stres koşullarında yapısal zayıf noktalar olduğu ortaya çıktı. Çalışmanın sonucu bispesifik antikorların güvensiz olduğu değil, stabilitelerinin bu bağlayıcıların nasıl yapılandırıldığına ve yerleştirildiğine güçlü şekilde bağımlı olduğudur. Gelecek tasarımlar, yeni nesil antikor terapilerinin üretim, depolama veya tedavi sırasında parçalanmadan tam klinik vaatlerini yerine getirebilmesi için bağlayıcı uzunluğunu, dizisini ve yerel ortamı optimize etmeyi gerektirecektir.
Atıf: Ingavat, N., Kok, Y.J., Dzulkiflie, N. et al. Structural stability of symmetric bispecific antibodies: a case study showing potential compromise near linker regions. Sci Rep 16, 9715 (2026). https://doi.org/10.1038/s41598-026-40607-2
Anahtar kelimeler: bispesifik antikorlar, protein stabilitesi, bağlayıcı tasarımı, antikor mühendisliği, biyofarmasötik geliştirme