Clear Sky Science · tr
Bilgisayar destekli ilaç tasarımı teknikleri kullanılarak potansiyel bir glyoxalase‑I inhibitörü olarak hidroksitriazolün keşfi
Neden küçük bir hücre temizleyicisini durdurmak kansere karşı savaşabilir
Kanser hücreleri genellikle o kadar hızlı büyür ki kendi atıkları içinde boğulurlar. Hayatta kalma hilelerinden biri, şeker yakımının zararlı yan ürünlerini detoksifiye eden yerleşik bir temizlik ekibidir. Bu çalışma, bilgisayarların on binlerce molekülü taradığı ve en iyi adayları test etmek için deneylerin yapıldığı bir yaklaşımla bu ekibin kilit üyelerinden biri olan glyoxalase‑I enzimini nasıl kapatabileceğimizi araştırıyor. Amaç, bir gün doktorların tümör hücrelerini içeriden seçici biçimde zehirlemelerine yardımcı olabilecek yeni ilaç “başlangıç noktaları” keşfetmektir.
Hücrelerimizin içindeki gizli atık sistemi
Her hücre enerji üretmek için sürekli şekeri parçalar ve bu süreç, methylglyoxal adlı reaktif bir atık kimyasal üretir. Normal miktarlarda, vücudumuz methylglyoxal'ı glutatyon yardımına dayanan iki aşamalı bir yol olan glyoxalase sistemi aracılığıyla zararsız laktik aside dönüştürür. Glyoxalase‑I bu zincirin ilk ve en kritik adımıdır. Şekeri yoğun bir hızla yakan kanser hücreleri, methylglyoxal'ın toksik seviyelere ulaşmasını önlemek için glyoxalase‑I'e büyük ölçüde bağımlıdır. Bu enzim bloke edilirse methylglyoxal birikir ve zarar görmüş hücreleri programlı hücre ölümüne itebilir. Bu nedenle glyoxalase‑I, tümör metabolizmasının temel bir zaafına saldıran antikanser ilaçlar için çekici bir hedeftir.
Silikon ve istatistikle kimyasal uzayı aramak
Rastgele maddeleri laboratuvarda test etmek yerine araştırmacılar, bilgisayar destekli ilaç tasarımı kullanarak 50.000'den fazla küçük molekülden oluşan büyük bir ticari koleksiyonda arama yaptılar. Özel yazılımlar önce her molekülü temizleyip standartlaştırdı, sonra vücut benzeri pH'da 3B şekillerini ve davranışlarını tahmin etti. Hızlı bir sanal tarama adımı, her adayın glyoxalase‑I'in aktif bölgesine ne kadar iyi uyabileceğini puanladı. Ekip daha sonra boyut, çözünürlük ve diğer ilaç‑benzerlik özellikleri hakkında basit kurallar uygulayarak vücutta muhtemelen işe yaramayacak molekülleri elledi. Daha ayrıntılı bir yerleştirme programı, en umut verici moleküllerin özellikle glyoxalase‑I'in kimyasının merkezinde yer alan çinko metal atomuna nasıl ulaşıp onu nasıl kavrayabileceğini inceledi.
Enzimin metal çekirdeğini kavramanın yeni bir yolu
Glyoxalase‑I'i bloke etme yönündeki önceki çabalar, metallere iyi bağlanan ancak genellikle zayıf stabilite veya istenmeyen yan etkilere sahip olabilen karboksilik asitler ve hidroksamik asitler gibi iyi bilinen kimyasal gruplara odaklandı. Mevcut çalışma bunun yerine farklı bir “metal‑yakalama” birimi ortaya çıkardı: hidroksitriazol halkası. Satın alınmak ve laboratuvarda test edilmek üzere seçilen on altı en yüksek sıra molekül arasında, bu halkayı taşıyan SPB07393SC kodlu bileşen öne çıktı. Sanal yerleştirmede hidroksitriazol grubu çinko atomuna kadar uzanırken, iki aromatik halkası enzimin yakınındaki yağlı ceplere girdi. Onlarca nanosaniye süresince yapılan bilgisayar simülasyonları, molekülün sıkıca bağlı kaldığını; sabit mesafeler, sıkı bir protein şekli ve kalıcı bir hidrojen bağı ağı gösterdiğini öne sürdü.
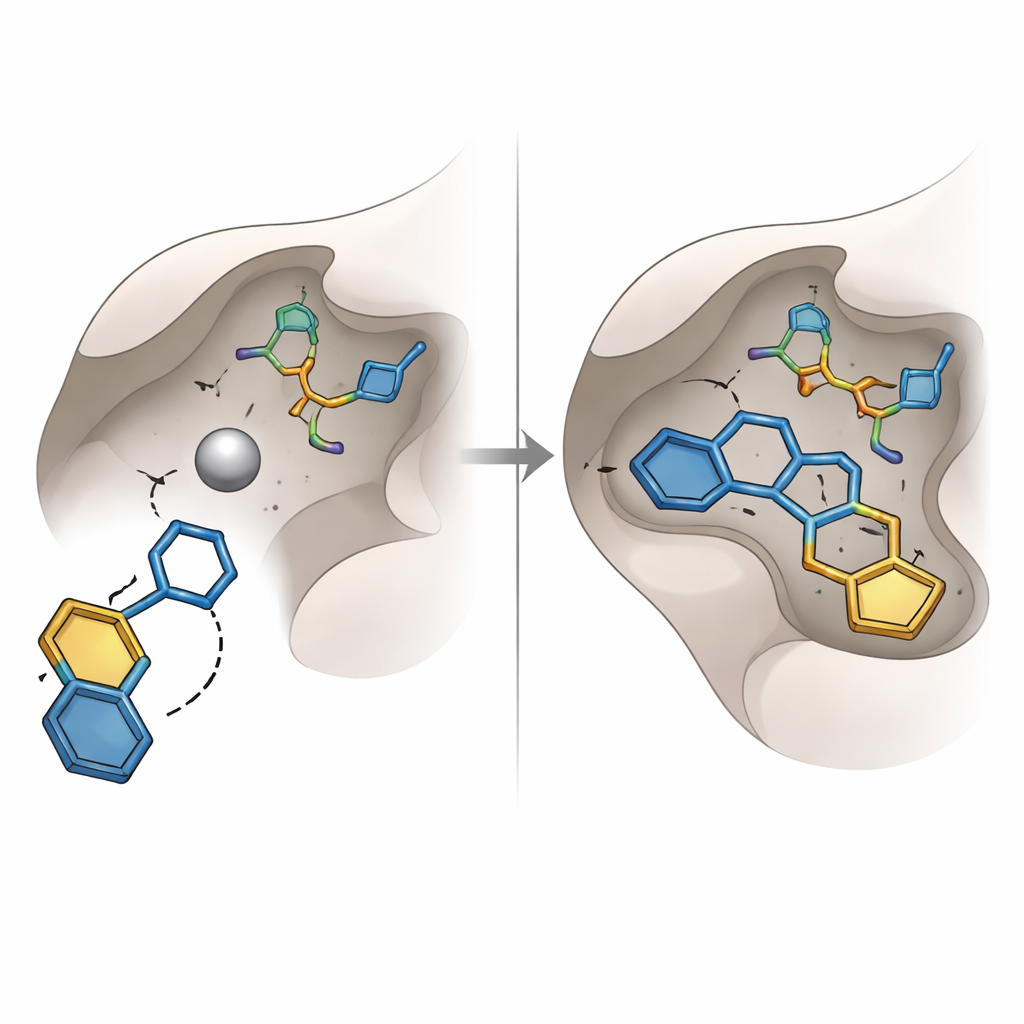
Tahminleri teste sokmak
Bilgisayar modellerinin gerçek dünyadaki etkilere dönüşüp dönüşmediğini görmek için ekip, seçilen moleküllerin saflaştırılmış insan glyoxalase‑I aktivitesini bir plaka temelli ölçümde ne kadar yavaşlattığını ölçtü. On altı adaydan on beşi, test edilen koşullar altında yalnızca zayıf veya önemsiz inhibisyon gösterdi; bu da yalnızca statik yerleştirme skorlarına güvenmenin tuzaklarını vurguluyor. Buna karşılık SPB07393SC enzimi güçlü şekilde inhibe etti; ortadan mikromolar potensiyle bu bileşiği bitmiş bir ilaçtan ziyade sağlam bir erken “hit” yaptı. Ek yazılım araçları, bu molekülün kabul edilebilir çözünürlüğe, iyi emilime, gerekirse beyne ulaşma yeteneğine ve belirli genetik veya karaciğerle ilişkili toksisiteler oluşturma olasılığının düşük olmasına işaret etti; ancak bu güvenlik tahminleri yine de deneysel doğrulama gerektirir.
Geleceğin kanser ilaçları için bunun anlamı
Bu çalışma hidroksitriazolü glyoxalase‑I'in çekirdeğindeki çinko atomuna ilaç adaylarını ankrajlamak için taze bir yol olarak tanıtarak ilaç tasarımcılarının kullanımına sunulan kimyasal seçenekleri genişletiyor. SPB07393SC kendisi yalnızca bir başlangıç noktası olsa da, enzim bloke etme gücü, tahmini ilaç‑benzeri davranışı ve hareket tabanlı simülasyonlarda görülen stabil bağlanması kombinasyonu, daha ileri iyileştirme için umut verici bir iskelet olarak öne çıkarıyor. Daha geniş anlamda, çalışma bilgisayar destekli taramanın hem güçlü yanlarını hem de sınırlarını gösteriyor: geniş kimyasal kütüphaneleri hızla birkaç gerçekçi adayla daraltabilir, ancak hangi moleküllerin gerçekten kanser hücrelerinin toksik atıklarını yönetmek için güvendikleri enzimi devre dışı bıraktığını ortaya çıkarmak için dikkatli laboratuvar deneyleri hâlâ kaçınılmazdır.
Atıf: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
Anahtar kelimeler: glyoxalase I, kanser metabolizması, bilgisayar destekli ilaç tasarımı, çinko‑bağlayıcı inhibitörler, moleküler yerleştirme