Clear Sky Science · tr
Monoklonal antikorların mannoz reseptörü yoluyla seçici temizlenmesi glikan eşleşmesine bağlıdır
İlaçlardaki şeker desenlerinin önemi
Günümüzün en başarılı ilaçlarından birçoğu monoklonal antikorlardır—kan dolaşımında haftalarca kalabilen ve kanser ile otoimmün hastalıklar gibi hedefleri hassas şekilde tanımlayan tasarlanmış proteinler. Ancak tüm antikorlar enjekte edildikten sonra aynı davranışı sergilemez. Bu çalışma, sonuçları büyük olabilecek aldatıcı derecede basit bir soruyu ele alıyor: bir antikora bağlı ince “şeker deseni” vücudun onu ne kadar hızlı uzaklaştıracağını nasıl belirliyor ve bu durum bağışıklık reaksiyonları gibi yan etkileri de şekillendirebilir mi?
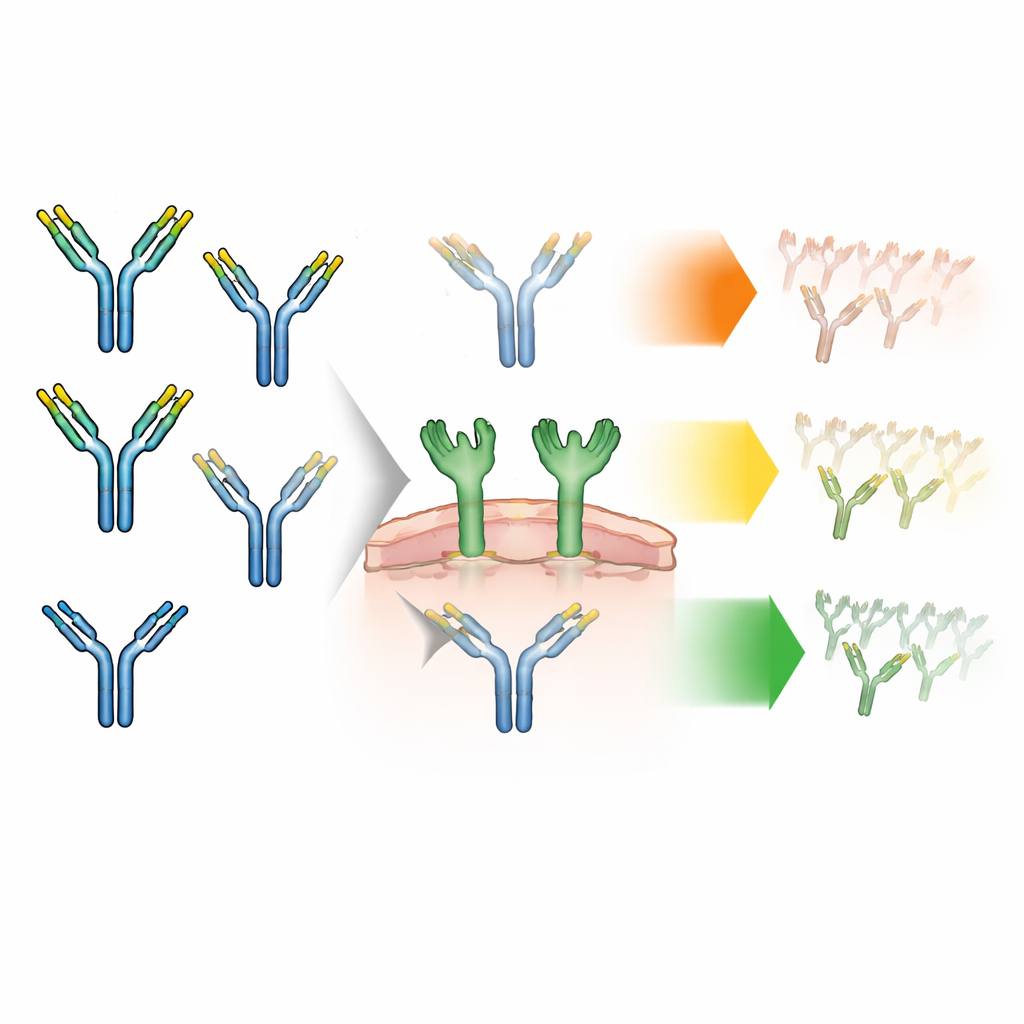
Trafik işaretleri olarak küçük şekerler
Antikorların omurgasında doğal olarak küçük şeker zincirleri—glikanlar—bulunur. Bu glikanlar çeşitli tiplerde olabilir. Çoğu “kompleks” yapıda iken, azınlığı daha basit bir tür olan “yüksek-mannoz”dur ve önceki çalışmalar bunun kan dolaşımından daha hızlı uzaklaşmayla ilişkili olduğunu göstermiştir. Her antikorun iki şeker bölgesi vardır ve bunlar bir çift oluşturur; bu çiftler eşleşmiş (simetrik çiftler) veya farklı (asimetrik çiftler) olabilir. Bugüne kadar ilaç üreticileri genellikle toplamda hangi şeker tiplerinden ne kadar bulunduğunu saydı; aynı antikor üzerindeki iki şekerin nasıl eşlendiğini sormadılar. Yazarlar, bu eşleşme deseninin antikorların immün hücrelerde bulunan ve şekerleri algılayan özel bir protein olan mannoz reseptörüyle ne kadar güçlü etkileşime gireceğini—dolayısıyla ilacın vücuttan ne kadar hızlı temizleneceğini—değiştirebileceğinden şüpheleniyordu.
Antikorları şeker çiftlerine göre ayırmak
Bunu araştırmak için ekip, yüksek-mannoz glikanları zenginleştirilmiş antikorlar tasarladı ve ardından bunları fiziksel olarak üç ana gruba ayırdı: iki kompleks şekerli antikorlar, bir kompleks ve bir yüksek-mannoz şekerli (asimetrik) antikorlar ve iki yüksek-mannoz şekerli (simetrik) antikorlar. Bu grupların boyut, şekil, yük ve stabilite gibi diğer tüm özellikler açısından neredeyse özdeş olduğundan ve normalde antikorları yıkımdan koruyan geri dönüşüm reseptörüne bağlanmalarının benzer olduğundan emin oldular. Bu, ileride hücre deneylerinde veya hayvanlarda gözlemledikleri farkların gizli hasar veya safsızlıklardan değil yalnızca şeker eşleşmesinden kaynaklandığını izlemeyi mümkün kıldı.
Hücrelerin antikorları içeri çekmesini izlemek
Sonra araştırmacılar, her bir şeker deseninin mannoz reseptörü taşıyan hücreler tarafından antikorların ne kadar hızlı yutulmasına izin verdiğini sordular. Farklı antikor fraksiyonlarını floresan bir etiketle işaretleyip bu reseptörü sergilemesi için değiştirilmiş insan hücreleri ile inkübe ettiler. Yaklaşık üç gün boyunca hücre içindeki parlaklığı alımla ölçerek izlediler. Tüm antikorlar bir dereceye kadar alındı, ancak hızlar farklıydı: iki yüksek-mannoz şekerli olanlar en hızlı içeri alındı, bir yüksek-mannozlu olanlar orta hızda, sadece kompleks şekerli olanlar ise en yavaş alındı. Ekip mannan—mannoz reseptörüyle yarışan doğal bir şeker—eklediğinde yüksek-mannoz antikorların alımı keskin şekilde düştü; bu da hızlı içeri alımın büyük ölçüde bu reseptörden kaynaklandığını doğruladı.
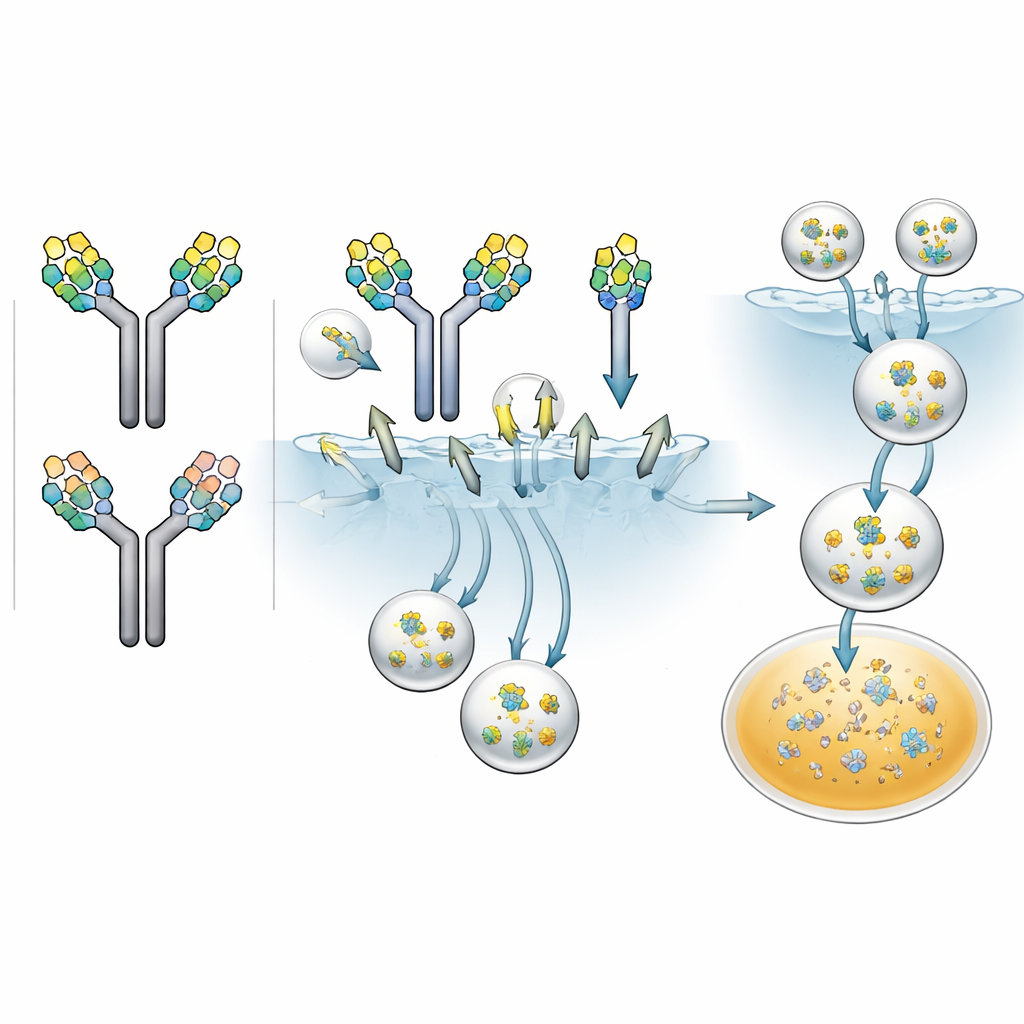
Şeker işaretli antikorları canlı hayvanlarda takip etmek
Belirleyici test, bu hücresel farkların gerçek dünyadaki ilaç davranışına yansıyıp yansımayacağıydı. Bilim insanları hem simetrik hem asimetrik yüksek-mannoz çiftleriyle zenginleştirilmiş ve yalnızca kompleks çiftleri içeren bir ilaç ürünü formüle edip bunu sıçanlara enjekte ettiler. Duyarlı kütle spektrometresi yöntemleri kullanarak sadece toplam antikor düzeyini iki hafta boyunca takip etmekle kalmayıp, aynı zamanda her bir şeker eşleşmesinin zaman içinde nasıl azaldığını da izleyebildiler. Desen çarpıcıydı: iki yüksek-mannoz şekerli antikorlar en hızlı kayboldu ve yarı ömrü yaklaşık 2,4 gün; bir yüksek-mannoz şekerli olanlar daha uzun sürdü, yaklaşık 7,2 gün; sadece kompleks şekerli olanlar ise yaklaşık 17,4 gün dayandı. Zaman içindeki maruziyet—koncentrasyon eğrisi altındaki alan—iki yüksek-mannoz çift için kompleks-sadece çifte göre %38'e, karışık çift için %73'e düştü. Özetle, her ekstra yüksek-mannoz şeker mannoz reseptörü için ilave bir "beni temizle" bayrağı gibi davrandı.
Daha güvenli ve daha uzun etkili ilaçlar için ne anlama geliyor
Hastalar açısından bu sonuçlar kağıt üzerinde benzer görünen iki antikor ilacının vücutta neden farklı davranabildiğini açıklığa kavuşturuyor. Çalışma, sadece yüksek-mannoz şekerlerin varlığının değil, aynı zamanda eşleşmesinin de antikorların ne kadar hızlı uzaklaştırılacağını güçlü şekilde yönlendirdiğini; muhtemelen mannoz reseptörü aracılı alım ve immün hücreler içindeki parçalanma üzerinden etkili olduğunu gösteriyor. Aynı yol antigenerleri bağışıklık yanıtını tetikleyen mekanizmalara besleyebildiği için bu şeker desenleri anti-ilaç antikorları ve alerjik reaksiyon riski üzerinde de etkili olabilir. Yazarlar, üreticilerin antikor terapilerini tasarlarken ve test ederken yalnızca toplam şeker bileşimini değil, glikan eşleşmesini de izlemeleri ve kontrol etmeleri gerektiğini savunuyor. Bunu yapmak, daha tahmin edilebilir dozlama, daha uzun süren yararlar ve istenmeyen bağışıklık yanıtı olasılığının azaltılmasına yardımcı olabilir.
Atıf: Baumeister, J., Meudt, M., Wei, W. et al. Selective clearance of monoclonal antibodies via the mannose receptor is dependent on glycan pairing. Sci Rep 16, 8489 (2026). https://doi.org/10.1038/s41598-026-40268-1
Anahtar kelimeler: monoklonal antikorlar, glikozilasyon, mannoz reseptörü, farmakokinetik, immünojenikite