Clear Sky Science · tr
RBP4, PI3K/AKT sinyal yolunu inhibe ederek ve makrofajları M1 tipine polarize ederek dil skuamöz hücreli karsinomunun ilerlemesini engelliyor
Dil Kanserinin Yeni Yaklaşımlara İhtiyacı Neden Var
Dil kanseri, konuşma, yeme ve tat alma yetisini ellerinden alabilir; ameliyat, kemoterapi ve radyasyon uygulansa bile uzun dönem sağkalım çoğu zaman hayal kırıklığı yaratır. Bu çalışma, kandaki beklenmedik bir yardımcı olan A vitamini taşıyıcısı protein RBP4’ü araştırıyor ve bu proteinin hem dil tümörlerinin büyümesini yavaşlatabildiğini hem de vücudun kendi bağışıklık savunmasını harekete geçirebildiğini gösteriyor. Molekülün kanser hücreleri içindeki ve çevresindeki bağışıklık hücreleri üzerindeki etkilerini açığa çıkararak, gelecekte tedavileri daha etkili ve daha az zarar verici kılabilecek yeni stratejilere işaret ediyor.
Dil Tümörlerinde Gizli Bir Protein
Araştırmacılar, dil skuamöz hücreli karsinomlu hastaların zaman içindeki gidişatını tahmin edebilecek hangi bağışıklık ilişkili genlerin önemli olduğunu görmek için büyük kanser gen veri tabanlarını taramakla başladılar. Yüzlerce aday arasında, kan akışında A vitaminini taşımasıyla en çok tanınan protein RBP4 özellikle ilgi çekici olarak öne çıktı. Ekip, tümör örneklerini çevredeki sağlıklı dil dokusuyla karşılaştırdığında RBP4 düzeylerinin kanser dokusunda tutarlı şekilde çok daha düşük olduğunu buldu. Bu desen, birkaç bağımsız veri kümesinde ve 20 hastadan alınan doku örneklerinde doğrulanarak RBP4 kaybının bu hastalığın yaygın bir özelliği olduğunu gösterdi.
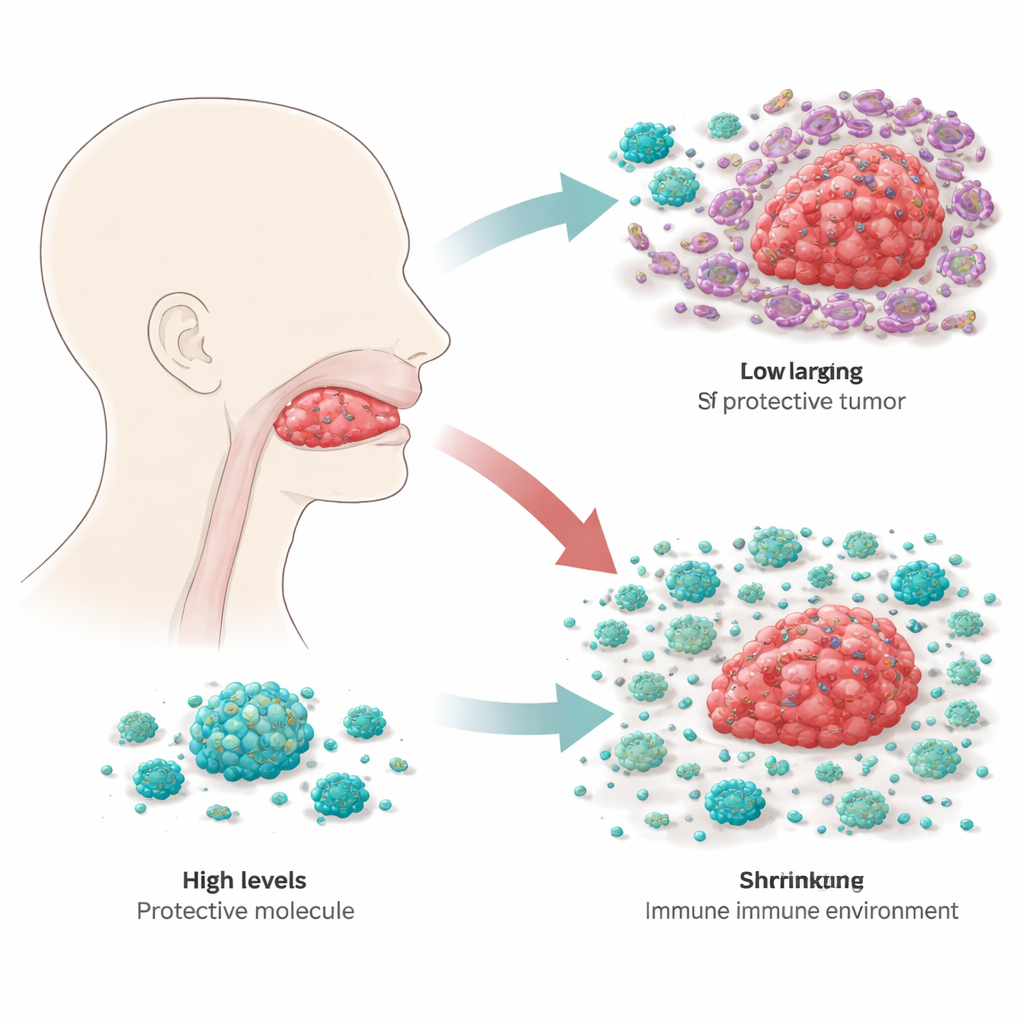
Tümör Büyümesini İçten Yavaşlatmak
RBP4’ün dil kanseri hücrelerinde gerçekte ne yaptığını öğrenmek için bilim insanları, tümör hücre hatlarını ya ekstra RBP4 üretir hâle getirdi ya da onu çok daha az üreten hâle getirdi. Laboratuvar kaplarında, daha yüksek RBP4’e sahip hücreler daha yavaş büyürken, RBP4 azaltılmış olanlar daha hızlı çoğalıyor ve yapay membranlar üzerinden daha iyi hareket edip istilâ ediyorlardı; bu davranışlar yayılma ve nüks ile bağlantılıdır. Bu modifiye hücreler farelere nakledildiğinde, ekstra RBP4’e sahip tümörler daha küçük kaldı, oysa RBP4 azaltılmış tümörler daha agresif büyüdü. Hücre içindeki ana büyüme-kontrol anahtarlarını izleyerek, ekip RBP4’ün birçok kanserin içsel gaz pedalı olarak kullandığı PI3K–AKT–mTOR adlı ana büyüme yolunu baskıladığını gösterdi. RBP4 yüksek olduğunda bu yol daha sessiz oluyor ve tümör hücreleri göç etmelerine yardım eden esnek, hareketli hâli benimsemekte daha az başarılı oluyorlar.
Bağışıklık Hücrelerini Tümör Savaşçılarına Dönüştürmek
Kanser izole bir şekilde büyümez; bağışıklık hücreleri, kan damarları ve destek hücrelerinden oluşan bir mahalle içinde yaşar; buna tümör mikroçevresi denir. Burada makrofajlar—tümörlere ya saldırabilen ya da onlara yardımcı olabilen büyük bağışıklık hücreleri—merkezi bir rol oynar. Araştırmacılar, daha fazla RBP4 içeren tümörlerin genellikle tümör öldürücü ve inflamasyonla ilişkili “M1” tipi makrofajları daha çok barındırma eğiliminde olduğunu; oysa sıklıkla tümör büyümesini destekleyen “M2” tipinin daha az bulunduğunu fark ettiler. Hücre kültüründe, saflaştırılmış RBP4’e maruz bırakılan veya daha fazla RBP4 salgılayacak şekilde genetik olarak değiştirilmiş dil kanseri hücreleri ile temas eden makrofajlar, M1, tümörle savaşan duruma kaydılar. Kanser hücrelerinde RBP4 azaltıldığında ise makrofajlar daha tümör-dostu profile doğru kayma eğiliminde oldu.
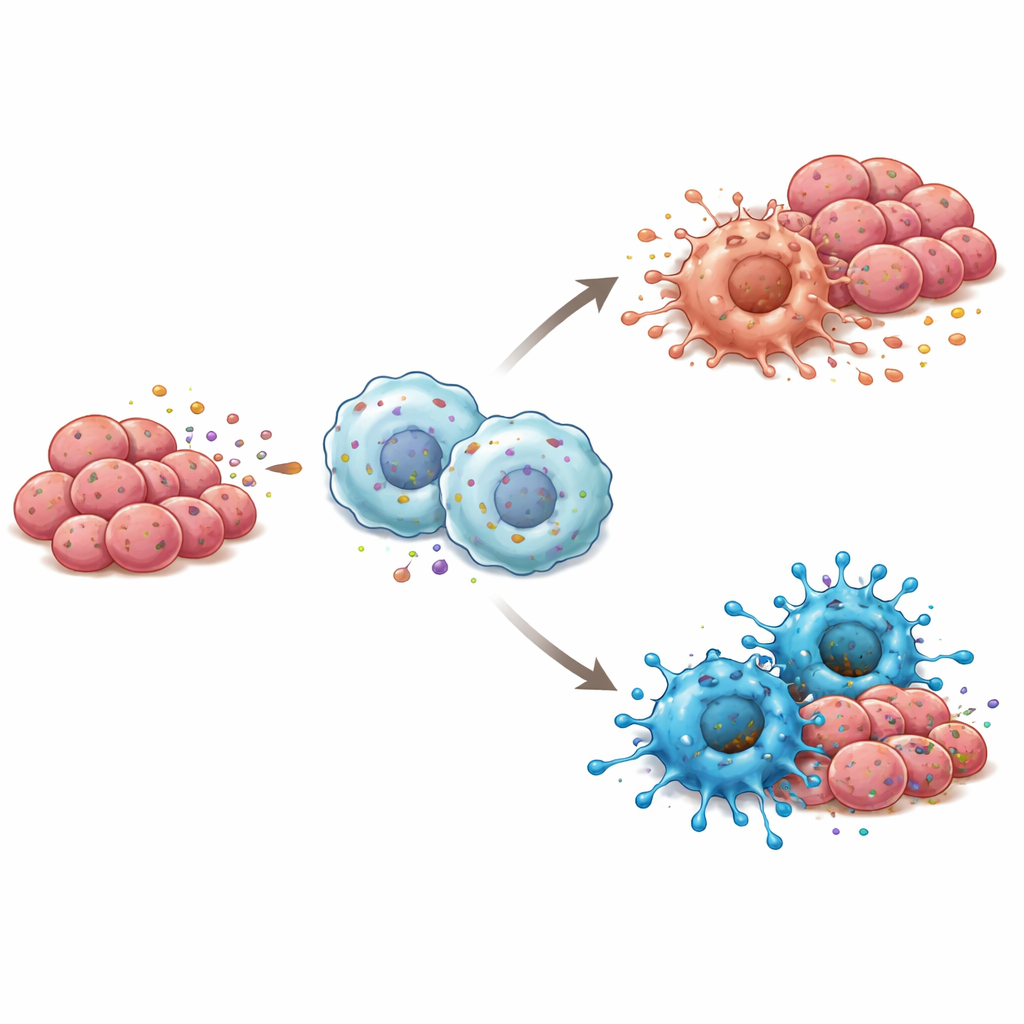
Bağışıklık Değişimini Sağlayan Sinyal Yolları
RBP4’ün makrofajları tümöre daha düşmanca bir tutuma itme biçimini anlamak için araştırmacılar bu bağışıklık hücrelerinde hangi içsel alarm sistemlerinin aktifleştiğini incelediler. RBP4’ün makrofaj yüzeyindeki TLR4 adlı bir dedektörü uyardığını ve bunun da inflamatuar yanıtları yöneten anahtar bir anahtar olan NF-κB’yi aktif hale getirdiğini buldular. TLR4’ü kimyasal bir inhibitörle bloke etmek bu zincir reaksiyonunu kapattı ve RBP4 varlığında bile makrofajların M1 durumunu benimsemesini engelledi. Farelerde, RBP4 açısından zengin dil kanseri hücrelerinden oluşan ve makrofajlarla karıştırılan tümörler daha yavaş büyüdü ve daha fazla M1 tipi hücre içerdi; ayrıca daha güçlü TLR4 ve NF-κB aktivitesi gözlendi; bu da bu yolun RBP4’ün bağışıklık etkileri için kilit olduğunu pekiştirdi.
Gelecekteki Tedavi İçin Ne Anlama Gelebilir
Bir arada ele alındığında, çalışma RBP4’ü dil kanseri üzerinde çift yönlü çalışan bir fren olarak betimliyor: tümör hücreleri içinde aşırı aktif bir büyüme devresini kısıyor, tümörün mahalle yapısında ise makrofajları daha tetikte savunuculara dönüştürmeye yardımcı oluyor. RBP4’ün hedefleriyle tam olarak nasıl etkileştiği ve en güvenli şekilde nasıl artırılabileceği gibi pek çok soru hâlâ cevapsız olsa da, çalışma RBP4’ün işlevlerini geri kazandırmanın veya taklit etmenin hem tümör genişlemesini yavaşlatabileceğini hem de vücudun kanser üzerindeki bağışıklık baskısını güçlendirebileceğini öne sürüyor. Hastalar için bu, sadece tümörü kesip atmakla kalmayıp aynı zamanda içsel devrelerini ve yerel “ekosistemi” yeniden şekillendirerek nüksü engelleyebilecek gelecekteki tedavilerin umudunu doğuruyor.
Atıf: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
Anahtar kelimeler: dil kanseri, RBP4, tümör mikroçevresi, makrofajlar, PI3K AKT yolu