Clear Sky Science · tr
Tümörlerde bakteriyel kolonizasyon bağışıklık aktivasyonunu ve kontrol noktası engelleme etkinliğini arttırıyor
Tümörlerdeki Küçük Kiracılar Neden Önemli?
Kanser tedavisi, vücudun kendi bağışıklık hücrelerini tümörlere karşı serbest bırakan immünoterapilerle dönüştü. Yine de birçok hasta hâlâ az fayda görüyor ve kimin yanıt vereceğini öngörmek zor oldu. Bu çalışma, dengeleri değiştirebilecek beklenmedik bir oyuncuyu inceliyor: tümörlerin içinde yaşayan bakteriler. Fare kanser modellerini inceleyerek, araştırmacılar bu mikroskobik kiracıların tümörün içinde ve çevresinde bağışıklık sisteminin nasıl davrandığını değiştirebileceğini ve bunun da yaygın olarak kullanılan anti–PD-1 immünoterapisinin iyi çalışıp çalışmayacağını belirleyebileceğini gösteriyor.
Tümörlerin İçindeki Gizli Bakteriler
Yıllarca en çok dikkat, bağırsakta yaşayan trilyonlarca mikroba ve bunların genel bağışıklığı nasıl şekillendirdiğine odaklandı. Daha yakın zamanda, birçok insan tümörünün küçük ama aktif bakteriyel topluluklar barındırdığı keşfedildi. Bu çalışmanın ekibi iki temel soruyu sordu: yaygın kullanılan fare tümör modelleri de bakteri içeriyor mu ve içeriyorsa bu bakteriler gerçekten tümörlerin büyümesini ve tedaviye yanıtını etkiliyor mu? İki modeli karşılaştırdılar: MCA-205 (bir tür sarkom) ve MOC1 (baş ve boyun kanseri modeli). DNA tabanlı testler, dizileme ve kültür yöntemleri kullanarak, MCA-205 tümörlerinin sistematik olarak canlı bakteriler taşıdığını, MOC1 tümörlerinin ise ağızda bol bakteri olsa bile taşımadığını buldular. MCA-205’te bakteriyel düzeylerin tümörler büyüdükçe artma eğiliminde olması, büyüyen tümörün mikroplar için uygun bir niş sağladığını düşündürüyor.
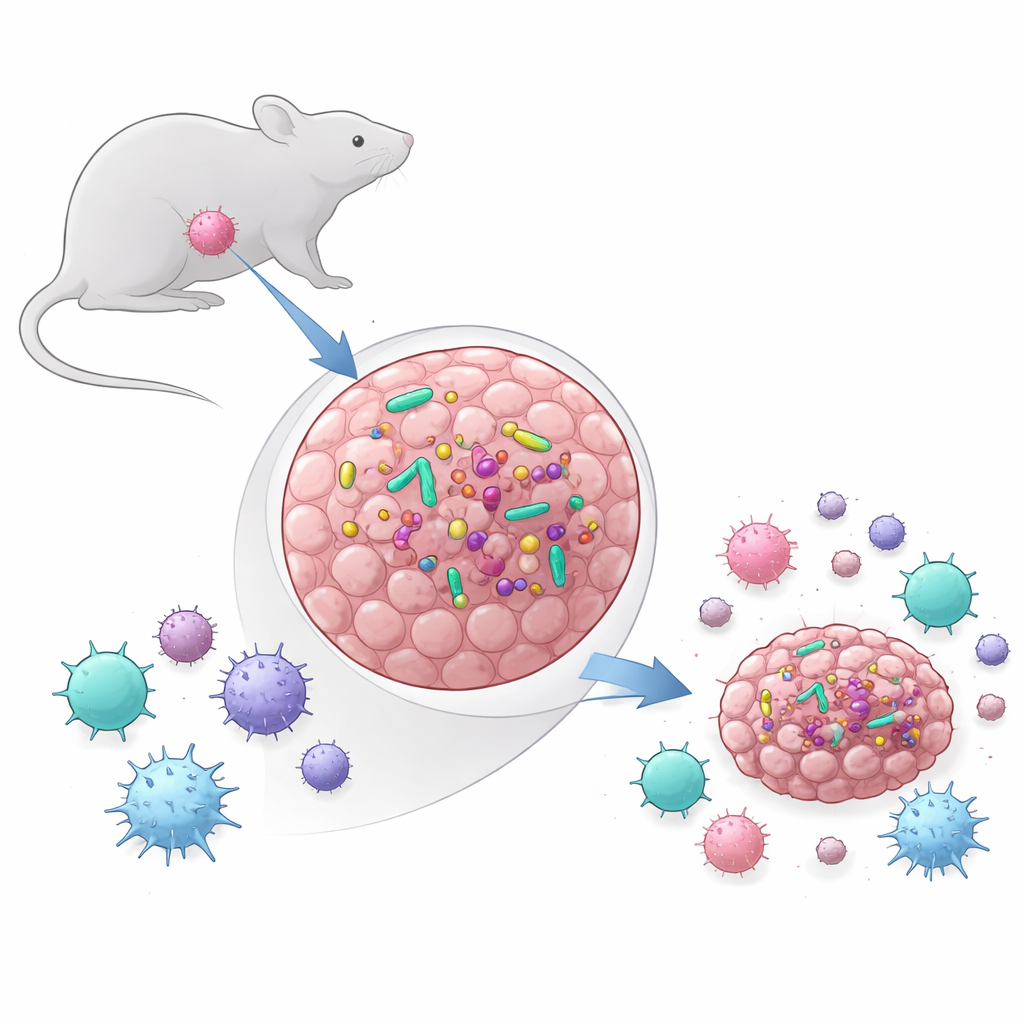
Böceklerin Geldiği Yeri İzlemek
Tümörlerin içinde bakteri bulunması başka bir soruyu gündeme getirdi: bu istilacılar deriden, ağızdan mı yoksa bağırsaktan mı geliyor? Tümörlerdeki bakteriyel DNA’yı dışkı, deri sürüntüleri ve oral sürüntülerle karşılaştırarak, araştırmacılar tümör içi topluluğun bağırsak ve ağızdaki zengin ekosistemlere göre daha basit ve daha az çeşitli olduğunu buldular. Tümörlerdeki bakteri tiplerinin çoğu gastrointestinal sistemde görülen çeşitlerle örtüşürken, nispeten azı cilttekilerle eşleşti. Bu, bakterilerin bağırsaktan veya ağız boşluğundan kana sızıp tümörü tohumlayabileceğini; ancak yalnızca belirli türlerin kalıcı olmayı başardığını düşündürüyor. Bakteriyel grup karışımı, birkaç insan kanserinde rapor edilenlerle benzerlik gösterdi ve bu fare tümörlerinin gerçek dünya tümör–mikrop etkileşimlerini modelleyebileceği fikrini güçlendirdi.
Tümör Bakterileri İmmünoterapi Başarısını Nasıl Şekillendiriyor
Çalışmanın merkezi bulgusu, tümör içinde yaşayan bakterilerin anti–PD-1 terapisi gibi bir kontrol noktası engelleyicinin başarısını belirleyebileceğidir; bu ilaç yorgun düşmüş öldürücü T hücrelerini yeniden canlandırmayı amaçlar. Araştırmacılar, tümöre nüfuz eden ve yerel bakterileri silen ancak bağırsak kolonizasyonunu büyük ölçüde koruyan antibiyotikler kullandığında, MCA-205 tümörlerinin anti–PD-1’e karşı çok daha az yanıt verdiğini gözlemlediler. Bağırsak mikrobiyotasının genişçe bozulması yanıtları daha da düşürdü. Buna karşılık, baştan tespit edilebilir bakterisi olmayan MOC1 tümörlerinde antibiyotikler hem bakteri yükü hem de tedavi sonucu üzerinde az etki gösterdi. MCA-205’te anti–PD-1’e yanıt verip küçülen tümörler, tedaviye dirençli olanlara göre genellikle daha fazla bakteri içeriyordu; bu da yüksek tümör içi bakteriyel yük ile daha iyi büyüme kontrolü arasında bağlantı kuruyor.
Bağışıklık Cephesinin İçinde
Bakterilerin bağışıklık dengesini nasıl eğdiğini anlamak için araştırmacılar tümörlerin içinde ve çevresindeki bağışıklık hücrelerini incelediler. Tümör nüfuz eden antibiyotiklerle tümör içi bakteriler uzaklaştırıldığında, daha az öldürücü CD8 T hücresi tümöre giriyor ve bu hücrelerin düzenleyici T hücrelerine oranı baskı lehine kayıyordu. Tümör materyalini toplayıp T hücrelerini aktive eden keşifçi hücreler olan dendritik hücreler de sayıca azaldı ve bakteriler yokken daha düşük aktivasyon belirtileri gösterdi. İlginç şekilde, tümöre zararsız ek bir E. coli suşu eklemek ya da temel bir mikrop algılama yolunu (MyD88) ana bağışıklık hücrelerinde devre dışı bırakmak terapinin etkinliğini artırmadı. Bu, herhangi bir bakteri varlığının veya basit alarm sinyalinin yeterli olmadığını; belirli toplulukların ve bağışıklık sistemiyle daha nüanslı iletişimin muhtemelen gerekli olduğunu ima ediyor.
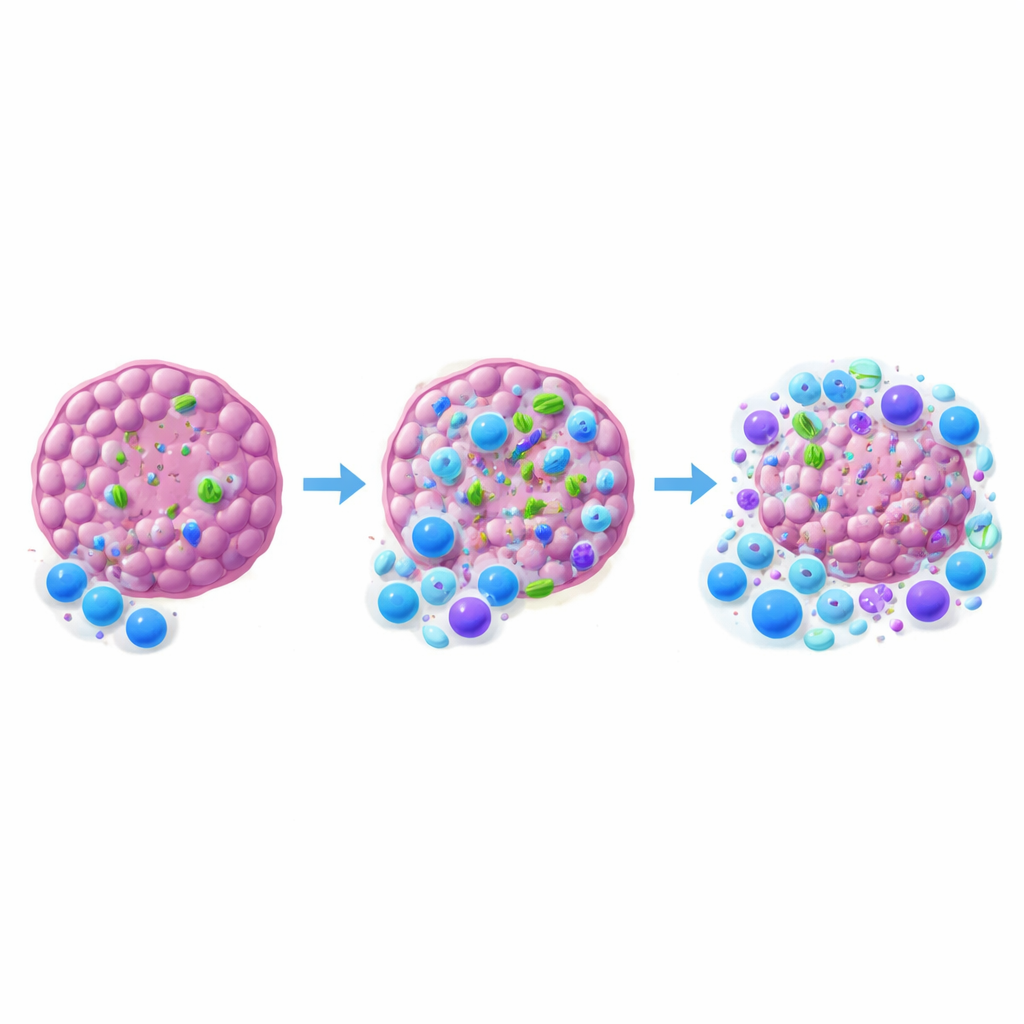
Gelecekteki Kanser Bakımı İçin Anlamı
Uzman olmayan biri için çıkarım, tümör içinde yaşayan bakterilerin basit seyirciler olmadığıdır. En az bazı kanserlerde onlar doğru bağışıklık hücrelerini tümöre çekmeye yardımcı olur ve anti–PD-1 ilaçlarının etkisini destekler. Diğer tümörler neredeyse bakteri içermeyebilir ve çok farklı yanıt verebilir. Bilim insanları farelerde yeni tedaviler tasarlayıp test ederken, belli bir tümör modelinin bakteri taşıyıp taşımadığını—ve hangi türleri taşıdığını—bilmek, sonuçları yorumlamak ve hastalara aktarılacak stratejileri seçmek için hayati olabilir. Uzun vadede, tümör içindeki küçük toplulukları dikkatle ayarlamak, ilaçlar ve bağışıklık hücreleriyle birlikte kanser immünoterapisini iyileştirmek için yeni bir araç haline gelebilir.
Atıf: Rolig, A.S., Ziglari, T., McGee, G.H. et al. Bacterial colonization of tumors drives immune activation and checkpoint blockade efficacy. Sci Rep 16, 8464 (2026). https://doi.org/10.1038/s41598-026-39758-z
Anahtar kelimeler: tümör içi mikrobiyota, kanser immünoterapisi, anti-PD-1, tümör mikroçevresi, bakteriler ve tümörler