Clear Sky Science · tr
PAR1 kinaz ailesinin iki üyesi PAR1b ve PAR1a arasında PAR1b'siz farelerin hayatta kalmasında gizli yedeklilik
Hücreler Kırık DNA İçin Nasıl Yedek Plan Bulur
Hücrelerimiz sürekli olarak DNA hasarıyla karşılaşıyor ve onarım sistemleri başarısız olursa sonuç kanser veya gelişimsel ölümdür. Bu çalışma farelerde şaşırtıcı bir kurtarma mekanizmasını araştırıyor: BRCA1 gibi kanserle ilişkilendirilen önemli bir genin işini yapmasına yardımcı olan anahtar bir protein eksik olduğunda, yakın bir akrabası sessizce devreye giriyor. Bu bulgu, erken embriyoların hayatta kalmak için gen kontrol sistemlerini nasıl yeniden düzenleyebileceğini gösteriyor ve neden bazı genetik kusurların öldürücü olurken bazılarının beklenmedik şekilde tolere edildiğine dair yeni içgörüler sunuyor.
Gizli Bir Role Sahip Hücre Düzenleyiciler Ailesi
Araştırmacılar, hücrelerin iç organizasyonunu korumaya yardımcı olan PAR1 kinaz adı verilen bir enzim ailesine odaklandı. Aile üyelerinden biri olan PAR1b, BRCA1’i hücre çekirdeğine yönlendirdiği için daha önce gösterilmişti; çekirdekte BRCA1 doğru DNA onarımını denetler ve hassas DNA çoğaltma bölgelerini korur. BRCA1’in farelerde tamamen ortadan kaldırılması embriyonik gelişimin erken safhalarında öldürücüdür; bu da önemini vurgular. Buna karşın, PAR1b’den tamamen yoksun farelerin yetişkinliğe kadar yaşaması şaşırtıcıydı; PAR1b BRCA1’den önce yer almasına rağmen. Bu çelişki, başka bir PAR1 kinazın belirli koşullarda sessizce PAR1b’nin yerini alabileceğini düşündürdü.
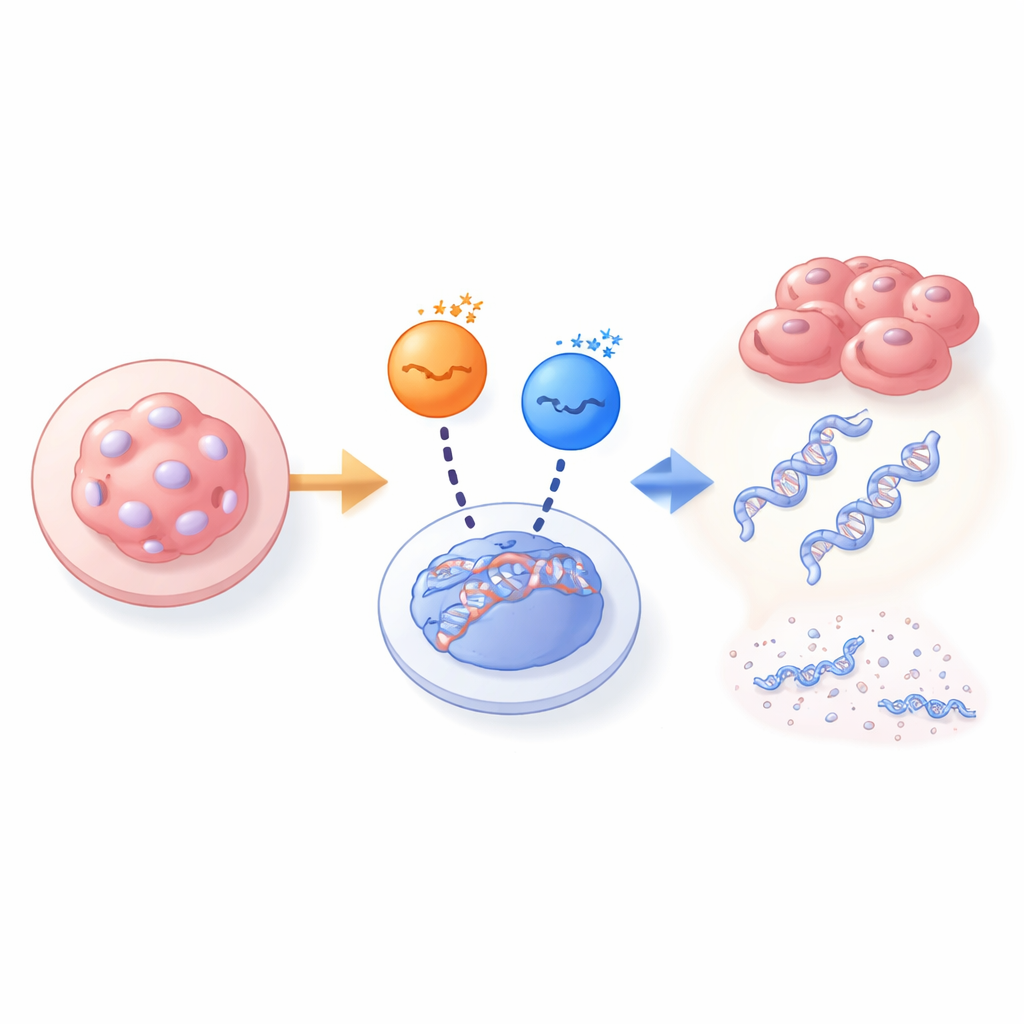
Bir Kinaz Arızalandığında Diğeri Devreye Giriyor
Bu gizemi araştırmak için ekip, normal embriyolardan elde edilen fare embriyonik fibroblastlarını PAR1b’den tamamen yoksun embriyolardan elde edilenlerle karşılaştırdı. Normal hücrelerde PAR1b’yi kapatmak, çekirdek içindeki BRCA1’i keskin biçimde azalttı ve DNA kırık göstergelerinde ani bir artışa yol açtı; bu da hücre büyümesini engelledi. Diğer PAR1 kinazların (PAR1a, PAR1c, PAR1d) susturulmasının ise çok az etkisi oldu. Ancak PAR1b-farelerinden türetilen hücrelerde PAR1b olmamasına rağmen BRCA1 yine de çekirdekte mevcuttu ve DNA nispeten sağlam kaldı. Bu PAR1b-null hücrelerde PAR1a’nın ortadan kaldırılması şimdi öldürücü hale gelirken, PAR1c veya PAR1d’nin ortadan kaldırılması böyle değildi. Bu bağımlılık değişimi, PAR1a’nın PAR1b’nin BRCA1’i yönlendirme rolünü devraldığını, ancak bunun yalnızca başından beri PAR1b’den yoksun olan embriyolarda gerçekleştiğini gösterdi.
Hayatta Kalma Stratejisi Olarak Erken Epigenetik Yeniden Kablolama
Araştırmacılar, bu gizli yedek sistemin epigenetikle—DNA’nın paketlenme ve kimyasal işaretlenme şeklini değiştirerek genleri açıp kapama biçimiyle—bağlantılı olduğunu düşündüler. Kromatin açıklığını genom çapında ölçen bir analiz kullanarak, normal ve PAR1b-null hücreler arasında DNA erişilebilirliğinin farklı olduğu binlerce bölge buldular. Birçok değişiklik kromozomların nasıl sarıldığı ve modifiye edildiğini kontrol eden genleri içeriyordu; bu da gen kontrol ağının geniş çapta yeniden programlandığına işaret ediyordu. Öne çıkan etkilerden biri, genelde BRCA1’in daha doğru onarım yöntemine karşı hücreleri hızlı ve basit bir onarım yoluna iten 53BP1 genindeydi. PAR1b-null hücrelerde 53BP1 gen gövdesi daha sıkı paketlenmişti ve RNA ile protein düzeyleri çok daha düşüktü.
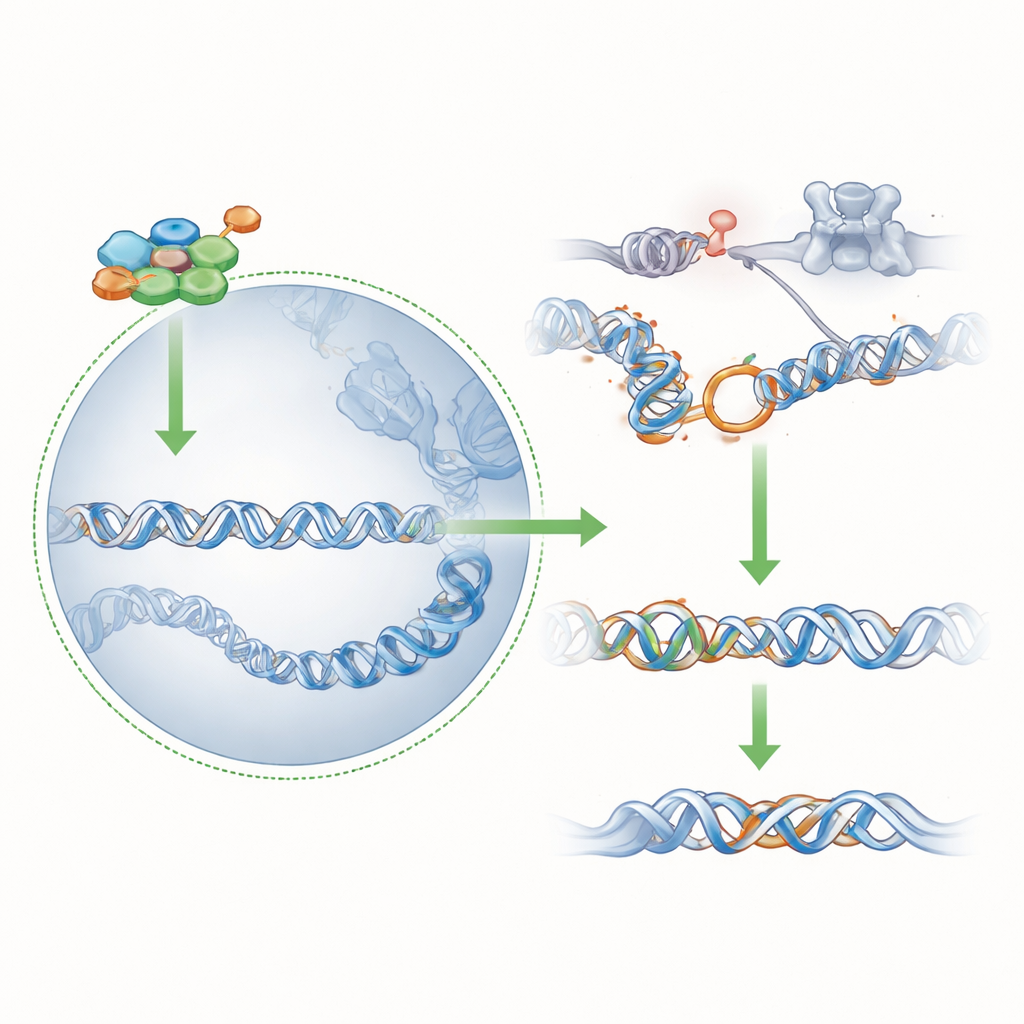
Onarım Yolları Arasındaki Dengede Kayma
53BP1’i azaltarak, embriyo aslında BRCA1’in tam gücüne olan bağımlılığını düşürüyor: çekirdeğe PAR1b yerine PAR1a tarafından taşınan mütevazı bir BRCA1 miktarı bile artık yeterli doğru onarımı destekleyerek hücrelerin yaşamasını sağlayabiliyor. Tüm PAR1 kinazlarını kapatan bakteriyel bir protein kullanan deneyler, PAR1b-null hücrelerde BRCA1’in çekirdek varlığının hâlâ PAR1 aile aktivitesine, özellikle PAR1a’ya bağlı olduğunu doğruladı. Birlikte, sonuçlar PAR1b’nin erken kaybının kromatin ve DNA onarım ağlarının hızlı bir şekilde yeniden şekillenmesini tetiklediği; BRCA1’in rakibi olan 53BP1’i susturduğu ve PAR1a’nın PAR1b yerine geçme yeteneğini ortaya çıkardığı bir tablo çiziyor.
Hastalık ve Tedavi İçin Anlamı
Bu çalışma “kriptik yedeklilik” fikrini tanıtıyor: var olan ancak normalde sessiz kalan ve yalnızca anahtar bir bileşen çok erken bir gelişim aşamasında kaybolduğunda görünür hâle gelen bir yedek fonksiyon. Farelerde bu, PAR1b kaybının BRCA1 kaybı gibi öldürücü olmasını engelliyor. Bulgular ayrıca, bazı PAR1b’yi zarar veren varyantlara sahip kişilerin benzer yedek mekanizmalar devreye girdiği için hayatta kalabileceğini, ancak bunun beyin fonksiyonu, metabolizma veya kanser riski üzerinde olası sonuçları olabileceğini düşündürüyor. Uzun vadede, erken epigenetik ayarlamaların 53BP1’i nasıl susturduğunu ve BRCA1 denetimini PAR1b’den PAR1a’ya nasıl kaydırdığını anlamak, bu değişiklikleri kasıtlı olarak taklit etmeye yönelik stratejiler geliştirmeyi ilham verebilir—ya PAR1b’yi kaybeden hücreleri korumak ya da kanser tedavisinde DNA onarım yollarını hassas şekilde ayarlamak için.
Atıf: Murata-Kamiya, N., Del Valle Lazarte, A.A., Kikuchi, I. et al. Cryptic redundancy between PAR1b and PAR1a, two members of the PAR1 kinase family, in the survival of PAR1b-knockout mice. Sci Rep 16, 5971 (2026). https://doi.org/10.1038/s41598-026-39737-4
Anahtar kelimeler: BRCA1, DNA onarımı, kinaz yedekliliği, epigenetik düzenleme, embriyonik gelişim