Clear Sky Science · tr
Otizm spektrum bozukluğu ile ilişkili Sema5A p.Arg676Cys, Arf6/FE65 sinyalini tetikleyip hücre morfogenezisini bozar
Çok Küçük Bir Değişiklik Beyin Bağlantılarını Nasıl Bozabilir?
Otizm spektrum bozukluğu, insanların iletişim kurma, etkileşim ve çevreye yanıt verme biçimlerini etkiler; ancak bir DNA değişikliğinin nasıl farklılaşmış beyin işlevine yol açtığına dair biyolojik adımlar sıklıkla gizemini korur. Bu çalışma, Sema5A adlı bir beyin “yönlendirme” proteinindeki böyle bir genetik değişikliği inceliyor ve bu proteindeki tek bir yer değiştiren yapı taşının genç nöronların gereğinden uzun, dolanmış dallar büyütmesine nasıl yol açabileceğini sıra dışı ayrıntıyla gösteriyor. Bu mikroskobik bağlantı hatasını anlamak, zamanla araştırmacıların beyin hücrelerini daha sağlıklı bir şekle doğru yönlendirecek tedaviler tasarlamasına yardımcı olabilir.
Çok Fazla Büyüyen Beyin Hücreleri
Beyin gelişimi sırasında genç sinir hücreleri, doğru eşleri arayan uzun, ince uzantılar gönderir; bunlar düşünce ve davranışın temelini oluşturan devreleri kurar. Bu büyümenin sıkı kontrol altında olması gerekir: dallanma çok zayıfsa hücreler bağlantı kuramaz; çok fazlaysa devreler gürültülü veya yanlış kablolanmış hale gelebilir. Önceki çalışmalar, 676. pozisyondaki bir amino asidin arginin yerine sisteine değiştiği otizm bağlantılı bir Sema5A versiyonunun, kültürdeki sinir hücrelerinin olağandışı uzun süreçler büyütmesine yol açtığını göstermişti. Yeni çalışma, bu mutant Sema5A’nın böyle kontrolsüz büyümeyi tetiklemek için hangi iç anahtarları ve yardımcı proteinleri kullandığını ortaya çıkarmayı amaçladı.
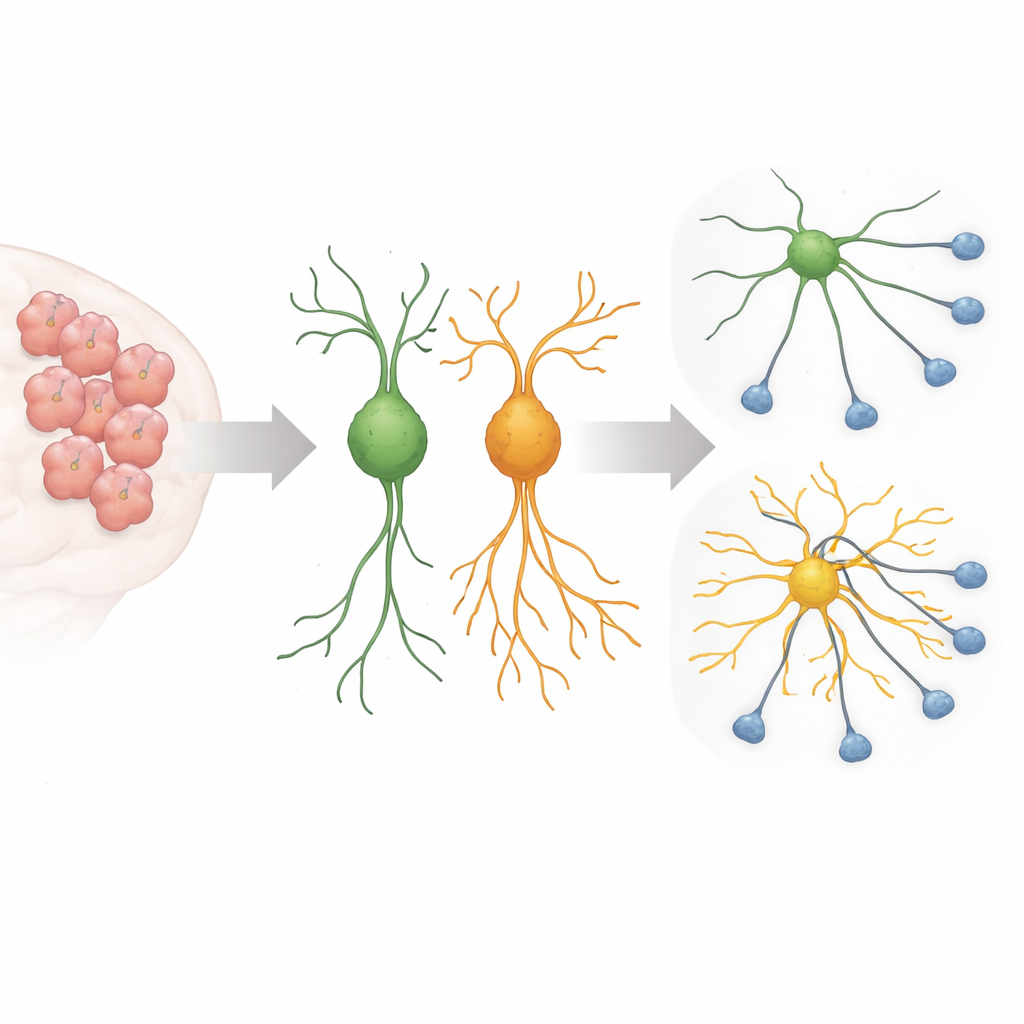
Hücre İçindeki Yanıltıcı Bir Sinyal
Araştırmacılar, hücre zarını ve uzantıları destekleyen iç iskeleti şekillendirmeye yardımcı olduğu bilinen küçük bir moleküler anahtar olan Arf6 ile bir iskambil proteini (iskele proteini) olan FE65’e odaklandı. Fare kaynaklı sinir benzeri hücrelerde ve primer fare beyin hücrelerinde bu proteinleri seçici olarak azaltmak için CRISPR–Cas13 sistemi kullanıldığında, Arf6 veya FE65 seviyelerinin düşürülmesinin mutant Sema5A’nın neden olduğu aşırı uzamayı keskin şekilde azalttığı bulundu. Uzun, örümcekimsi uzantılar daha tipik uzunluklara çekildi ve nöronal olgunlaşma belirteçleri düştü; bu da mutasyonun etkisinin büyük ölçüde bu özel sinyal yoluna bağlı olduğunu düşündürüyor.
Hücrenin Şekil Motoruna Bağlanma
Nöronların içinde, aktini—hücre dallarındaki başlıca yapısal filament—kontrol ederek şekil sağlayan bir molekül ailesi bulunur. Bu ailenin kilit üyelerinden Rac1, normalde nörit uzamasına yardımcı olmak için aktive olur, ancak aşırı aktivite kontrolsüz büyümeyi tetikleyebilir. Ekip, normal Sema5A taşıyan hücrelerde Arf6’nın sağlıklı uzama sırasında olağan Rac1 aktivasyonu için gerekli olduğunu, oysa FE65’in bunun için zorunlu olmadığını gösterdi. Ancak mutant Sema5A bulunan hücrelerde hem Arf6 hem de FE65 kritik hale geldi: bunlardan herhangi birini azaltmak ya da hücreyi ELMO2 ile bağlanan FE65 bölgesiyle aşırı doldurmak, anormal derecede yüksek Rac1 aktivitesini normale doğru düşürdü. Bu, zararlı Sema5A versiyonunun Rac1’i aşırı uyarmak ve nöritleri gereğinden fazla uzatmak için özellikle Arf6–FE65–ELMO2–DOCK5 kompleksiyle bağlantı kurduğunu ima ediyor.
Sinyal Ortaklarının Yoğun Bir Merkezi
Bu parçaların nasıl bir araya geldiğini görmek için bilim insanları ayrıca ELMO2 tabanlı “sinyalosomları”—büyüme sinyallerini iletmek üzere bir araya gelen protein kümeleri—in de incelemesini yaptı. Arf6 veya FE65 azaltıldığında, mutant Sema5A ifade eden hücrelerin gövdelerinde ve büyüyen uçlarında daha az ELMO2 kompleksi oluştu; bu da Arf6 ve FE65’in Sema5A mutasyonunu hücre şekline fiziksel bir değişime dönüştüren mekanizmayı oluşturmaya yardımcı olduğu fikriyle uyumlu. Çalışma, Arf6 ve Rac1 gibi küçük moleküler anahtarların, FE65 gibi iskeletleyiciler tarafından desteklenerek birçok otizm ilişkili geni beyin devrelerinin son mimarisiyle bağlayan merkezi düğümler olarak işlev gördüğü daha geniş bir tabloya oturuyor.
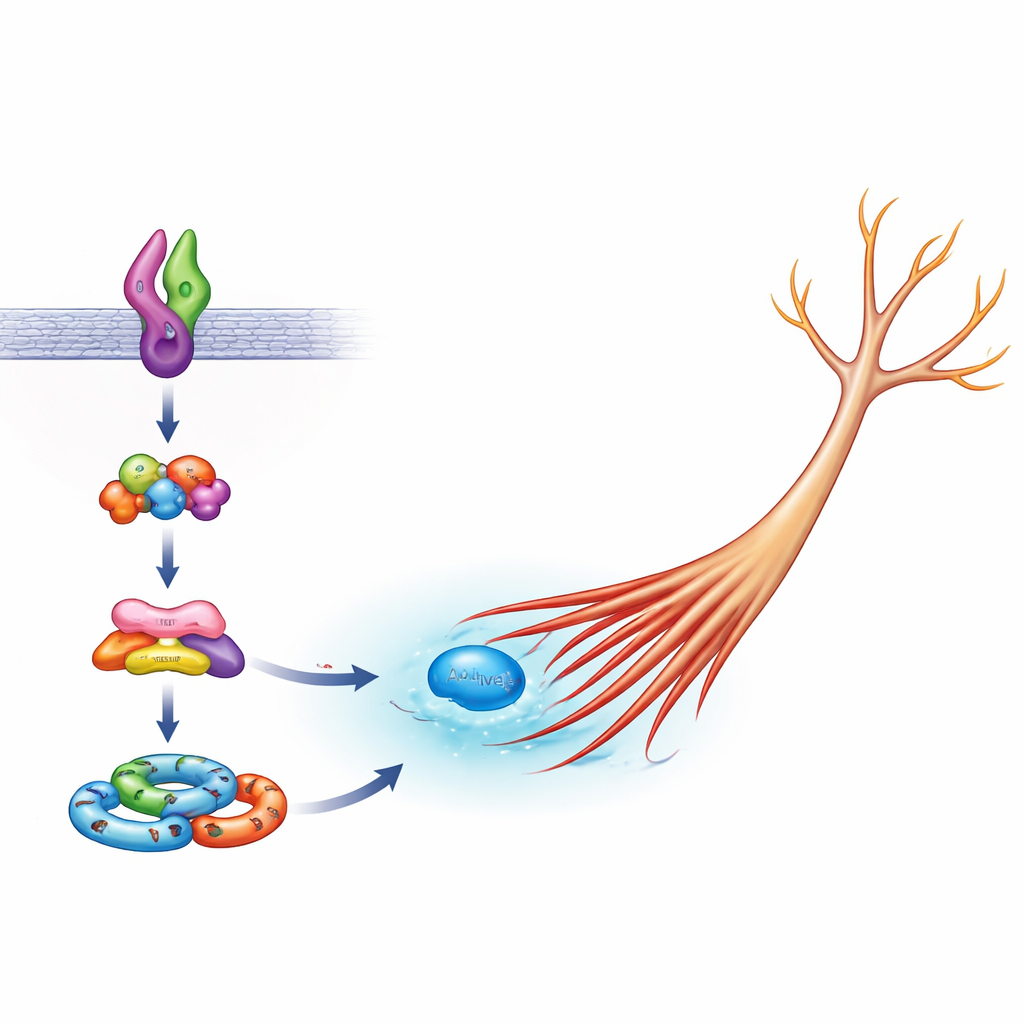
Bu Mikroskobik Zincirin Önemi
Uzman olmayan bir kişi için protein isimlerinin alfabetik karışımı otizm deneyiminden uzak görünebilir. Yine de bu çalışma somut bir köprü sunuyor: Sema5A’daki hassas bir genetik değişikliğin, yardımcı moleküllerden oluşan belirli bir zinciri aşırı etkinleştirerek sinir hücrelerinin dallarını gereğinden fazla uzatmasına ve potansiyel olarak beynin alışılmadık biçimde kablolanmasına nasıl neden olduğunu izliyor. Arf6, FE65 ve ELMO2 sinyal kompleksini bu zincirin kritik bağlantıları olarak belirleyerek çalışma, gelecekteki ilaç hedeflerine işaret ediyor. İlke olarak, bu aşırı etkin yolu nazikçe aşağı çekebilecek ilaçlar bir gün Sema5A ile ilişkili otizme bağlı hücre şekli değişikliklerini düzeltmeye yardımcı olabilir ve nörogelişimsel bozuklukların daha büyük bulmacasına önemli bir katkı sağlayabilir.
Atıf: Takahashi, M., Yako, H., Miyamoto, Y. et al. Autism spectrum disorder-associated Sema5A p.Arg676Cys drives Arf6/FE65 signaling and aberrant cell morphogenesis. Sci Rep 16, 9423 (2026). https://doi.org/10.1038/s41598-026-39722-x
Anahtar kelimeler: otizm spektrum bozukluğu, Sema5A mutasyonu, nöronal morfogenez, Rac1 sinyalleşmesi, Arf6 FE65 yolu