Clear Sky Science · tr
Fare kaynaklı CD25’e özgü rekombinant bir immünotoksin kullanarak insan olmayan primat beyninde belirli nöron tiplerinin hedeflenmesi
Bu beyin çalışması neden önemli
Belirli beyin hücre gruplarının hareket, duygu ve davranışı nasıl kontrol ettiğini anlamak, Parkinson hastalığı ve otizm gibi bozuklukların tedavisi için kilit önemdedir. Ancak beyin, iç içe geçmiş hücrelerden oluşan yoğun bir orman gibidir ve çoğu araç birden çok ağacı aynı anda keser. Bu çalışma, bir maymunun beyninde yalnızca seçilmiş bir nöron türünü minimum yan hasarla yok etmenin bir yolunu sunuyor; bu da belirli devrelerin davranış ve hastalığı nasıl şekillendirdiğine dair çok daha keskin deneylerin önünü açıyor.
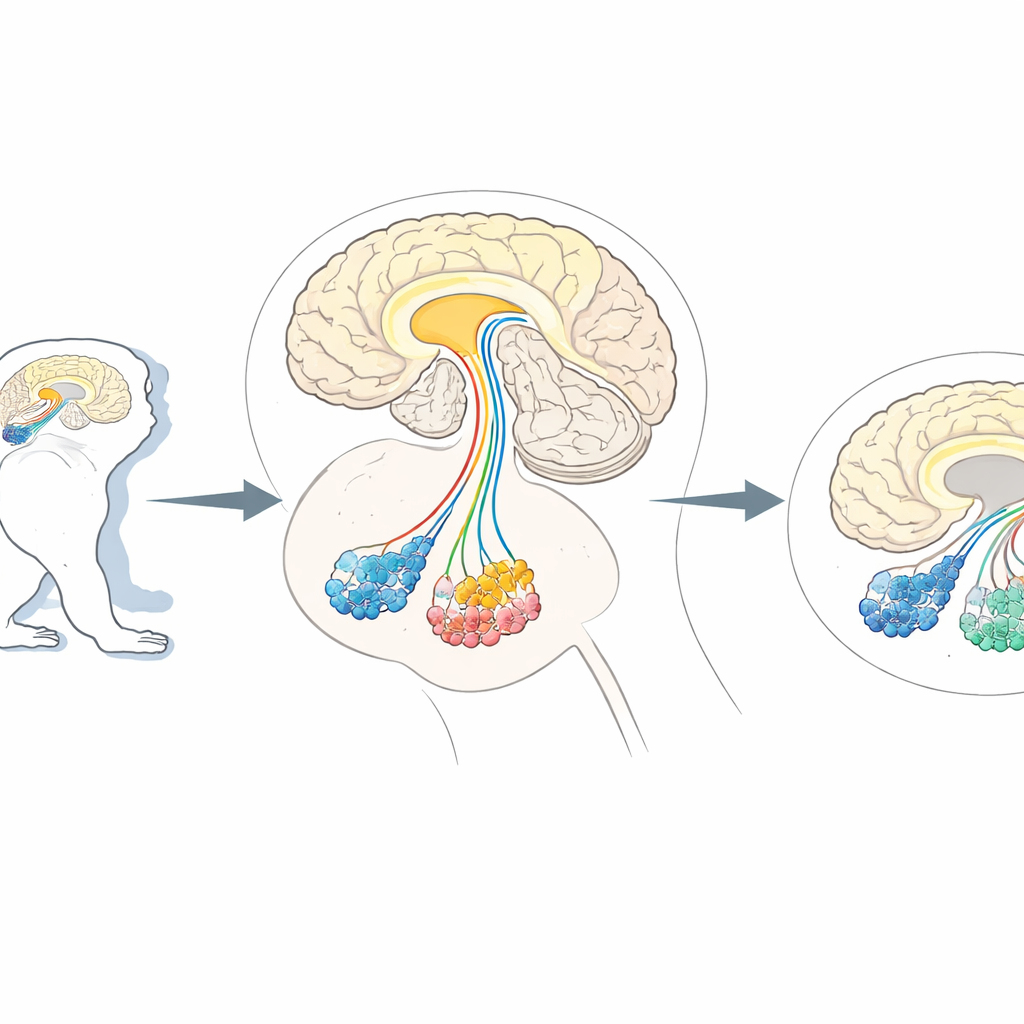
Hassas beyin “hücre budamasına” duyulan ihtiyaç
Araştırmacılar genellikle marmoset ve makak gibi insan olmayan primatlara başvurur, çünkü onların beyinleri bizimkine çok benzer biçimde düzenlenmiştir. Bu hayvanlar, Parkinson’a bağlı hareket sorunlarından sosyal davranışta otizme benzer değişikliklere kadar daha üst düzey beyin işlevlerini etkileyen durumlar için vazgeçilmez modellerdir. Mevcut yöntemler belirli yolları susturabilir veya uyarabilir, ancak bu karmaşık beyinlerde yalnızca tek bir nöron tipini diğerlerine zarar vermeden gerçek anlamda ortadan kaldırmak hâlâ zordur. Farelerdeki önceki çalışmalar bir hile kullandı: seçilen nöronlar, CD25 adlı insan hücre yüzey işaretini sergileyecek şekilde mühendislik ile donatıldı; bu işaret, yalnızca işaretli hücreleri tanıyıp öldüren tasarım bir toksin tarafından hedeflenebiliyordu. Ancak aynı işaret maymunlarda immün hücrelerde ve muhtemelen beyin hücrelerinde doğal olarak bulunduğundan, toksinin maymunlarda yanlış hedeflere saldırma riski vardı.
Daha güvenli bir moleküler neşter tasarlamak
Yazarlar, primatlarda kullanım için uyarlanmış yeni bir moleküler neşter geliştirmeye karar verdi. İnsan CD25 sürümünü hedeflemek yerine, maymunlardaki doğal CD25’e çok daha az benzeyen fare CD25’ine odaklandılar. Önce bir tavşanı fare CD25 proteiniyle immünize ettiler ve bir çip temelli yöntem kullanarak fare CD25’ine güçlü bağlanan ancak insan formuna bağlamayan antikor üreten bireysel tavşan hücrelerini seçtiler. Bunların arasından RMAb-52 adını verdikleri, çok yüksek bağlanma gücüne sahip öne çıkan bir antikoru belirlediler. Ardından bu antikorun anahtar parçalarını Pseudomonas bakterisinden alınan toksik bir parçayla birleştirerek anti-mCD25-PE38 adını verdikleri tek bir mühendislik ürünü “immünotoksin” proteini oluşturdular.
Aleti sınama süreci
Test tüpü deneylerinde yeni immünotoksin, insan CD25’e kıyasla fare CD25’ine çok daha sıkı bağlandı; bu da seçiciliğini doğruladı. Fare CD25’i taşıyacak biçimde mühendislik yapılmış kültürlenmiş hücrelere uygulandığında, toksin çok düşük dozlarda bunların yaşamasını belirgin şekilde azalttı; oysa insan CD25 taşıyan hücreler zarar görmedi. Sonraki adımde ekip canlı marmosetlere geçti. Sinir lifleri boyunca geriye doğru yol alan özel bir viral vektör kullanarak, substantia nigra adlı derin bir beyin bölgesinden striatuma sinyal gönderen ve hareket kontrolü için kritik olan dopamin üreten nöronlara fare CD25 genini ilettiler. Virüsün bu nöronlarda işaretleyiciyi açması için zaman verdikten sonra anti-mCD25-PE38 proteinini doğrudan hedef orta beyin bölgesine enjekte ettiler.
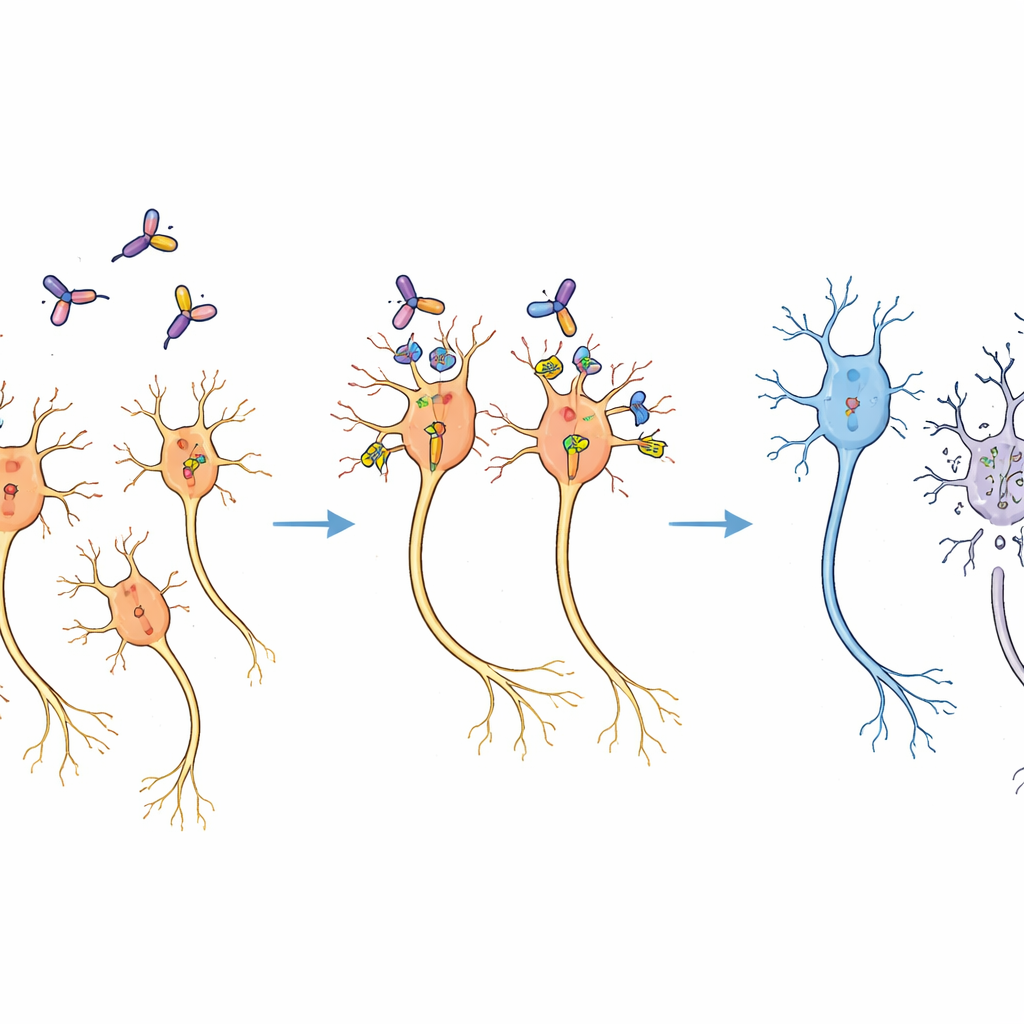
Yaygın hasar olmadan seçici kayıp
Tedaviden iki hafta sonra marmosetlerin beyin kesitleri durumu açıkça gösterdi. İmmünotoksinin verildiği tarafta, dopamin üreten nöron sayısı, dopamin sentezleyen bir enzimle boyama sonucu, tedavi uygulanmamış tarafa göre yaklaşık üçte ikiye düşmüştü. Buna karşın çevreleyen beyin dokusu mikroskop altında normal görünüyordu ve viral vektörün gittiği diğer beyin bölgelerinde belirgin hücre kaybı gözlenmedi. Pilot deneyler zaten rastgele doku yaralanmasını önleyen bir doz aralığı belirlemişti ve seçilen doz bu güvenli pencerenin içinde kaldı. Kaybın deseni, virüs ve toksinin beklenen yayılımıyla uyumluydu; bu da nöronların fare CD25’i sergileyecek şekilde mühendislik yapılmış oldukları için özel olarak ortadan kaldırıldığını, toksinin hücrelere gelişi güzel zarar vermediğini gösteriyordu.
Gelecekteki beyin araştırmaları için anlamı
Bilim dışı okuyucu için ana mesaj, araştırmacıların primat beyinlerinde seçilmiş nöron popülasyonları için son derece seçici bir silme düğmesi geliştirmiş olduklarıdır. Retrograd viral teslim sistemi ile fareye özgü bir immünotoksini birleştirerek, Parkinson hastalığında rol oynayan dopamin devreleri gibi tanımlanmış yolları yakın hücreleri koruyarak ortadan kaldırabilirler. Bu strateji, hayvanın kendi CD25’i ile tehlikeli çapraz reaksiyonlardan kaçınır ve doğal reseptörün mevcut olduğu veya hastalıkta yükseldiği durumlarda özellikle faydalı olacaktır. Uzun vadede bu yaklaşım, beynin kablolamasındaki bireysel rotaların hareket, karar verme ve psikiyatrik belirtilere nasıl katkıda bulunduğunu haritalamaya yardımcı olacak ve geniş ölçekte tüm beyni etkilemek yerine bozuk devreleri ayarlayan hedefe yönelik tedavilere bizi yaklaştıracaktır.
Atıf: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
Anahtar kelimeler: insan olmayan primat nörobilimi, immünotoksin hedefleme, dopamin nöronları, marmoset beyin devreleri, Parkinson hastalığı modelleri