Clear Sky Science · tr
Sudanlı Escherichia coli suşlarındaki kanonik ve yeni dirençle ilişkili missense mutasyonların yapısal modellemesi ve docking analizi
Günlük sağlık için neden önemli
Antibiyotiğe dirençli enfeksiyonlar artık nadir tıbbi meraklar değil; idrar yolu enfeksiyonları, cerrahi girişimler ve yoğun bakım gibi rutin tedavileri giderek daha fazla tehdit ediyor. Bu çalışma, Sudan’dan izole edilen Escherichia coli örneklerini yakından inceleyerek çok özel bir soruyu ele alıyor: bakteriyel proteinlerdeki küçük genetik değişiklikler, yaygın antibiyotiklerin etkinliğini nasıl yeniden şekillendiriyor? Maliyeti yüksek laboratuvar deneyleri yerine bilgisayar tabanlı yapısal modelleme kullanarak, yazarlar standart testlerin ve küresel veri tabanlarının gözden kaçırabileceği gizli direnç paternlerini ortaya çıkarıyor—özellikle direncin en hızlı arttığı kısıtlı kaynaklı bölgelerde. 
Bakterinin araç kutusunun içini görmek
Araştırmacılar, tek baz değişimiyle bir proteinin yapı taşlarından birinin değiştirildiği "missense" mutasyonlara odaklandı. Sudan’da toplanan 55 E. coli izolâtının tüm genom dizilerini analiz ederek, fluoroquinolonlar, makrolidler ve rifampisin gibi önemli antibiyotik sınıflarının doğrudan hedef aldığı bakteriyel proteinlere odaklandılar. Bu hedefler arasında DNA’yı büken enzimler (giyraz ve topoisomeraz IV), protein sentezleyen ribozom ve RNA polimeraz yer alıyor. Bu proteinlerde tespit edilen 71 mutasyondan 19’u, birden çok tahmin aracı tarafından muhtemel fonksiyonel hasar açısından işaretlendi ve çarpıcı bir şekilde bunların çoğu küresel direnç veri tabanlarında henüz kayıtlı olmayan yeni varyasyonlar olarak göründü.
Tanıdık hedeflerde yeni problem noktaları
En önemli değişikliklerden bazıları, yeni sentezlenen proteinlerin ribozomdan çıkış tünelini oluşturmaya yardımcı olan L22 adlı bir ribozomal proteinde kümelendi. Bu bölge aynı zamanda eritromisin gibi makrolid antibiyotiklerin bağlanma bölgesidir. Çalışma, çoğu tek bir suş içinde yoğunlaşan ve tünelin tam boyunca ile ribozomal RNA ile temas noktalarında bulunan daha önce raporlanmamış yoğun L22 mutasyonları tespit etti. Hesaplamalı analizler, bu değişikliklerden birkaçının yerel yapıyı destabilize ettiğini veya daha esnek hale getirdiğini; bunun da makrolid moleküllerinin tünelde daha gevşek oturmasına yol açabileceğini öne sürdü. Aynı zamanda, ParC ve ParE gibi DNA işlem enzimlerinde ve RNA polimerazda daha tanıdık "kanonik" direnç mutasyonları da görüldü; bu, Sudanlı suşların bazı küresel direnç işaretlerini paylaştığını, ancak kendi yerel farklılıklarını da barındırdığını doğruluyor.
Şekil değişiklikleri antibiyotik tutunmasını nasıl zayıflatıyor
Ekip dizilim listelerinin ötesine geçerek bu mutasyonların antibiyotikler ile hedefleri arasındaki üç boyutlu uyumu nasıl değiştirebileceğini sordu. Moleküler docking simülasyonları kullanarak farklı ilaçların normal ve mutasyona uğramış proteinlere nasıl bağlandığını karşılaştırdılar. Topoisomeraz IV proteini ParC için, ilaç temas bölgesine yakın anahtar mutasyonlar, fluoroquinolon trovafloksasin’in öngörülen bağlanmasını önemli ölçüde zayıflattı; bu, enzim–DNA–ilaç kavşağında daha gevşek bir tutuşu yansıtıyor. İlgili ParE proteininde mutasyonlar novobiosinin bağlanmasını ölçüde azalttı. Buna karşılık, giyraz proteini GyrA’daki yeni bir mutasyon enzimin yapısını destabilize etmiş görünmesine rağmen, fluoroquinolon moksifloksasin’in ne kadar sıkı bağlandığını belirgin şekilde değiştirmedi; bu da direncin bazen ilacı doğrudan dışlamak yerine enzimin performansını ince şekilde bozarak ortaya çıkabileceğine işaret ediyor. 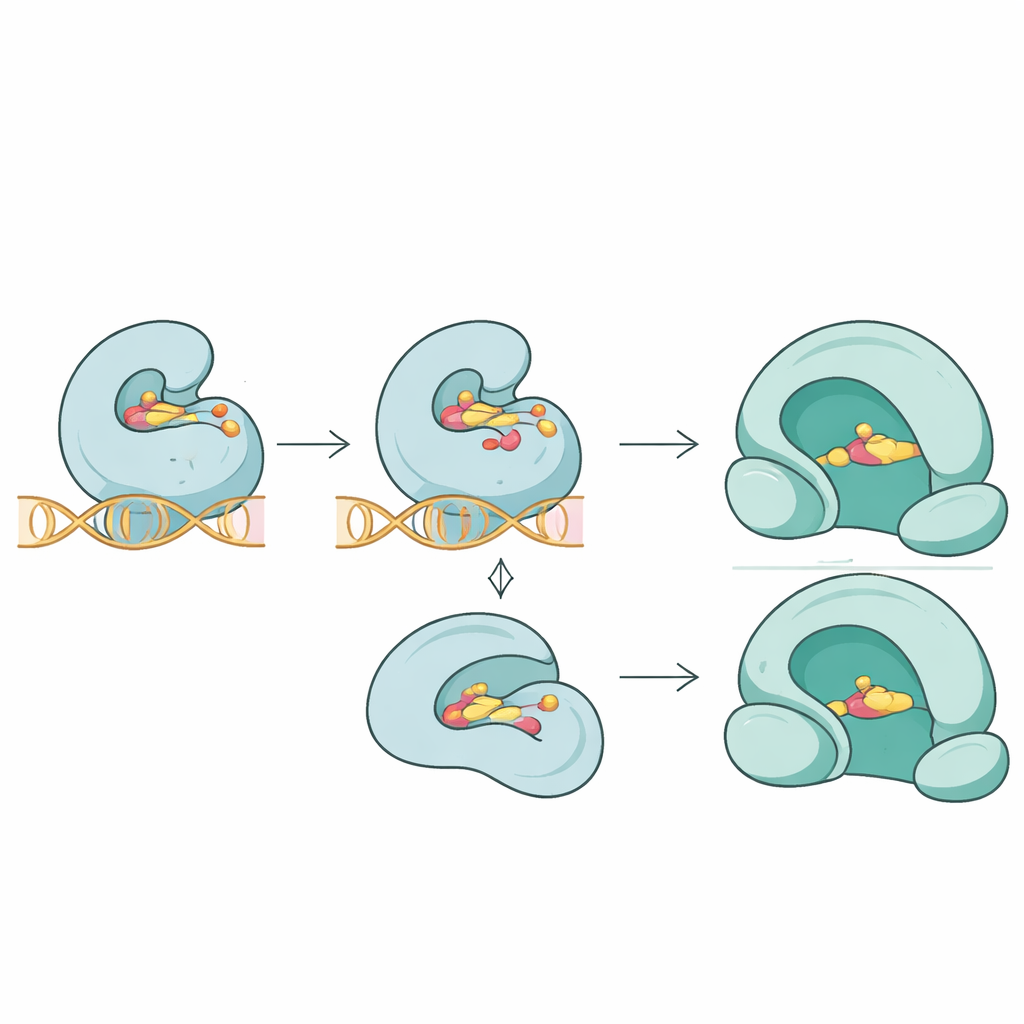
Farklı ilaçlar üzerinde karışık etkiler
Tüm mutasyonlar aynı etkiye sahip değildi. RNA polimeraz proteini RpoB’daki klasik rifampisin direnç değişiklikleri, yakınlardaki farklı bir bölgeyi hedefleyen daha yeni, yapısal olarak farklı bir inhibitörün bağlanmasını fazla bozmadı; bu, gelecekteki ilaçların mevcut direnç paternlerini atlayacak şekilde tasarlanabileceğini düşündürüyor. Ribozomal protein L22 için eritromisinle yapılan docking çalışmaları, sonuçların bir yamalı resmini ortaya koydu: bazı mutasyonlar bağlanmayı zayıflattı, bazıları az bir etki yaptı ve biri öngörülen uyumu hafifçe iyileştirdi. Bu bulgular, direncin nadiren tamamen her şey veya hiçbir şey olduğunu vurguluyor; bunun yerine her mutasyon protein stabilitesini, esnekliğini ve ilaç bağlanmasını farklı yönlere doğru itiyor ve tedavi üzerindeki nihai etki bu değişikliklerin canlı bir bakteri hücresi içinde nasıl bir araya geldiğine bağlı.
Hastalar ve sürveyans için anlamı
Halk açısından temel mesaj şudur: Sudan gibi yerlerdeki bakteriler, hem iyi bilinen hem de daha az bilinen yollarla dirence doğru evriliyor. İyi bilinen yollar uluslararası programlarca zaten izlenen klasik mutasyonları içerirken, bu çalışma birçok ek yerel olarak zenginleşmiş mutasyonun da antibiyotikleri daha ince yollarla zayıflatabileceğini gösteriyor. Bu değişiklikleri ayrıntılı protein yapıları üzerine haritalayarak yazarlar, laboratuvarda test edilmesi ve bölgesel tanı panellerinde dikkate alınması gereken kısa bir mutasyon listesi sunuyor. Pratik anlamda, akıllı bilgisayar modellemesinin sınırlı laboratuvar kapasitesine sahip ülkelere ortaya çıkan direnci daha iyi izlemekte yardımcı olabileceğini; bunun da daha güvenilir tedavi seçimlerini destekleyerek bakteriyel evrim karşısında bir adım önde olacak ilaç tasarımlarını teşvik edebileceğini savunuyor.
Atıf: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
Anahtar kelimeler: antimikrobiyal direnç, Escherichia coli, missense mutasyonlar, yapısal biyoinformatik, Sudan