Clear Sky Science · tr
Antijen-spesifik T hücresi aktivasyonu için CD32a sinyalleştirmeli fagositozu kullanan THP-1-CAR monositlerinin optimizasyonu
Bağışıklık Sistemine Yeni Hünerler Öğretmek
Modern hücre tedavileri zaten bağışıklık hücrelerini kanseri avlamaya yeniden programlıyor, ancak çoğu T hücrelerine dayanıyor; oysa T hücreleri katı tümörlerin zorlu ortamında zorlanabiliyor. Bu çalışma bunun yerine başka güçlü bir savunmacıya—vücudun profesyonel “yiyicileri” olan makrofajlara—yöneliyor ve onları yalnızca zararlı hücreleri veya virüsleri daha verimli yemeyecek şekilde değil, aynı zamanda daha kalıcı, hedefe yönelik bir saldırı için T hücrelerini çağıracak şekilde nasıl yeniden kablolayabileceğimizi sorguluyor. Çalışma, hem COVID‑19 gibi enfeksiyonlara hem de zor tedavi edilen solid tümörlere uygulanabilecek daha iyi kimerik antijen reseptörü (CAR) makrofajları oluşturmak için tasarım kurallarını ortaya koyuyor.
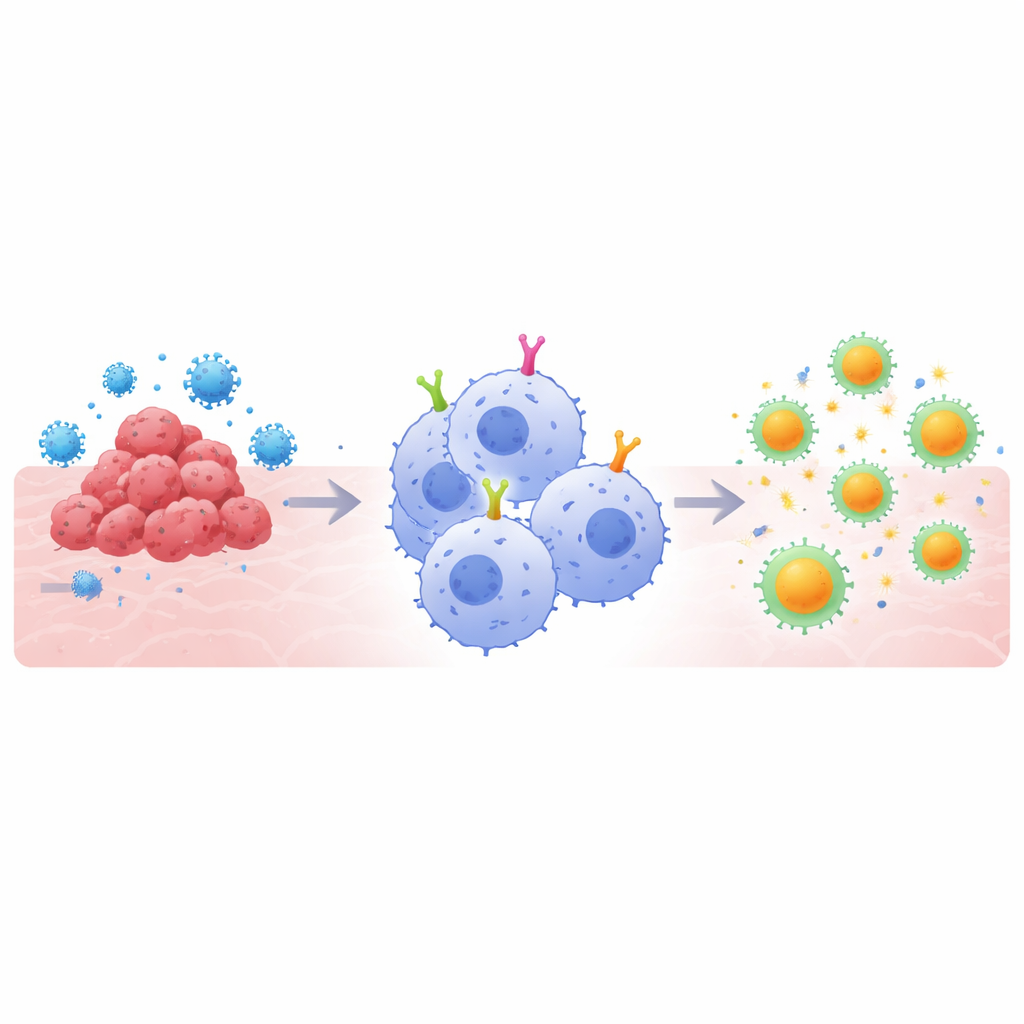
Neden Süper-Yiyici Hücreler Önemli?
CAR tabanlı terapiler, bağışıklık hücrelerini seçilmiş bir hedefi—örneğin bir tümör proteini veya viral bir spike—tanıyacak şekilde özel yüzey reseptörleriyle donatarak çalışır. T hücresi versiyonları belirli kanser tedavilerinde devrim yarattı, ancak solid tümörler ve bazı enfeksiyonlar karşısında engellerle karşılaşıyor. Makrofajlar farklı bir açı sunuyor: doğal olarak tehditleri yutar ve bunları T hücrelerine gösterilebilecek parçalara ayırır; böylece“doğuştan” gelen ve “edinsel” bağışıklık kolları arasında köprü kurarlar. Bununla birlikte, çoğu CAR tasarımı başlangıçta T hücreleri için geliştirildi, makrofajlar için değil. Yazarlar, makrofajların güçlü yönlerinden tam olarak yararlanmak için CAR’ların iç sinyal parçalarının—hedef bağlandığında hücreye ne yapması gerektiğini söyleyen segmentlerin—özellikle bu yiyici hücrelere uyarlanması gerektiğini düşündüler.
En İyi İç Kablolamayı Bulmak
Araştırma ekibi, makrofaja dönüştürülebilen bir insan monosit hücre hattı (THP‑1) içine verilen CAR’ların içinde birkaç farklı iç sinyal bölgesini sistematik olarak karşılaştırdı. Fagositoz ve inflamasyonu normalde yönlendiren reseptörlerden alınan CD3ζ (klasik T hücresi modülü), CD32a (antikorla kaplı hedeflere bağlanan bir reseptör), CR3 bileşenleri CD11b ve CD18 (anahtar kompleman reseptörleri) ve mikrobiyal tehlike sensörü TLR4 gibi alanlara odaklandılar. SARS‑CoV‑2 spike proteini ile kaplı boncuklar ve psödo virüsler kullanarak, her CAR tasarımının hücrelerin hedefleri yutma, iltihaplı moleküller üretme ve ardından virüsü daha önce görmüş insan CD8 T hücrelerini aktive etme becerisini ölçtüler. Ardından en umut verici tasarımları, aynı kuralların kanser ortamında da geçerli olup olmadığını görmek için birçok solid tümörde aşırı üretilen bir protein olan mezotelin hedefleyen CAR’lara aktardılar.
Daha İyi Yiyiciler ve Sinyal Güçlendiriciler İnşa Etmek
Açık bir desen ortaya çıktı: CD32a tabanlı CAR’lar, geleneksel CD3ζ alanını kullananlara kıyasla daha güçlü ve daha hızlı fagositozu istikrarlı şekilde yönlendirdi; oysa CD3ζ daha fazla alışılmış aktivasyon motifine sahipti. Başka bir deyişle, sinyal ile makrofaj mekanizması arasındaki “uyum”, yalnızca sinyal gücünden daha önemliydi. CD32a üzerine CR3 türevi parçalar (CD11b veya CD18) eklemek çoğu durumda yeme kapasitesini daha fazla artırmadı, ancak TNF‑α ve IL‑1β gibi önemli inflamatuar sitokinlerin düzeylerini yükseltti. TLR4 içeren kombinasyonlar inflamatuar sinyalleri ve T hücresi uyarıcı kapasite ile ilişkili yüzey belirteci CD86’yı daha da artırdı; bununla birlikte bu durumun bedeli olarak hücre yüzeyindeki CAR düzeylerinde azalma ve bir ölçüde azalmış fagositoz gözlendi.
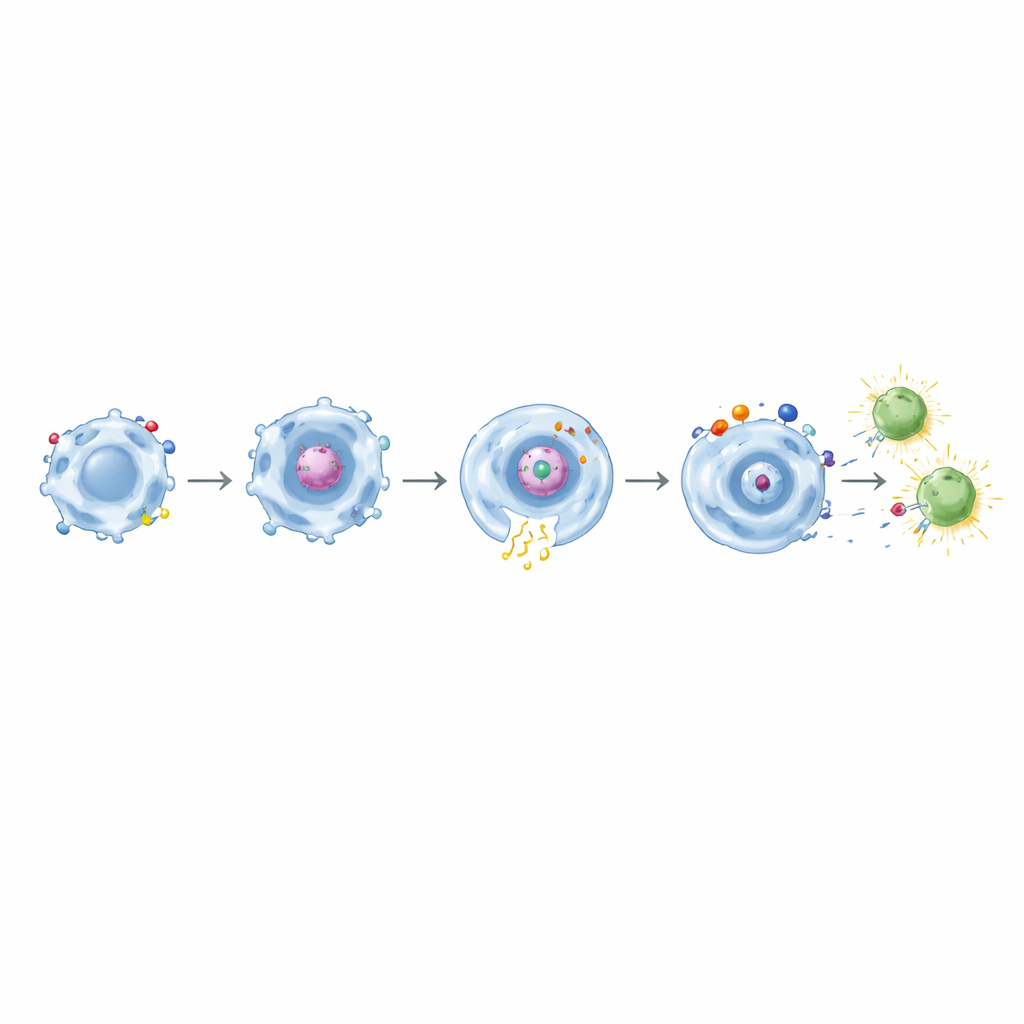
Yemekten T Hücresine Öğretmeye
Özellikle, CD32a tabanlı CAR taşıyan makrofajlar spike proteinini yuttuktan sonra daha önce COVID‑19 aşısı olmuş kişilerden alınan hafıza CD8 T hücrelerini aktive edebildiler. Bu T hücreleri erken aktivasyon belirteçlerini açtı ve interferon‑γ ile TNF‑α gibi efektör moleküller üretti. Etki, CD32a’yı CD11b, CD18 veya TLR4 ile eşleştiren çift bölmeli CAR’larla daha da güçlendi. Mezotelin hedefleyen benzer tasarımlar mühendislik ürünü tümör hücrelerine karşı test edildiğinde, yine hedefe bağımlı hassas fagositoz ile artmış inflamatuar sinyalleşmeyi bir arada gösterdiler. Bunların arasında CD32a+TLR4 kombinasyonu güçlü bir “doku alarmı” olarak öne çıktı; sitokin salınımını ve CD86’yı en etkili şekilde artırırken hedefe özgü tümör yeme özelliğini korudu.
Gelecek Tedaviler İçin Bunun Anlamı Ne Olabilir?
Bir gözlemci için bu çalışma, makrofaj mühendisliğinin tek tip bir problem olmadığını gösteriyor. İç sinyal modüllerini değiştirip birleştirerek, bilim insanları ya hastalıklı hücrelerin verimli temizliğine odaklanan ya da tümörün baskılayıcı ortamını yeniden şekillendirip T hücrelerini işe çağıran bağışıklık güçlendiricileri gibi davranan hücreler şekillendirebilir. CD32a‑tabanlı CAR’lar, makrofajlarda geleneksel T hücresi modüllerinden daha iyi performans göstererek hem viral hem de tümör hedeflerinde çalışan sağlam bir temel olarak ortaya çıktı. Bu sonuçlar laboratuvar modellerinden elde edilmiştir ve primer insan hücrelerinde ile hayvan çalışmalarında doğrulanmaları gerekecektir; ancak hızlı fagositozu kesin T hücre aktivasyonu ile birleştirerek solid tümörler ve kalıcı enfeksiyonlarla daha iyi mücadele edebilecek yeni nesil CAR makrofaj terapileri için bir yol haritası sağlarlar.
Atıf: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
Anahtar kelimeler: CAR makrofajlar, CD32a sinyalleştirmesi, fagositoz, solid tümör immünoterapisi, T hücresi aktivasyonu