Clear Sky Science · tr
Radyobiyolojik simülasyonlar için arafaz hücre çekirdeğinin bir polimer fiziği modeli
DNA Evimizin Şekli Neden Önemli
Radyasyon tıpta iki ucu keskin bir kılıç gibidir: kanser hücrelerini öldürebilir, ancak sağlıklı dokuyu da zarar görebilir. Hem risklerin hem de faydaların merkezinde, hücre çekirdeği içinde sıkıca paketlenmiş DNA bulunur. Bu makale, o nükleer “DNA şehrinin” ayrıntılı, fizik esinli 3B modelinin, radyasyonun kromozomları nasıl kırıp hatalı birleştirebileceğini tahmin etmeye nasıl yardımcı olabileceğini gösteriyor; bu da kanser tedavisini iyileştirme ve uzay radyasyonu risk tahminlerini geliştirme potansiyeli taşıyor.
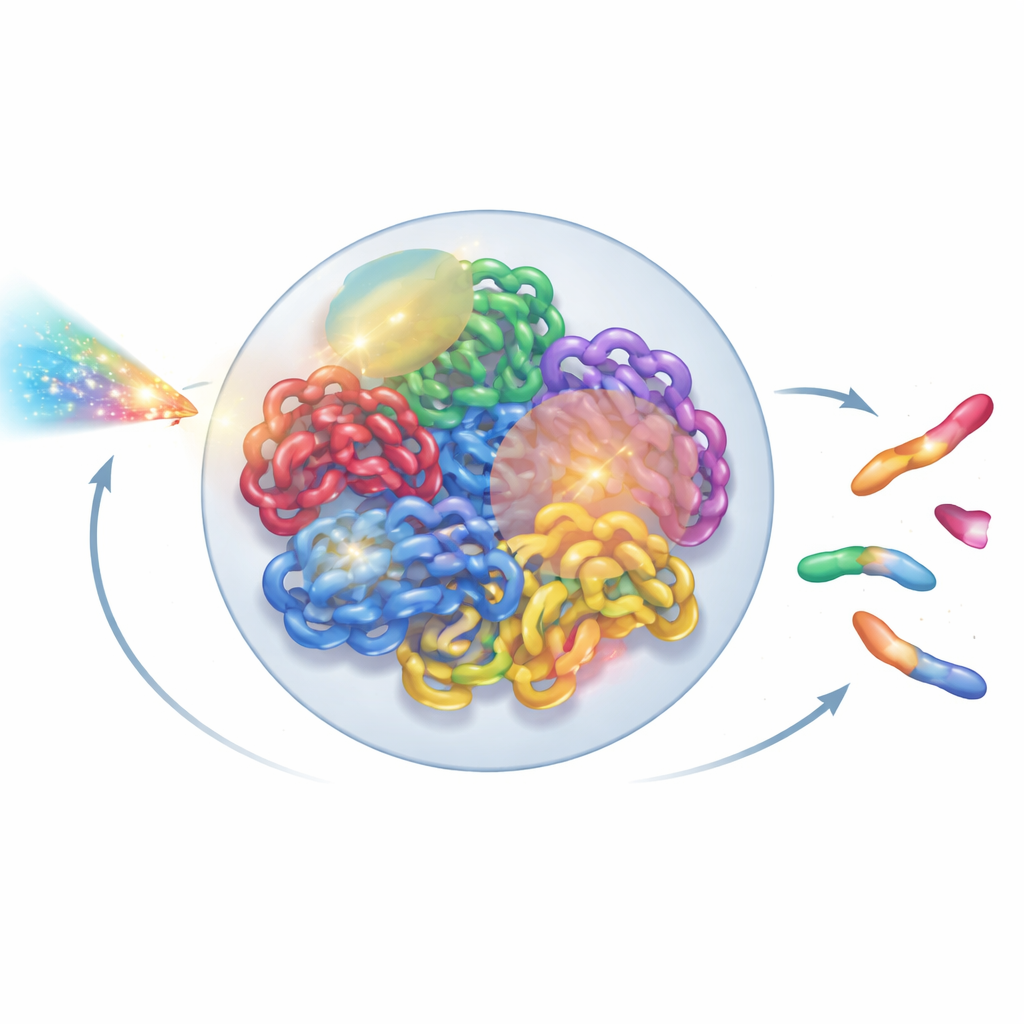
Genomu Canlı Bir Yapı Olarak Görmek
Her insan hücresinin içinde iki metre uzunluğundaki DNA, sadece birkaç mikrometre çapındaki küçük bir çekirdeğe katlanmıştır. Bu katlanma rastgele değildir: her kromozom kendi bölgesini işgal etme eğilimindedir; bu bölgeler mahallelere ve döngüsel alanlara ayrılır. Süper çözünürlüklü mikroskopi ve Hi-C temas haritaları gibi yeni deneysel araçlar, bu karmaşık 3B düzeni olağanüstü ayrıntıyla ortaya koydu. Yine de çoğu radyasyon modeli hâlâ DNA’yı basitleştirilmiş bir çizgi düğümü veya idealize döngüler olarak ele alıyor ve bu daha yüksek düzey organizasyonu göz ardı ediyor. Yazarlar, gerçek kromatin mimarisi hakkında biyologların öğrendiklerine saygı gösteren, ancak sıradan laboratuvar bilgisayarlarında çalıştırılabilecek kadar hızlı olacak bir tüm-çekirdek modeli oluşturmayı hedeflediler.
Polimer Fiziği ile Sanal Bir Çekirdek Kurmak
Ekip, kromozomları esnek zincirler olarak modelleyerek, plastikler ve yumuşak maddeleri anlamak için kullanılan aynı polimer fiziği fikirlerinden yararlandı. Büyük hesaplama maliyetini dizginlemek için problemi üç gevşeme aşamasına böldüler. Önce kromatin alanları adı verilen büyük yapı bloklarını çekirdek boyunca yerleştirip bunların birbirlerini itmesine, uzunlamasına gerilmelerine ve daha geniş altbölgelerde kümelenmelerine izin verdiler. İkinci olarak, her alan içinde daha ince kromatin liflerini, bağlanma proteinleriyle bir arada tutulan döngüsel bölgeler dahil olmak üzere yerleştirmek için yakın çekime girdiler. Üçüncü olarak, tüm liflerin nükleer sınır içinde serbestçe etkileşmesine izin vererek gerçekçi bir nihai konfigürasyona yaklaştılar. Süreci bu şekilde bölerek ve hiyerarşik arama ile paralel hesaplama hileleri ekleyerek, çalışma süresini uygulanamaz dört aydan 64 çekirdekli bir iş istasyonunda her sanal çekirdek için yaklaşık üç saate düşürdüler.
Radyasyon İzlerinden DNA Kopmalarına ve Onarımlara
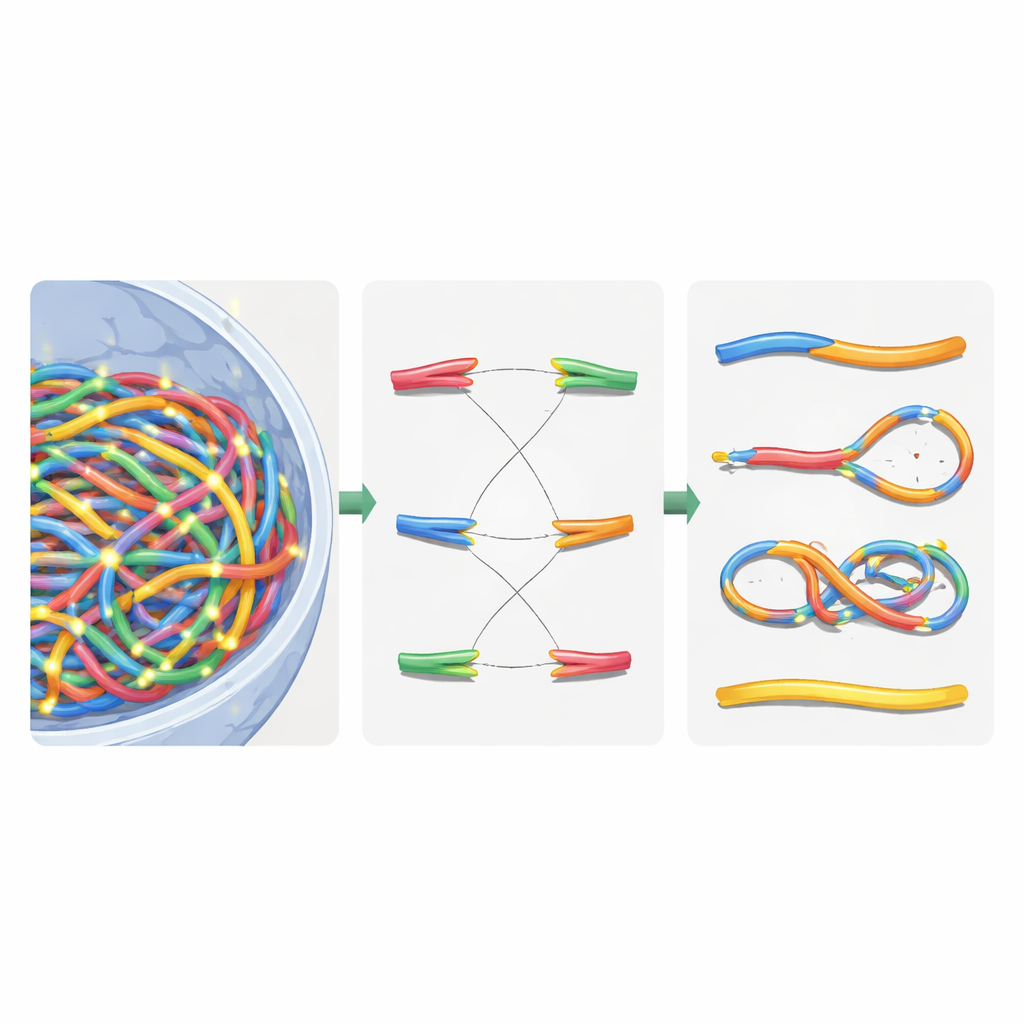
Sanal çekirdek kurulduktan sonra, yazarlar Geant4-DNA simülasyonlarıyla üretilen ayrıntılı radyasyon izlerini üst üste koydular. Her iyonlaşma olayı için hangi kromatin alanının, hangi fiber segmentinin ve nihayet hangi nükleotidin en yakın olduğunu bulmak için hiyerarşik bir arama kullandılar; tüm on milyar nükleotid konumunu bellekte tutmaya hiç gerek kalmadı. Bunun yerine, yeniden kullanılabilir bir kromatin şablonu tuttular ve sahada koordinat dönüşümleri uyguladılar. DNA omurgasındaki iyonlaşmalar şerit kopmaları olarak ele alındı ve zıt şeritlerdeki yakın kopmalar çift şeritli kopmalar oldu. Hücrenin onarım mekanizmasını taklit etmek için yazarlar mesafeye dayalı yeniden birleştirme kuralı getirdiler: birbirine yakın duran serbest DNA uçlarının yeniden birleşme olasılığı daha yüksekti. Yeniden birleştirme kararları, tüm uçlar ya eşleştirilene ya da onarılmadan bırakılana kadar adım adım verildi ve doğru onarımlar ile hatalı birleştirmeler yeniden oluşturuldu.
Kırık Kromozomları Ağ Mantığıyla Sıralama
Bu sanal onarımdan sonra çekirdek, yeniden birleştirilmiş kromozomlar ve geride kalan parçaların karışımını içeriyordu. Ne olduğunu sınıflandırmak için yazarlar onarılan genomu yönsüz bir grafiğe çevirdiler: kromozom segmentleri kenarlara, uçları ve kırık noktaları ise düğümlere dönüştü. Standart bir bağlı bileşen algoritması kullanarak, her yeni kromozom benzeri nesneyi otomatik olarak kurtarabiliyor ve sentromer (hücre bölünmesi için bağlantı noktaları) ve telomer (doğal uçlar) sayısı gibi anahtar özellikleri sayabiliyorlardı. Buradan ikisentromerliler (iki sentromeri olan kromozomlar), halkalar ve delesyonlar belirlendi. Ardından simülasyonlarını gama ışınları ve alfa parçacıklarına maruz bırakılmış insan deri hücrelerindeki klasik deneylerle karşılaştırdılar ve toplam kromozom anormalliklerinin ölçülen değerlere yaklaşık %20 içinde yeniden üretildiğini buldular; bu, önceki modellere göre önemli bir iyileşme gösteriyor.
Bu Hastalar ve Astronotlar İçin Ne Anlama Geliyor
Basitçe söylemek gerekirse, bu çalışma DNA’nın çekirdek içindeki “nerede” oturduğunun ve “nasıl” katlandığının, radyasyon hasarının tehlikeli kromozom değişikliklerine nasıl eklendiğini güçlü biçimde etkilediğini gösteriyor. Gerçekçi 3B genom mimarisini, verimli fizik tabanlı simülasyonu ve kırık kromozomların grafik tabanlı çıktısını birleştirerek, yazarlar yapısal biyoloji ile radyobiyoloji arasında güçlü bir köprü sunuyorlar. Detaylı onarım zamanlamasının eklenmesi ve tüm genom dizileme verilerinin kullanılması gibi gelecekteki iyileştirmelerin, bu yaklaşımı kanser tedavisinde kullanılan veya derin uzayda karşılaşılan yüksek enerjili parçacıkların biyolojik etkisini tahmin etmede daha da iyi hale getirebileceğini savunuyorlar. Sonuç olarak, hücrelerimizin içindeki DNA evinin daha iyi modelleri, daha güvenli ve daha etkili radyasyon tedavileri uyarlamaya ve uzun vadeli radyasyon risklerinin anlaşılmasını keskinleştirmeye yardımcı olabilir.
Atıf: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
Anahtar kelimeler: radyasyon kaynaklı DNA hasarı, kromatinin 3B mimarisi, kromozom anormallikleri, polimer fiziği modellemesi, parçacık terapisi