Clear Sky Science · tr
Yoğun bakım ünitesindeki sepsisli hastaların erken dönemde periferik kan mononükleer hücre mitokondriyal işlevinin ilerleyişi
Hücrelerimizin enerji santrallerinin ölümcül enfeksiyonda neden önemli olduğu
Sepsis, enfeksiyona karşı yaşamı tehdit eden bir yanıt olup her yıl yüzbinlerce insanı yoğun bakım ünitelerine (YBÜ) götürür ve dünyada milyonlarca kişinin ölümüne yol açar. Hekimler sepsis sırasında birçok organın işlevinin bozulduğunu bilir, ancak bağışıklık hücrelerimizdeki küçük “enerji santralleri”—mitokondrilerin—örtük rolünü belirlemek daha zordu. Bu çalışma, sepsisli YBÜ hastalarını kritik bakımın ilk haftası boyunca izleyerek, kanın önemli bağışıklık hücrelerinin enerji üretiminin zaman içinde nasıl değiştiğini ve bu değişikliklerin hayatta kalma ile ilişkisinin olup olmadığını inceledi.
Sepsis sırasında kandaki duruma bakmak
Araştırmacılar, iltihaplanmayı başlatan ve mikroplarla savaşan önemli bir beyaz kan hücresi grubu olan periferik kan mononükleer hücrelere (PBMC) odaklandı. Bu hücreler vücutta dolaştığı ve kolay örneklenebildiği için bağışıklık sisteminin durumuna dair kullanışlı bir pencere sunar. Ekip, Hollanda’daki bir YBÜ’de sepsis veya septik şok geçiren 40 yetişkin hastayı, sepsisi olmayan ve metabolik olarak diğer açılardan sağlıklı olacak şekilde yaş ve cinsiyete göre özenle eşleştirilmiş 30 hastane kontrolü ile karşılaştırdı. Sepsisli hastalardan kan üç kez alındı—YBÜ’ye kabulün ilk iki günü içinde ve tekrar yaklaşık 3–4. günler ile 5–6. günlerde—kontrollerden ise tek örnek alındı. Her örnekten araştırmacılar bağışıklık hücrelerini izole etti, standart bir besin çözeltisine koydu ve mitokondrilerin farklı koşullar altında oksijeni ne kadar hızlı tükettiğini ölçtü; bu, hücrelerin enerji santrallerinin ne kadar çalıştığının doğrudan bir göstergesiydi. 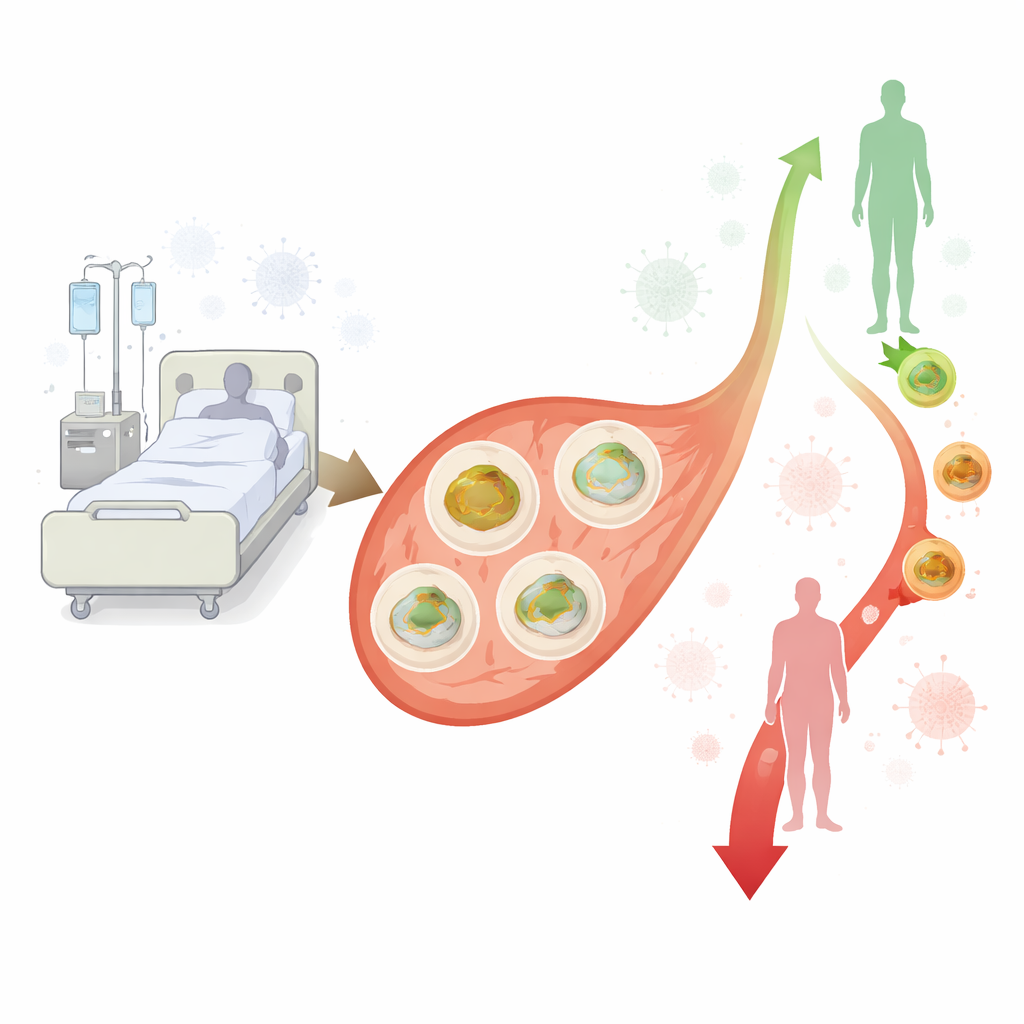
Yüksek viteste çalışan bağışıklık hücresi motorları
Sepsisin hücresel enerji üretimini basitçe “kapattığı” fikrinin aksine, ekip bağışıklık hücrelerindeki mitokondriyal aktivitenin kontrollerdekinden tutarlı şekilde daha yüksek olduğunu buldu. Tüm zaman noktalarında bazal solunum (dinlenme halindeki temel oksijen kullanımı) artmıştı. Yararlı enerji üretimiyle ilişkili bileşenler—ATP ile bağlantılı solunum—ve mitokondrilerin maksimum solunum kapasitesi de özellikle ilk haftanın ilerleyen günlerinde eğilim olarak daha yüksekti. Yakıt yakılıp enerji üretilmeden gerçekleşen bir tür “boşa solunum” olan proton sızıntısı bile artmıştı. Birlikte değerlendirildiğinde, bu bulgular en azından dolaşımdaki bağışıklık hücrelerinde enerji mekanizmasının erken sepsiste durmak yerine gaz verildiğini; muhtemelen aktifleşmiş bağışıklık yanıtının yoğun taleplerini yansıttığını düşündürüyor.
Daha yüksek aktivite ile uyumlu gen sinyalleri
Bu daha yüksek solunum hızının moleküler düzeyde desteklenip desteklenmediğini görmek için araştırmacılar mitokondriyal mekanizmanın kritik parçalarını kodlayan birkaç genin aktivitesini inceledi. 10 sepsisli hasta ve 10 eşleştirilmiş kontrolde bir alt küme olarak oksidatif fosforilasyon komplekslerinin parçalarını—yakıtı ATP’ye çeviren protein topluluklarını—kodlayan gen ekspresyonunu ölçtüler. Özellikle iki gen, SDHB (kompleks II’nin bir parçası) ve ATP5F1A (kompleks V, ATP sentazın bir parçası), sepsisli hastalarda birden fazla zamanda anlamlı şekilde daha aktifti; kontrole göre yaklaşık %40–50 artış gösterdiler. Bu moleküler “hızlanma” çekirdek mekanizmada görülen fonksiyonel verilerle iyi örtüşüyor ve bağışıklık hücresi mitokondrilerinin sepsiste parçalanmak yerine daha fazla çalışmaya zorlandığı fikrini güçlendiriyor. 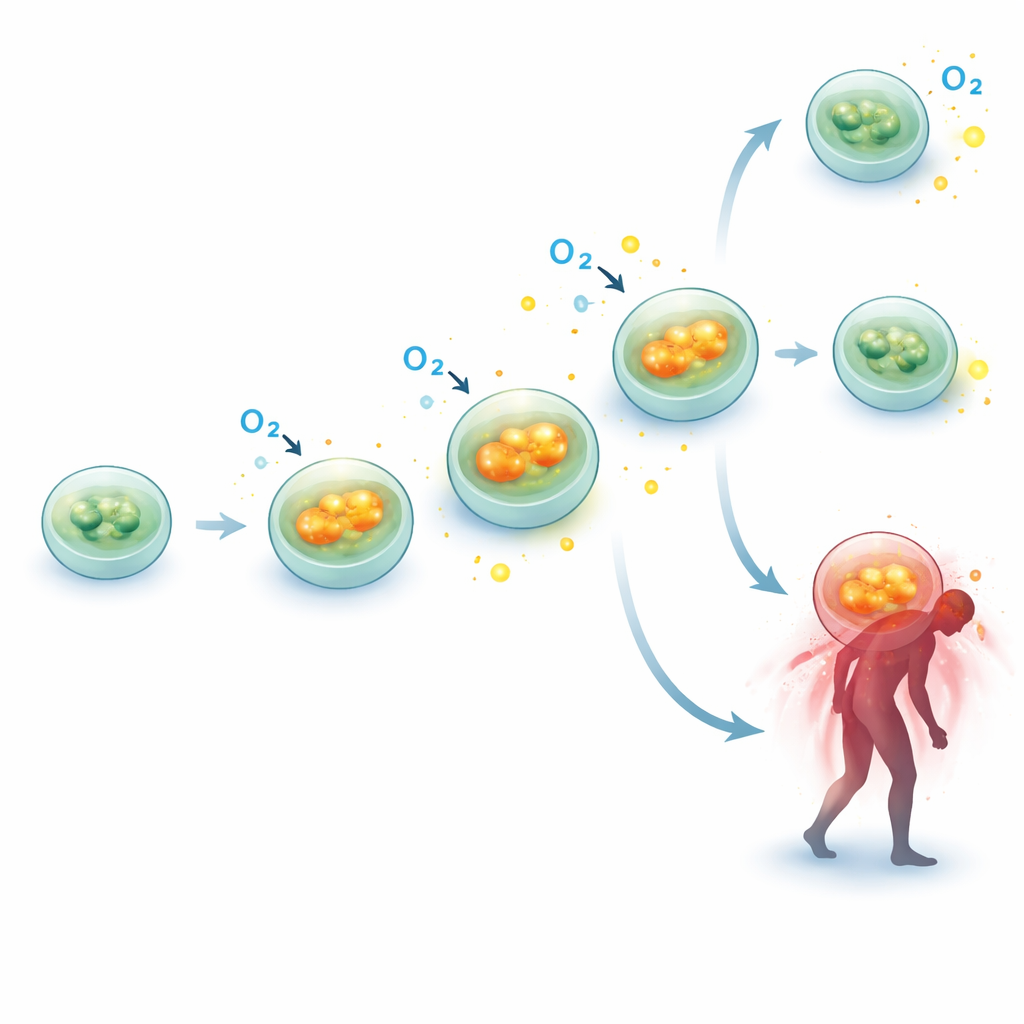
Enerji değişiklikleri yaşam ve ölümü nasıl etkiliyor
En çarpıcı bulgu bu mitokondriyal değişikliklerin sonuçlarla nasıl ilişkili olduğuydu. Ekip, üç aylık dönemde sağ kalanlarla hayatını kaybedenleri karşılaştırdığında, ilk ölçümde mitokondriyal işlevde büyük farklılıklar görmedi. Ancak ilk haftadaki değişim yönü farklı bir hikâye anlattı. Sağ kalanlarda bağışıklık hücrelerindeki mitokondriyal solunum hafifçe azalma eğilimindeydi veya stabil kaldı. Daha sonra ölen hastalarda ise aynı ölçümler—bazal, ATP‑bağlı, maksimum solunum ve yedek kapasite—hafta ilerledikçe daha da arttı. İstatistiksel analiz, ilk ve son ölçümler arasındaki bazal solunumdaki daha güçlü artışın, hastalığın şiddet skorları hesaba katılsa bile üç ay içinde ölüm riskinin daha yüksek olmasıyla ilişkili olduğunu öne sürdü. Ölüm sayısının sınırlı olması nedeniyle yazarlar bu bağlantının keşif niteliğinde olduğunu ve doğrulanması gerektiğini vurguluyor; yine de dolaşımdaki bağışıklık hücrelerinde sürekli artan bir metabolik dürtünün uyarı işareti olabileceğine dair bir ipucu sunuyor.
Sepsisli hastalar için bunun anlamı nedir
Uzman olmayan bir okuyucu için temel mesaj şu: erken sepsiste dolaşımdaki bağışıklık hücrelerinin içindeki enerji santralleri basitçe iflas etmiyor; bunun yerine aşırı hız moduna geçiyor gibi görünüyor. Bu ekstra çaba vücudun enfeksiyonla ilk mücadelesini destekliyor olabilir, ancak bazı hastalarda bu durum düşmek yerine tırmanmaya devam ediyor ve kan bağışıklık hücrelerindeki bu kalıcı aşırı aktivite daha kötü hayatta kalma ile ilişkiliydi. Çalışma henüz bu mitokondriyal itmenin faydalı mı, zararlı mı yoksa farklı evrelerde her ikisi mi olduğunu göstermiyor; ancak sepsisin enfeksiyon ve iltihap kadar vücudun enerji ekonomisiyle de ilgili olduğunu vurguluyor. Gelecekte bu hücresel enerji kullanımını dikkatle izlemek ve belki de nazikçe yönlendirmek, hekimlerin YBÜ’de sepsisle savaşan hastalar için riski değerlendirme ve tedaviyi kişiselleştirme yollarından biri olabilir.
Atıf: Moonen, H.P.F.X., Slingerland-Boot, R., de Jong, J.C.B.C. et al. Progression of peripheral blood mononuclear cell mitochondrial function during the early phase of sepsis in intensive care unit patients. Sci Rep 16, 8828 (2026). https://doi.org/10.1038/s41598-026-39202-2
Anahtar kelimeler: sepsis, mitokondri, immün hücreler, kritik hastalık, hücresel metabolizma