Clear Sky Science · tr
Şiddetli tip‑2‑yüksek astım endotipleri için inhalasyonla verilebilecek küçük‑molekül IL‑33/ST2 antagonistlerinin in silico tanımlanması
Nefes Almayı Neden Etkiler
Milyonlarca şiddetli astım hastası için, çağdaş inhalerler ve gelişmiş enjeksiyonlar bile onları nefes darlığına ve tehlikeli atak riski altında bırakabiliyor. Bu çalışma, tanıdık hap benzeri ilaçların astımdaki akciğerlerdeki “alarm” sinyallerinden birini engelleyecek şekilde inhalasyon yoluyla yeniden tasarlanıp tasarlanamayacağını araştırıyor. Sadece bilgisayar simülasyonları kullanarak, araştırmacılar şiddetli, alerji kaynaklı astımda rol oynayan önemli bir reseptöre uyabilecek küçük moleküller aradılar; amaç hazır bir ilaç sunmaktan ziyade gelecekteki laboratuvar testleri için zemin hazırlamaktır.
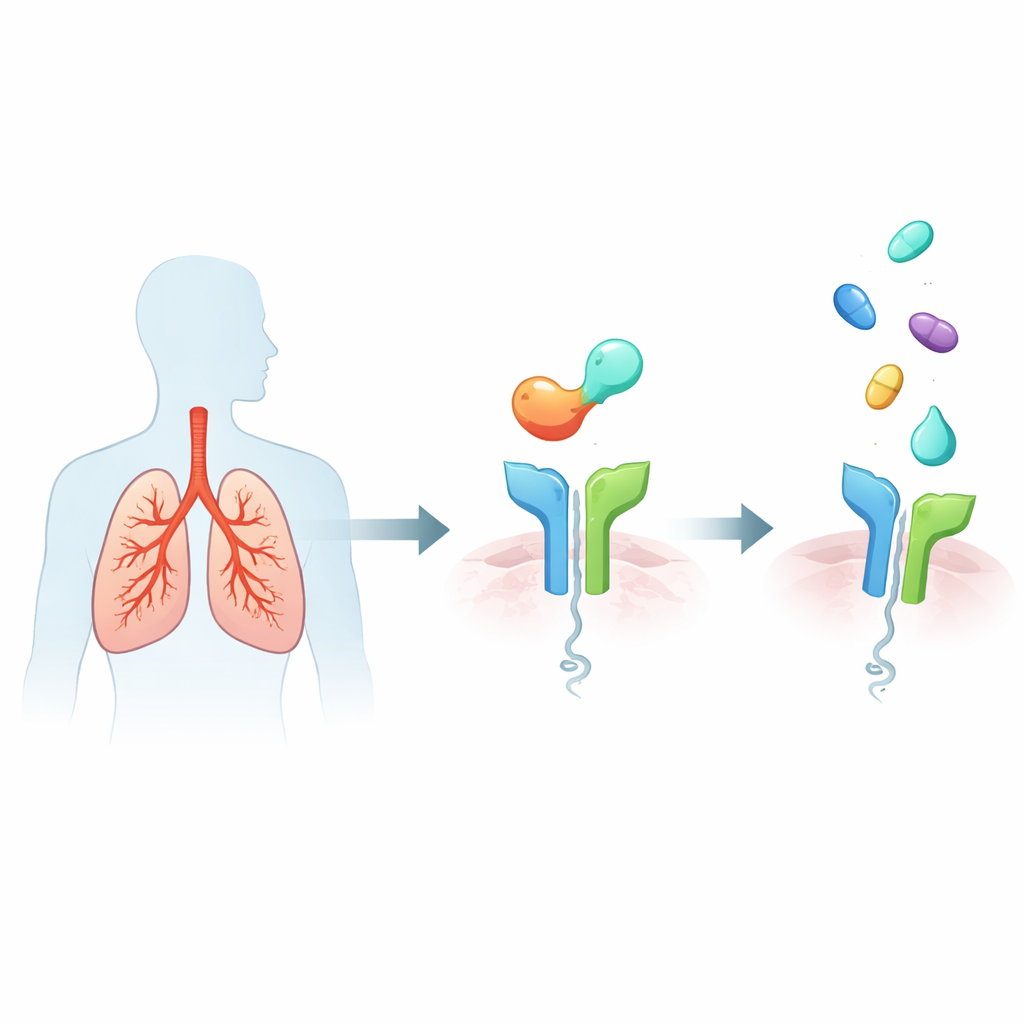
Astımlı Akciğerlerdeki Alarm Sistemi
Şiddetli tip‑2‑yüksek astım, hava yollarını mukus ve iltihap hücreleriyle dolduran, solunum yollarını daraltan ve zaman içinde akciğer yapısını hasara uğratabilen aşırı aktif bir bağışıklık yanıtıyla karakterizedir. Önemli bir tetikleyici, stres altındaki hava yolu örtü hücreleri tarafından salınan IL‑33 adlı bir proteindir. IL‑33, çeşitli bağışıklık hücrelerinde ST2 adlı bir reseptöre tutunur; bunlar daha sonra hırıltı, alevlenmeler ve uzun vadeli hava yolu yeniden şekillenmesi gibi astımın tipik özelliklerini tetikleyen güçlü haberci moleküller salar. Artmış IL‑33/ST2 aktivitesi daha kötü belirtiler ve daha sık ataklarla ilişkilendirildiği için, ST2 çekici bir yukarı akış hedefi olarak öne çıkıyor: ST2 engellenirse, birçok aşağı akış iltihap sinyali aynı anda yatıştırılabilir.
Antikorlar’dan Günlük Tarz İlaçlara
Şiddetli astım için mevcut bazı tedaviler, kanda iltihap proteinlerini temizleyen veya bunların reseptörlerini engelleyen enjeksiyon yoluyla verilen antikorları kullanır. Bazıları için etkili olsa da, bu biyoteknolojik ilaçlar pahalıdır, enjeksiyonla verilmelidir ve yolaktaki daha alt düzey sinyallere odaklanır. Buna karşılık, küçük‑molekül ilaçlar—daha çok geleneksel hap veya inhalerlere benzeyen—ölçeklenebilir şekilde üretilebilir, kolayca depolanabilir ve potansiyel olarak doğrudan akciğerlere verilebilir. Zorluk, ST2’nin IL‑33 ile geniş bir protein‑protein yüzeyi aracılığıyla bağlanmasıdır; bu, küçük moleküllerin bir enzimin derin cepte tuttuğu gibi kolayca bozamayacağı bir yapıdır. Bu nedenle yazarlar, ST2–IL‑33 kompleksine ait yüksek çözünürlüklü yapısal verilere ve modern in silico araçlara başvurarak bilinen anti‑iltihap ilaçlardan herhangi birinin beklenmedik şekilde bu arayüzün bir kısmına tutunup tutunamayacağını araştırdılar.
Bilgisayar ile Reseptör Yüzeyinin Taranması
Araştırma ekibi, IL‑33’e bağlı insan ST2’nin kristal yapısını kullanarak önce IL‑33’ü kaldırıp reseptörün bağlanma yüzeyini açığa çıkardı ve küçük bir molekülün yerleşebileceği en umut verici bölgeyi belirlemek için bir cep bulma programı kullandı. Ardından Montelukast ve Zafirlukast gibi lökotrien blokörleri, immünomodülatör talidomid türevleri ve JAK inhibitörleri gibi astım veya ilgili bağışıklık hastalıklarında halihazırda kullanılan on klinik açıdan ilgili küçük molekül seçtiler; ayrıca referans olarak daha önce rapor edilmiş ST2‑odaklı bir molekül eklediler. Sanal docking yazılımı ile her bileşik ST2 yüzeyine binlerce kez konumlandırıldı ve en iyi konumlar tahmini bağlanma güçlerine göre puanlandı. Zafirlukast, bilinen ST2‑yönelimli karşılaştırıcıyı ve Montelukast’ı hafifçe geride bırakarak en üst sırada yer aldı.
Ekranda Öncü Bir Molekülü Ayarlamak
Zafirlukast tahmini bağlanma ve genel ilaç‑benzeri davranış açısından en umut verici dengesi gösterdiği için yazarlar bu molekülün yapay zekâ destekli bir tasarım aracıyla değiştirilmiş bir versiyonunu oluşturdular. Amaç ST2’ye tutunuşunu korurken tahmini güvenlik profilini iyileştirmekti. Yeniden tasarlanmış analogun docking skoru çok benzerdi ve in silico olarak daha az toksik olması öngörüldü. Ayrıntılı temas haritaları, ana bileşik ile modifiye edilmiş bileşiğin IL‑33’ün normalde temas ettiği bazı aynı ST2 amino asitlerine dokunduğunu gösterdi; bu da onların arayüzün işlevsel açıdan önemli bölgelerini işgal ettiklerine dair ipucu veriyor. Uzun süreli moleküler dinamik simülasyonlar—suda ve tuzlu ortamda yarım mikrosaniyelik sanal hareket—reseptör ve ligandın her ikisinin de esnek kaldığını; küçük molekülün yüzeye sıkıca kilitlenmek yerine farklı pozisyonları denediğini gösterdi. Zaman içindeki etkileşim enerjilerinin hesapları, nispeten düz bir protein‑protein yüzeyini araştıran bir moleküle uygun şekilde anlamlı ama dinamik bir birlikteliğe işaret etti.
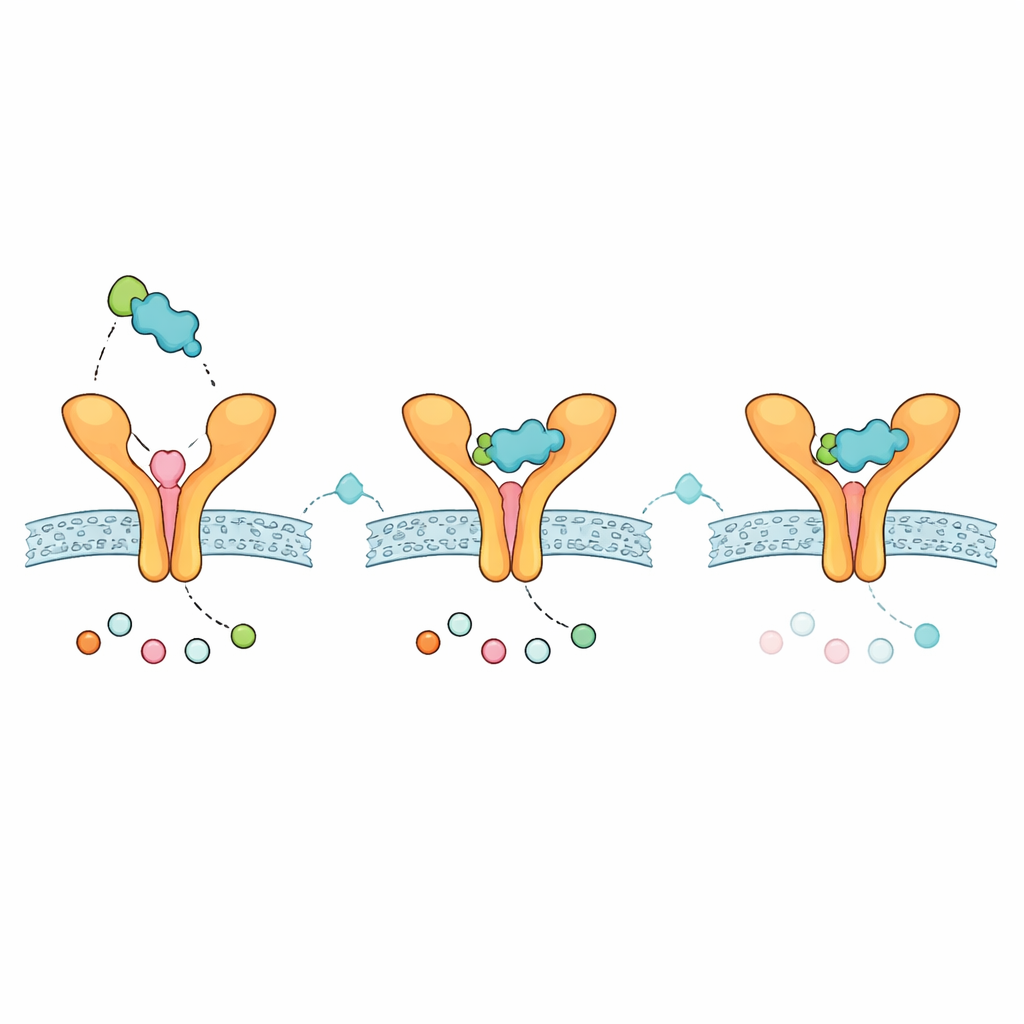
Gelecekteki Bir Inhalerin Nasıl Davranabileceğine Dair İpuçları
Yeniden tasarlanmış Zafirlukast’ın muhtemel bir ilaç olarak davranıp davranamayacağını araştırmak için ekip, emilim, dağılım, metabolizma, atılım ve toksisiteye ilişkin standart hesaplamalı kontrolleri çalıştırdı. Analog, yaygın oral ilaç‑benzerlik kurallarını karşıladı, orta boyut ve yağda çözünürlük gösterdi ve beyne girmeyeceği öngörüldü—bu özellikler, tüm vücutta sınırlı yan etkiyle akciğere odaklı bir tedavi için avantajlı olabilir. Çözünürlük tahminleri modele göre değişti; bu da özellikle inhalasyon gibi oral olmayan yollar için dikkatli bir formülasyon gerektiğini gösteriyor. Bileşiğin ayrıca belirli karaciğer enzimleriyle etkileşime girebileceği öngörüldü; bu da başka ilaçlarla birlikte kullanılacaksa potansiyel ilaç‑ilaç etkileşimlerinin göz önünde bulundurulması gerektiğini işaret ediyor.
Bu Çalışma Gerçekte Ne Gösteriyor
Yeni bir astım ilacı sunmaktan ziyade, bu çalışma hava yolu hücrelerinin yüzeyindeki IL‑33/ST2 alarm sistemine müdahale edebilecek küçük molekülleri bulmak ve rafine etmek için adım adım bir hesaplamalı strateji gösteriyor. Çalışma, Zafirlukast ve bir yapay zekâyla optimize edilmiş akrabasını laboratuvar deneyleri için makul başlangıç noktaları olarak vurguluyor; bu bileşiklerin ST2 arayüzünün kilit parçalarını işgal edebildiklerini ve genel olarak kabul edilebilir tahmini güvenlik ve ilaç‑benzeri özelliklere sahip olduklarını gösteriyor. Ancak tüm kanıtlar sanal düzeydedir: bu çalışmalar bu moleküllerin IL‑33’ün ST2’ye bağlanmasını engellediğini, iltihap sinyalini azalttığını veya hastaların daha rahat nefes almasına yardımcı olduğunu kanıtlamaz. Bu sorular biyokimyasal testler, hücre çalışmaları, hayvan modelleri ve nihayetinde klinik deneyler gerektirecektir. Şimdilik çalışma, hesaplamalı bir yol haritası ve bedenin kendi astım alarm düğmesini pratik, inhale edilebilir bir ilaç hedefine dönüştürmeyi amaçlayan bilim insanları için kısa bir aday iskelet listesi sunuyor.
Atıf: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
Anahtar kelimeler: şiddetli astım, IL‑33 ST2 yolu, küçük‑molekül antagonistleri, in silico ilaç tasarımı, inhale edilen tedaviler