Clear Sky Science · tr
Yapı-temelli modelleme CYP153A6’nın toluen türevlerine karşı yeni aktivitesinin moleküler temelini ortaya koyuyor
Zor Kimyasal İşleri Doğaya Devretmek
Kimyagerler ve sanayi, kirleticileri temizlemek veya ilaç ve koku maddeleri için bileşenler üretmek gibi amaçlarla karbon–hidrojen bağlarına oksijen ekleyen reaksiyonlara dayanır. Bunu sert kimyasallar veya ağır metal atıkları olmadan, temiz biçimde yapmak zordur. Bu çalışma, toprak bakterisinden elde edilen CYP153A6 adlı doğal bir katalizörü inceliyor ve basit ama büyük sonuçları olabilecek bir soru soruyor: bu enzim, yakıtların ve çözücülerin yaygın bileşenleri olan toluen benzeri kimyasalları daha faydalı ve çevre dostu ürünlere seçici olarak “yükseltecek” şekilde yönlendirilebilir mi?
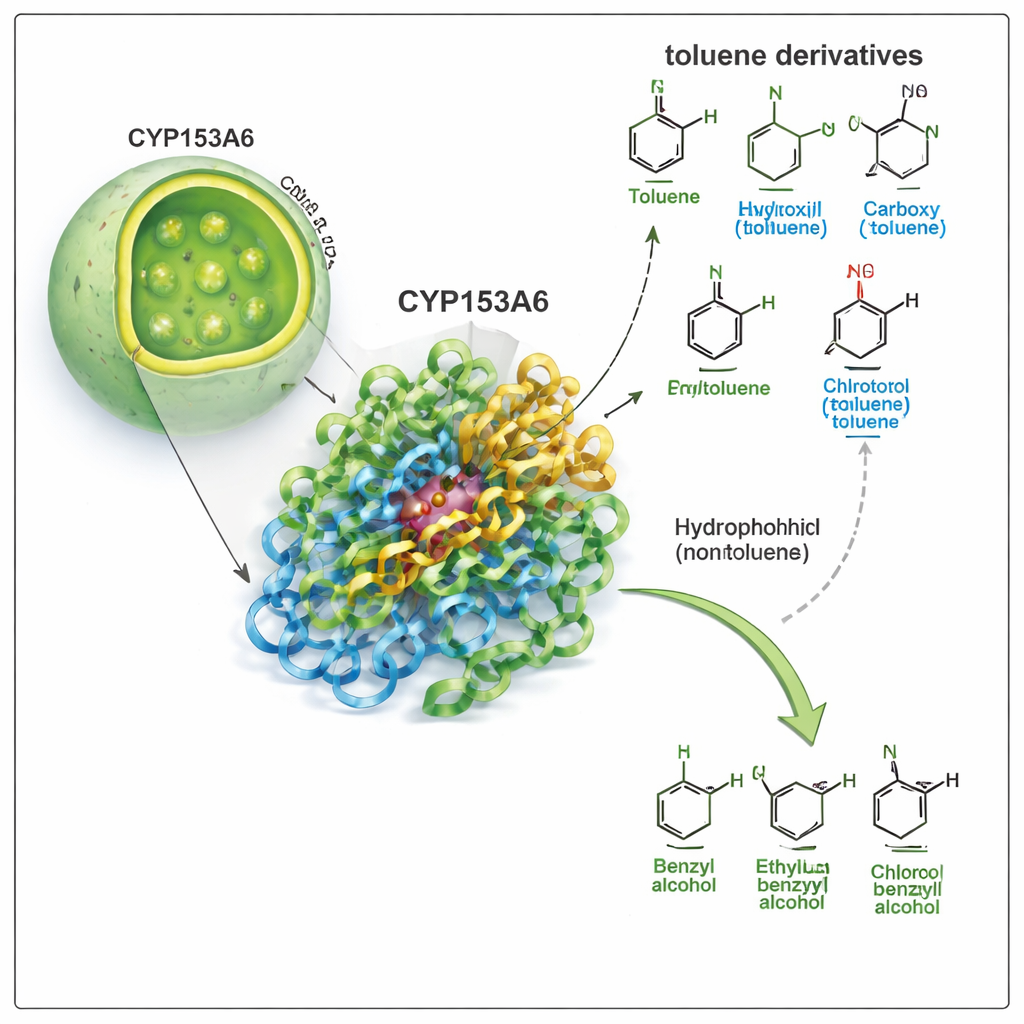
Tek Bir Noktayı Seçen Bir Enzim
CYP153A6, doğanın çok yönlü oksidasyon uzmanları olan geniş sitokrom P450 ailesine aittir. Birçok endüstriyel katalizörden farklı olarak bu enzim suda, ılımlı sıcaklıkta çalışır ve bir molekül üzerinde çok belirli pozisyonları seçer. Önceki çalışmalar CYP153A6’nın basit hidrokarbon zincirlerinin uçlarına ve bazı bitkisel koku moleküllerine oksijen eklediğini göstermişti. Burada yazarlar, enzimin toluen ve ilgili bileşiklerde benzylic (benzen halkasına bağlı küçük yan zincir) pozisyonuna saldırıp saldıramayacağını soruyor. Bu dönüşüm toluen türevlerini benzil alkollere çevirir; bunlar ilaçlar, aromalar ve ince kimyasallar için değerli yapı taşlarıdır.
Enzimin Hangi Molekülleri Sevdiğini Test Etmek
Grup önce CYP153A6 üreten genetiği değiştirilmiş E. coli hücrelerini, bütün hücre veya hücre dışı ekstrakt olarak kullanarak biyo-dönüşüm deneyleri yaptı. Enzimi aromatik halka üzerindeki farklı gruplarla (metil, klor, metoksi, hidroksil veya nitro gibi) ve bunların yerleşimle-riyle (para, meta veya orto) değişen bir toluen türevleri paneline maruz bıraktılar. Enzim, p-simen, p-ksilin, p-metil-anisol ve p-klorotoluen gibi apolar veya hafifçe polar bileşiklerde çok iyi performans göstererek benzylic metil grubunu tutarlı biçimde benzil alkole dönüştürdü. Çarpıcı şekilde, p-krezol, p-metil benzil alkol ve p-nitrotoluen gibi daha güçlü polar molekülleri tamamen göz ardı etti; oysa yapısal olarak benzerlerdi. Bu desen enzimin cebinin güçlü şekilde hidrofobik olduğunu ve polar grupları sevmediğini düşündürdü.
Moleküler Makinenin 3B Haritasını İnşa Etmek
CYP153A6’nın üç boyutlu yapısı deneysel olarak çözülmemiş olduğundan araştırmacılar bilinen yapıya sahip yakından ilişkili bir P450 kullanarak yüksek kaliteli bir bilgisayar modeli oluşturdu. Bu modeli geometrisini kontrol ederek ve proteinin zaman içinde kararlı kalıp kalmadığını görmek için uzun moleküler dinamik simülasyonları çalıştırarak doğruladılar; protein kararlı kaldı. Simülasyonlar, dışarıya dar tünellerle bağlı gömülü bir aktif bölgeyi ortaya koydu; substratlar bu tünellerden girip ürünler dışarı çıkar. Bu tüneller, yüzeydeki esnek döngüler tarafından şekillendirilir ve kapatılır; bu da enzimin hidrofobik molekülleri reaktif heme demir merkezine yönlendirirken su ve oksitlenmiş ürünlerin kaçmasına izin vermesini açıklamaya yardımcı olur.
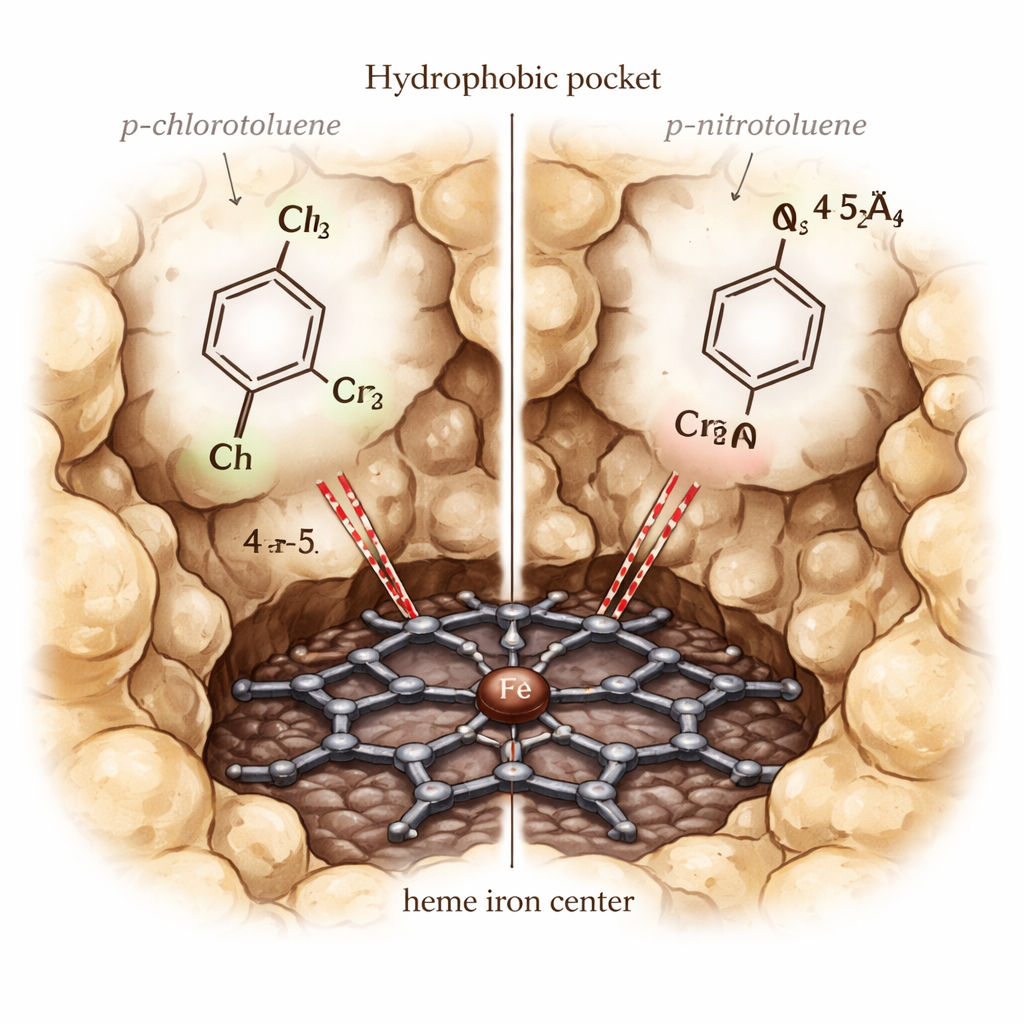
Moleküllerin Yerleşmesini, Hareketini ve Reaksiyonunu İzlemek
Model elde edildikten sonra yazarlar farklı toluen türevlerinin CYP153A6 içinde nasıl bağlandığını simüle etti. Birçok hafifçe farklı protein şekli ve heme demirinin birkaç elektronik durumu denenerek ensemble docking (kümeleştirilmiş yerleşim) adı verilen bir yaklaşım kullandılar; amaç gerçek substratları non-substratlardan ayırt eden en iyi düzenlemeleri belirlemekti. Kazanan senaryo, demirin dinlenme ferrik durumda olduğu ve cebe ekstra su molekülleri bulunmadığı durumdu ve bilinen substratları doğru şekilde tercih etti. Takip simülasyonları, her molekülün heme ile göreceli konumunu kare kare izledi. p-simen ve p-ksilin gibi iyi substratlar benzylic metil grupları demire dönük olacak şekilde demire yakın kaldı ve tahmini bağlanma enerjileri oldukça elverişliydi. Kötü substratlar genellikle uzaklaştı, garip yönelimler benimsedi veya cebin çoğunlukla yağlı yan zincirleriyle olumsuz etkileşimlere girdi.
Neden Birine Benzeyen Biri Reaksiyona Giriyor da Diğeri Girmiyor
Öne çıkan bir bilmece şuydu: p-klorotoluen CYP153A6 tarafından verimli şekilde oksitlenirken, p-nitrotoluen edilmedi; oysa her ikisi de cebin içine sığıyor ve simülasyonlarda benzer bağlanma gücüne sahip görünüyordu. Bunu çözmek için yazarlar enzimin yüksek reaktif “Bileşik I” durumunda daha ayrıntılı kuantum mekaniği/klasik mekaniği (QM/MM) hesaplamaları yaptılar. Bu hesaplamalar nitro grubunun benzylic karbona çok fazla elektron yoğunluğu çektiğini ve bu karbonun oksitlenmesini zorlaştırdığını gösterdi; geometrik olarak yeterince yakın olsa bile. Buna karşılık kloro grubu heme ile substrat arasında daha iyi elektronik iletişime izin veriyor; aromatik halka ve metil grup üzerinde daha yüksek spin yoğunluğu ve kritik hidrojen soyutlama adımı için daha reaktif bir hizalanma yansıtıyor.
Temiz Kimya İçin Anlamı
Günlük terimlerle CYP153A6, belirli yakıt benzeri molekülleri oksijenin belirli bir noktaya eklenmesi için tam olarak doğru şekilde tutan küçük, yağlı bir eldivermiş gibi davranır—bunları daha suya çözünebilir, kullanışlı ve sonuçta daha kolay bozunur ürünlere çevirir. Çalışma enzimin apolar yerineçilere öncelik verdiğini ve bir toluen türevinin dönüştürülüp dönüştürülmeyeceğini şekil ve elektron akışının birlikte belirlediğini gösteriyor. CYP153A6’nın bu molekülleri nasıl tanıdığını ve aktive ettiğini açıklayarak, aromatik kirleticilerin temizlenmesine veya karmaşık kimyasalların daha sürdürülebilir şekilde üretilmesine yardımcı olabilecek geliştirilmiş versiyonların mühendisliği için bir plan sunuyor.
Atıf: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
Anahtar kelimeler: biyokataliz, sitokrom P450, toluen hidroksilasyonu, enzim mühendisliği, yeşil kimya