Clear Sky Science · tr
Kadmiyum, ROS–TCA yolunu aktive ederek fare spermatositlerinde ferroptozisi tetikliyor
Yaygın Bir Metalin Erkek Sağlığı İçin Neden Önemli Olduğu
Kadmiyum, pillerde, pigmentlerde ve diğer endüstriyel ürünlerde kullanılan yumuşak bir metaldir. Toprakta, suda ve gıdada birikebilir ve zaman içinde sessizce vücudumuza girer. Birçok çalışma kadmiyum maruziyetini erkeklerde düşen sperm sayısı ve bozulmuş sperm kalitesi ile ilişkilendirmiştir, ancak spermi oluşturan hücrelere nasıl zarar verdiği tam olarak net değildi. Bu çalışma, soruna odaklanarak kadmiyumun farede sperm oluşturan hücreleri, demirle ilişkili ve mitokondrilerdeki (hücresel enerji santralleri) stresli bir enerji sistemiyle bağlantılı belirli bir hücre ölümü yoluna nasıl ittiğini ortaya koyuyor.
Kirlenmeden Savunmasız Spermatositlere
Kadmiyum, erkek üreme sistemi için iyi bilinen bir çevresel zararlıdır. İş yerinde maruz kalan veya kirli bölgelerde yaşayan erkekler genellikle azalmış sperm sayısı, hareketliliği ve normal şekil ile hatta sperm DNA’sında hasar gösterir. Hayvan çalışmaları da bunları doğruluyor; küçülmüş testisler, zayıflamış koruyucu bariyerler, düşük testosteron ve geniş çaplı germ hücre kaybı raporlanmış. Yazarlar daha önce kadmiyumun testis dokusunda demir bağımlı sıra dışı bir hücre ölümü türü olan ferroptozisi tetikleyebileceğini gözlemlemişlerdi. Mevcut çalışmada, kadmiyumun fare spermatositlerine nasıl zarar verdiğini ve bu demirle bağlantılı ölüm yolunun rol oynayıp oynamadığını anlamak için bu hücrelere odaklandılar.
Demir Aşırı Yükü ve Özel Bir Hücre Ölümü Türü
İncelemek için ekip, bir fare spermatosit hücre hattını kültürde büyüttü ve hücreleri kadmiyuma maruz bıraktı; bazı deneylerde ferroptozisi engellediği bilinen ilaçlar da kullanıldı. Kadmiyum hücre canlılığını yaklaşık yarıya düşürdü ve hücre bölünmesini yavaşlattı. Hücre içinde serbest demir düzeyleri ve malondialdehit adı verilen bir yağ hasarı belirteci keskin şekilde arttı, oysa koruyucu bir enzim olan GPX4 azaldı. Demir depolanması ve dışa aktarımıyla ilgili diğer proteinler arttı; bu da demir yönetiminin ciddi şekilde bozulduğunu gösteriyordu. Araştırmacılar demir şelatörü ve lipid koruyucu bir molekül gibi ferroptozis engelleyicileri eklediklerinde, bu zararlı değişimlerin birçoğu hafifledi ve hücre sağkalımı iyileşti. Bu değişimler birlikte ferroptozisin imzasıyla uyumlu; kadmiyumun hücreleri belirsiz bir şekilde öldürmekten çok, onları demir- ve lipid kaynaklı bu özel ölüm programına ittiğini gösteriyor.
Kuşatma Altındaki Mitokondriler
Hikâye, bilim insanları dikkatlerini reaktif oksijen türleri (ROS) gibi yan ürünler de üreten enerji merkezleri mitokondrilere çevirdiklerinde derinleşti. Mikroskop altında sağlıklı spermatositler uzun, ipliksi mitokondriler gösterirken, kadmiyuma maruz kalan hücrelerde kısa, parçalanmış mitokondriler görüldü; bu yapısal hasarın bir işaretiydi. Ölçümler mitokondriyal ROS’un zirve yaptığını ve mitokondri zarındaki elektriksel potansiyelin—işlev için önemli bir gösterge—azaldığını doğruladı. Hücreler, stres sensörü Nrf2 tarafından yönetilen proteinler de dahil olmak üzere iç savunma sistemlerini yükselterek yanıt verdi, ancak bu savunmalar yeterli olmadı. Önemli olarak, ferroptozis engelleyici ilaçlar mitokondriyal ROS’u azalttı ve mitokondri sağlığını kısmen geri getirdi; bu da zarar görmüş enerji santrallerini doğrudan demir-bağımlı ölüm yoluna bağladı.
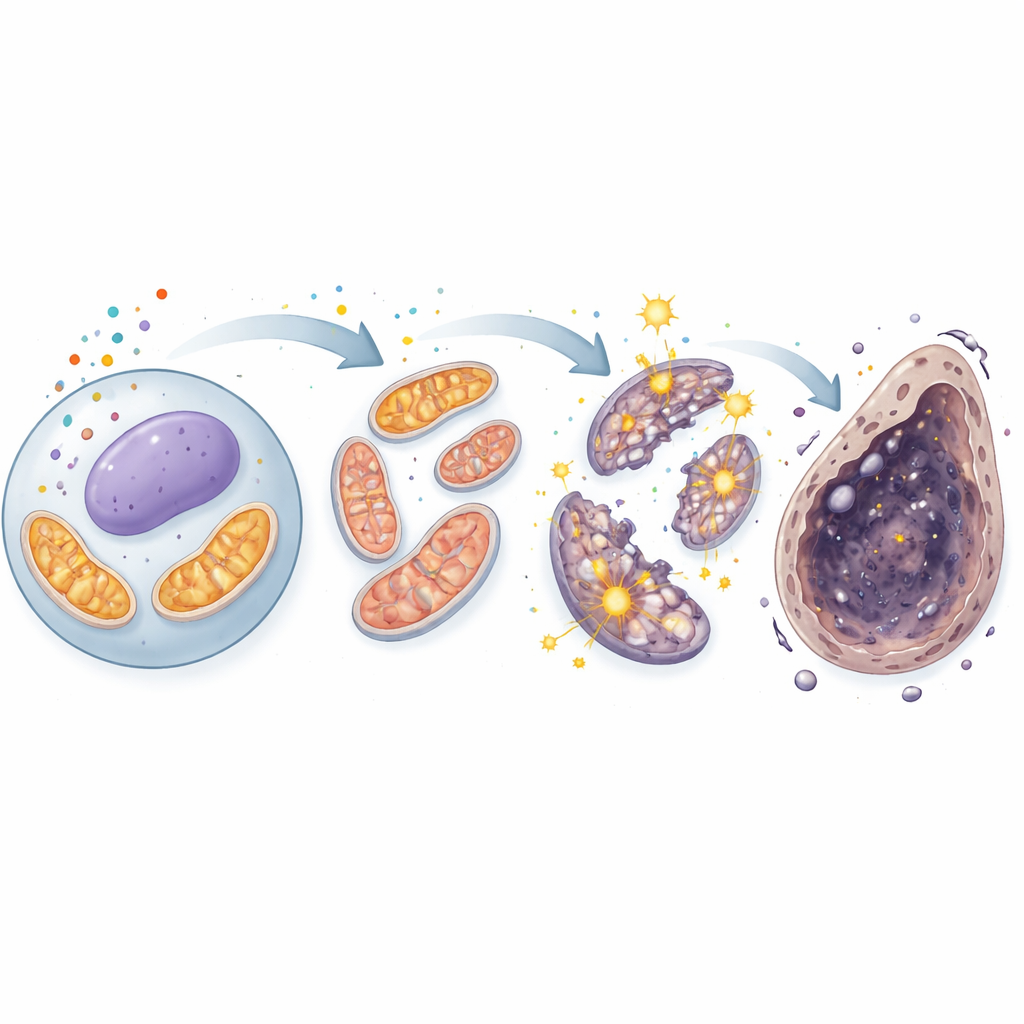
Hücresel Enerji Santralinde Döngüsel Kötüleşme
Gen aktivite profillemesi ve metabolit ölçümlerinin bir kombinasyonunu kullanarak araştırmacılar, kadmiyumun yalnızca mitokondrileri zedelemediğini—aynı zamanda onların temel enerji devresini, trikarboksilik asit (TCA) döngüsünü de ele geçirmiş gibi göründüğünü gözlemlediler. İki merkezi TCA ara ürünü olan alfa‑ketoglutarat ve süksinat düzeyleri anlamlı şekilde arttı ve döngüye taze yakıt sağlayan bir enzim olan pirüvat karboksilazın aktivitesi yükseldi. Bu, hasarlı hücrelerde TCA döngüsünün paradoksal olarak aşırı etkin hale geldiğini, solunum zinciri üzerinden daha fazla elektron zorlandığını ve bunun sonucu olarak daha fazla ROS sızıntısı olduğunu düşündürüyor. Bu ekstra ROS daha sonra demir kimyası ve zar hasarını besleyerek ferroptozisi güçlendiriyor. Yine, ferroptozis inhibitörleri bu metabolik bozulmaları geri çekti ve kadmiyum, mitokondriyal aşırı etkinlik ve demir-bağımlı hücre ölümü arasındaki sıkı bağlantıyı vurguladı.
Bu Bulguların Üreme ve Gelecek Araştırmalar İçin Anlamı
Basitçe ifade etmek gerekirse, çalışma kadmiyumun spermatositlere doğrudan mitokondrilerine zarar vererek ve enerji döngüsünü zararlı bir aşırı sürüşe sokarak saldırdığını gösteriyor. Bu kombinasyon hücreleri reaktif oksijen molekülleriyle dolduruyor ve demir dengesini bozarak onları ferroptozise itiyor. Spermatositler sağlıklı sperm üretimi için gerekli olduğundan, bunların kaybı kadmiyum maruziyetinin erkek fertilitesi ile güçlü bağlantısını açıklamaya yardımcı olabilir. Bu deneyler bir kabın içindeki fare hücrelerinde gerçekleştirilmiş olsa da, gelecekteki hayvan ve insan çalışmalarının test edebileceği net bir mekanistik harita sunuyor. Çalışma ayrıca potansiyel koruyucu stratejilere işaret ediyor: mitokondriyal stresi yatıştıran, TCA döngüsünü ince ayarlayan veya demir kaynaklı membran hasarını önleyen ilaçlar veya besinler, kadmiyum gibi çevresel metallere karşı erkek üreme sistemini korumaya yardımcı olabilir.
Atıf: Xiong, L., Yi, L., Zeng, X. et al. Cadmium induces ferroptosis in mouse spermatocytes by activating the ROS–TCA pathway. Sci Rep 16, 8449 (2026). https://doi.org/10.1038/s41598-026-38827-7
Anahtar kelimeler: kadmiyum toksisitesi, erkek üreme yeteneği, mitokondriyal stres, ferroptozis, reaktif oksijen türleri