Clear Sky Science · tr
Entegre yapısal modelleme ve veri odaklı hedefli mutagenezle DEK1 kalpain domaininin çözünebilirliğinin hesaplamalı optimizasyonu
Bitki proteinlerini ‘davranır’ hâle getirmenin önemi
Bitkilerin nasıl büyüdüğünü kontrol eden birçok protein, laboratuvarda incelemeye çalışıldığında çözünmeyi reddeden, büyük ve kırılgan moleküllerdir. DEK1 adlı bu proteinlerden biri, tek hücre düzeyinden başlayarak bitki vücutlarının şekillenmesine yardım eder. Ancak DEK1’in hayati bir bölgesi bakteri ortamında üretildiğinde topaklandığı için 3B yapısı belirlenememiş ve bu da onu anlamayı ve kullanmayı yavaşlatmıştır. Bu çalışma, hesaplamalı modelleme ve akıllı, veri odaklı tasarım kullanarak bu sorunlu bölgeyi yapısını bozmadan daha çözünebilir hâle getirebileceğini gösteriyor—zor proteinleri dizginlemek için genel bir reçete sunuyor.
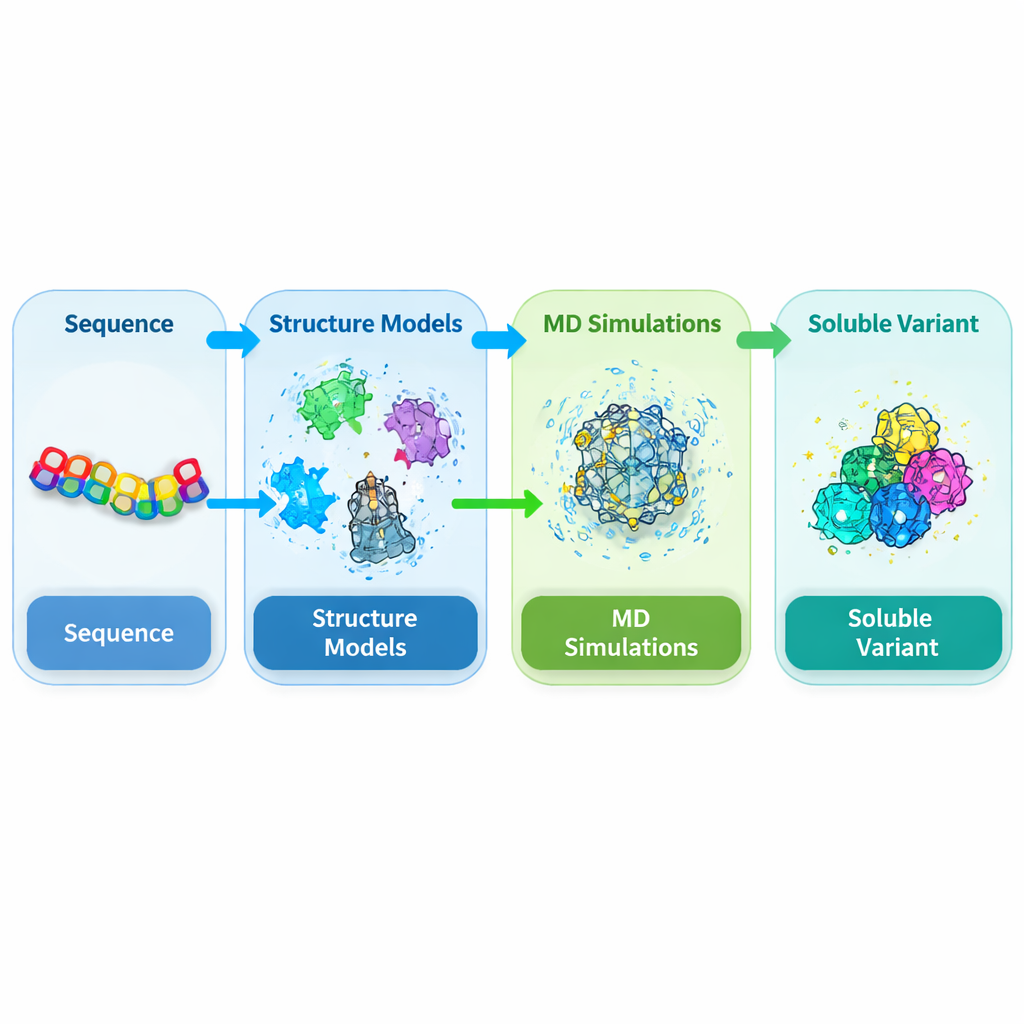
Önemli bir bitki proteindeki sorunlu bölgeyi hedef almak
DEK1, hücre zarlarına gömülü sıra dışı derecede büyük bir proteindir ve bir kesme enzimi bölgesi olan kalpain domaini ile sonlanır. Genetik çalışmalar bu domenin yosunlar ve tarım bitkileri gibi bitkilerde normal gelişim için gerekli olduğunu göstermiştir, ancak yapısı hiçbir zaman deneysel olarak çözülememiştir. Araştırmacılar bu kalpain çekirdeğini (CysPc olarak adlandırılır) yaygın konağın olan Escherichia coli’de üretmeye çalıştıklarında, bu çekirdek genellikle çözünmez hale gelir ve yoğun inklüzyon cisimleri oluşturur. Bu durum detaylı yapısal ve fonksiyonel çalışmalar için gereken miktar ve kalitede saflaştırmayı neredeyse imkansız kılar. Bu nedenle yazarlar, CysPc domainini genel şeklini koruyarak daha kolay çözünebilecek şekilde yeniden tasarlamayı amaçladılar.
Başlangıçtan güvenilir bir 3B model oluşturmak
Bu bitki kalpainine ait deneysel bir yapı olmadığından, ekip önce 3B şeklini tahmin etmek zorundaydı. AlphaFold2, SWISS-MODEL ve I-TASSER dahil olmak üzere birkaç son teknoloji yapı tahmin aracını birleştirdiler ve bu tahminleri memeli kalpainlerine ait bilinen yapılarla dayandırdılar. Bir mutabakat yaklaşımı kullanarak, elde edilen modelleri omurga geometrisi, paketlenme ve bilinen yapısal kalıplarla uyumu değerlendiren çoklu kalite testleriyle rafine edip kontrol ettiler. Bu bağımsız kontroller, CysPc domaininin entegre modelinin tek bir tahminden daha güvenilir olduğunu gösterdi ve amino asit dizisine yapılacak küçük değişikliklerin çözünebilirliği nasıl iyileştirebileceğini araştırmak için sağlam bir başlangıç noktası sağladı.
Simüle edilmiş bir çözücüde sanal mutasyonları test etmek
3B model elde edildikten sonra yazarlar, protein ve çevresindeki su moleküllerinin bilgisayarda zaman içinde izlenmesini sağlayan kapsamlı moleküler dinamik simülasyonları çalıştırdılar. Yüzeyde yer alan, esnek, hidrofobik veya agregasyonu teşvik etmesi tahmin edilen kalıntılara odaklandılar. Aday pozisyonlar tek tek daha su dostu amino asitlere çevrildi ve ardından her biri için 200 nanosaniye simülasyon gerçekleştirildi. Her varyant için su ile temas eden yüzey alanı, proteinin ne kadar kompakt kaldığı ve atomların ne kadar dalgalandığı gibi çözünebilirlikle ilgili özellikler ölçüldü. Birçok tekli mutasyon, genel katlanmayı değiştirmeden çözeltide maruz kalmayı veya iç hidrojen bağlarını mütevazı biçimde artırdı; bu da CysPc’nin temel iskeletinin dikkatle seçilmiş ikameleri tolere edebileceğini düşündürdü.
Algoritmaların mutasyon uzayını aramasına izin vermek
Tek bir kalıntıyı değiştirmek nadiren çözünebilirlikte dramatik kazançlar sağlar, bu yüzden araştırmacılar sonraki aşamada iki ve üçlü mutasyon kombinasyonlarını incelediler. En iyi tekli mutasyonlardan oluşturulmuş bir çift ve üçlü varyant kütüphanesi ürettiler ve her birini yeniden simüle ettiler. Bu tasarımları adil biçimde puanlamak ve sıralamak için, çözünürlükle ilişkili olduğu bilinen çoklu simülasyon özelliklerini birleştiren ağırlıklı bir indeks tanımladılar; bu indeks artan hidratasyonu ve iç bağlanmayı ödüllendirirken aşırı esnekliği cezalandırıyordu. Ardından büyük üçlü mutant uzayında gezinmek ve en umut verici kombinasyonları önermek için bir pekiştirmeli öğrenme algoritması (Proximal Policy Optimization) kullandılar. Bu veri odaklı arama, en iyi aday olarak MUT347 adlı belirli bir üçlü mutantta yoğunlaştı.
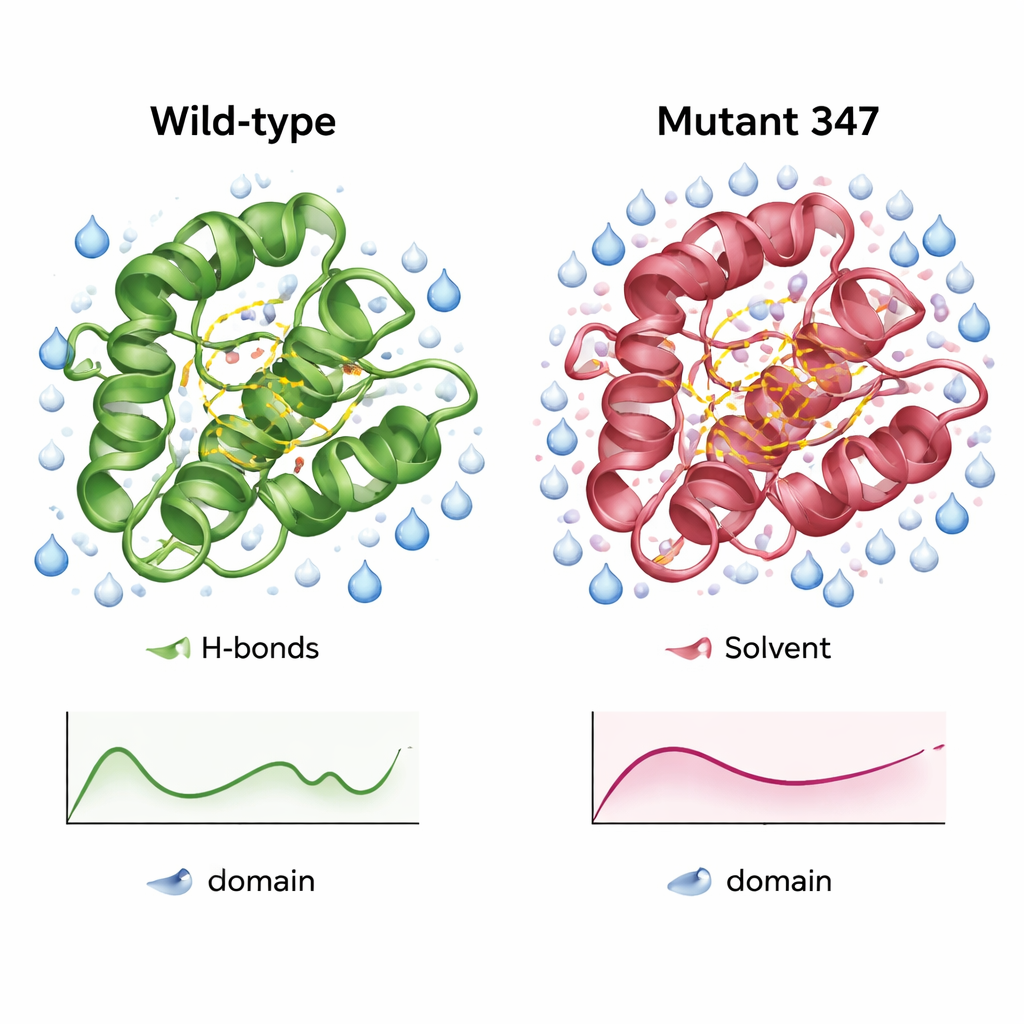
Daha kompakt, daha iyi hidratlanmış bir enzim versiyonu
Yabani tip CysPc domaini ve MUT347’ün ayrıntılı simülasyonları, mühendislik ürünü varyantın nasıl farklılaştığını ortaya koydu. MUT347 daha hızlı dengelendi ve başlangıç şekline göre daha küçük genel sapmalar gösterdi; bu da çözeltide daha büyük yapısal kararlılığa işaret ediyor. Döngüleri ve zincir uçları biraz daha az gevşekti, oysa çekirdek katalitik bölge orijinal esnekliğini koruyordu; bu da fonksiyonel olarak önemli hareketlerin korunduğunu düşündürüyor. Üçlü mutant, belirli bölgelerde daha fazla iç hidrojen bağına ve daha geniş su erişimli yüzeye sahipti; bunlar daha iyi organize olmuş ve daha iyi hidratlanmış bir yüzeyin işaretleridir. Farklı tuz konsantrasyonları ve pH seviyelerinde MUT347, orijinal proteine kıyasla tutarlı biçimde daha düşük dalgalanmalar gösterdi; bu davranış, topaklanma eğiliminin azalmasıyla ilişkilidir.
Bu çalışmanın protein incelemesi ve yeniden kullanımı açısından anlamı
Uzman olmayanlar için çıkarım şudur: yazarlar, deneylerle önceden bilinen bir yapıya gerek duymadan, hesaplamaya dayalı bir reçete kullanarak önemli bir bitki proteininin sorunlu, topaklanan parçasını daha çözünebilir ve iyi huylu bir versiyona dönüştürdüler. Modern yapı tahmini, uzun süreli simülasyonlar ve aynı anda birçok tasarım seçeneğini idare edebilen öğrenme algoritmalarının birleşimiyle, katlanmayı stabilize etmesi ve yüzeyi suya daha elverişli hale getirmesi öngörülen bir üçlü mutasyon belirlediler. Gerçek deney tüplerinde kazanımları doğrulamak için hâlâ deneysel çalışmalara ihtiyaç olsa da, bu çerçeve üretilmesi zor diğer ökaryotik proteinleri kurtarmada geniş biçimde yararlı olabilir ve nihayetinde şu anda erişilemeyen yapı ve fonksiyonların kilidini açmaya yardımcı olabilir.
Atıf: Dabiri, M., Levarski, Z., Struhárňanská, E. et al. Computational optimization of DEK1 calpain domain solubility through integrated structural modelling and data-driven targeted mutagenesis. Sci Rep 16, 7767 (2026). https://doi.org/10.1038/s41598-026-38805-z
Anahtar kelimeler: protein çözünürlüğü, hesaplamalı mutagenez, moleküler dinamikler, bitki kalpaini DEK1, protein mühendisliği