Clear Sky Science · tr
Ekstremofilik Ts2631 endolizinini̇n termal kararlılığının kalıntı düzeyindeki belirleyicileri
Sıcaklığı seven virüsler geleceğin antibiyotikleri için neden önemli?
Antibiyotik direnci artarken, bilim insanları tehlikeli bakterileri öldürmenin yeni yollarını bulmak için yarışıyor. Umut verici yaklaşımlardan biri, bakterileri enfekte eden virüslerden —bakteriyofajlardan— ödünç alınan silahlardan yararlanmak. Bu virüsler, bakteri hücre duvarlarında delikler açan endolizin adı verilen enzimler üretir. Burada ele alınan çalışma, İzlanda sıcak su kaynaklarında yaşayan bir virüsten gelen olağanüstü ısıya dayanıklı Ts2631 endolizinine odaklanıyor. Bu proteinin kaynama yakınındaki sıcaklıklarda bu denli kararlı olmasını sağlayan bireysel yapı taşlarını ortaya çıkararak, araştırmacılar ilaç ve biyoteknoloji için daha dayanıklı, daha uzun ömürlü antibakteriyel enzimler tasarlamayı umuyorlar. 
Kaynayan sıcak su kaynaklarında şekillenen viral bir araç
Ts2631, 60 °C’nin çok üzerine çıkan sularda yaşamayı seven Thermus scotoductus adlı bakteriyi enfekte eden bir bakteriyofajdan gelir. Ts2631 enzimi, bakteriyel hücreleri çevreleyen dayanıklı ağ olan peptidoglikandaki belirli bir bağı keser. Ts2631’i öne çıkaran özellik, aşırı termal kararlılığıdır: çözeltiye bağlı olarak yaklaşık 100–105 °C’ye kadar katlanmış halinde kalır. Bu, çoğu proteinin parçalanmaya başladığı sıcaklıkların çok üzerindedir. Yazarlar, Ts2631’i ılıman sıcaklıktaki bir virüsten gelen en iyi çalışılmış kuzeni T7 lizozim ile karşılaştırarak doğanın Ts2631’i bu kadar zorlu koşullarda ayakta tutmak için hangi yapısal hileleri kullandığını anlamaya çalıştı.
Daha kısa döngüler ve farklı yapı taşı karışımı
Proteinler, 20 tür amino asit zincirinden oluşur ve karmaşık şekillere katlanırlar. Araştırmacılar Ts2631 ve T7 lizozimin 3B yapılarını üst üste koyduklarında, genel mimarinin çok benzer olduğunu buldular: her ikisi de sıkı bir heliks ve zincir çekirdeğine sahip. Temel fark, bu elemanları birleştiren esnek döngü bölgelerindedir. Ts2631’de bu döngüler daha kısa ve daha az esneklik gösterirken, T7 lizozimde daha uzun ve gevşek döngüler görülür. Ts2631 ayrıca ısı direnciyle sıkça ilişkilendirilen belirli amino asitlerden daha fazlasını taşır: rijit prolin; tirozin ve triptofan gibi aromatik kalıntılar; ve pozitif yüklü arginin. Aynı zamanda serin, aspartik asit ve glutamik asit kalıntılarından daha az içerir; bu kalıntılar yüksek sıcaklıklarda proteinleri daha savunmasız hale getirebilir. Bu desen yalnızca T7 lizozime karşı değil, aynı zamanda Ts2631’in yüz binlerce viral ve milyonlarca bakteriyel proteinle karşılaştırıldığında da geçerlidir.
Önemlerini test etmek için tek amino asit değiştirmeleri
Korelasyondan nedenselliğe geçmek için ekip, Ts2631’de sistematik olarak 55 tek tek amino asidi değiştirdi ve her bir mutasyonun erime sıcaklığına (Tm) ve enzimin bakteri hücre duvarlarını parçalama yeteneğine nasıl etki ettiğini ölçtü. Çinko içeren aktif bölge çevresindeki bazı değişiklikler özellikle zararlı oldu. Üç çinko-koordine eden kalıntı (H30, H131 ve C139) değiştirildiğinde proteinin Tm’si yaklaşık 20 °C’ye kadar düştü ve aktivite kayboldu. İki korunmuş tirozin (Y60 ve Y69) da kararlılığa katkıda bulundu. Şaşırtıcı şekilde, sisteinler C80 ve C90 arasında bir tür kovalent bağ olan disülfid bağının kaldırılması, aktiviteyi yok etmesine rağmen erime sıcaklığını aslında yükseltti. Bu, deney tüpünde çok kararlı olmanın her zaman bir proteinin gerçek koşullarda daha iyi işlev göreceği anlamına gelmediğini gösterir. 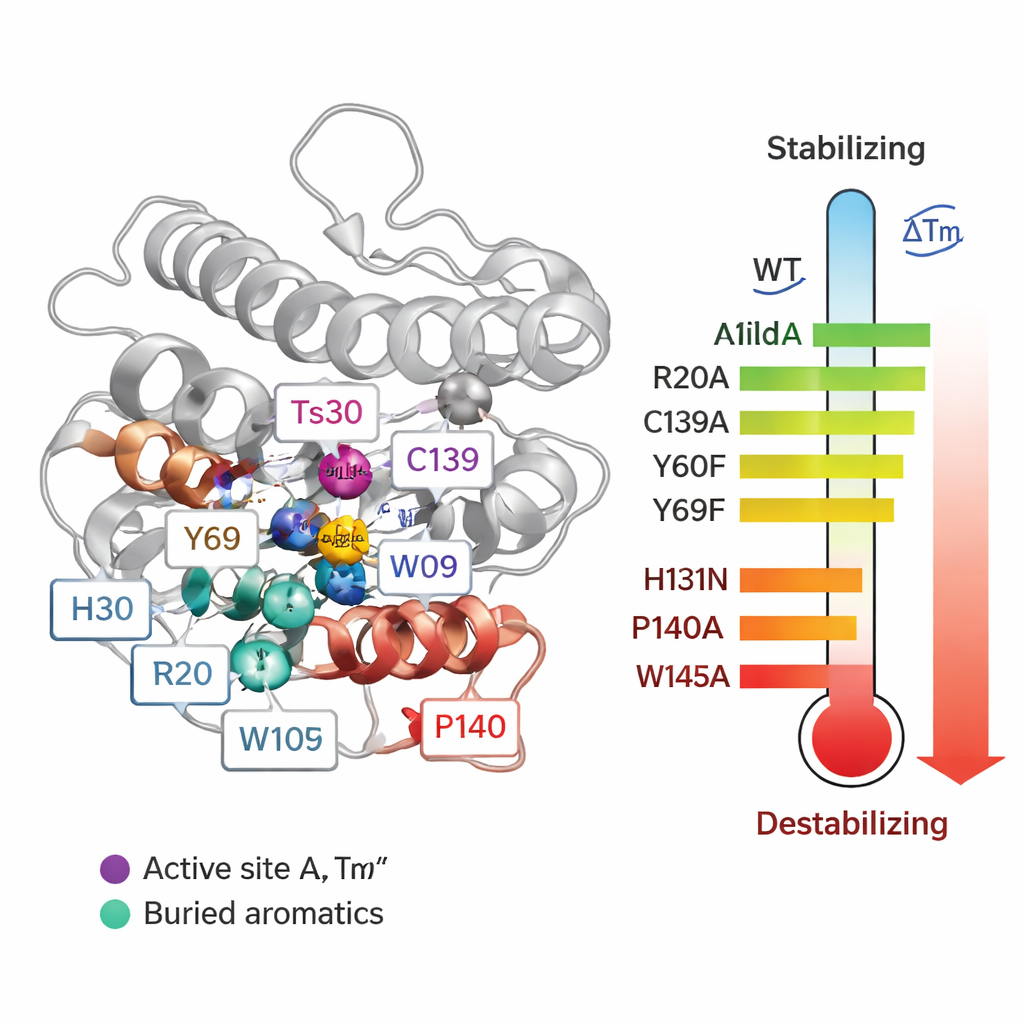
Gizli aromatik “çapa”lar ve bakteriyel duvara kilit bir tutuş
En çarpıcı sonuçlar prolin ve triptofan kalıntılarının mutasyona uğratılmasından geldi. Çinkoya bağlanan C139’un hemen yanına yerleşmiş tek bir prolin (P140) değiştirildiğinde, Tm 21 °C’den fazla düştü ve ısıl işlem sonrası aktivite zayıfladı; çünkü mutasyon, metal bağlanması için gereken özel bağ geometrisini bozdu. Derin gömülü birkaç triptofan (W102, W109 ve özellikle W145) da kritik çıktı: bunların alanine ile değiştirilmesi Tm’de %14–24 aralığında düşüşlere neden oldu ve enzimi ısıl aktivite testlerinde çok daha hassas hale getirdi. Bu aromatik kalıntılar, proteinin çekirdeğini yerinde kilitleyen iç çapa görevi görür. Argininler arasında çoğunun kararlılık üzerinde az etkisi varken, R20 peptidoglikana tutunmak için vazgeçilmez çıktı. R20 değiştirildiğinde enzim bakteri hücre duvarına zayıf bağlandı ve ısıl işlemde aktivitesini kaybetti; bu da bazı kalıntıların salt termal dayanıklılıktan ziyade işlevselliğe daha fazla katkıda bulunduğunu ortaya koyuyor.
Sıcak su kaynaklarından daha sağlam antibakteriyellere
Bir arada ele alındığında, çalışma Ts2631’in olağanüstü ısı direncinin tüm proteinin tek tip bir şekilde güçlendirilmesinden ziyade iyi yerleştirilmiş birkaç amino aside dayandığını gösteriyor. Çinko-bağlayıcı kalıntılar, aktif bölge yakınındaki korunmuş bir prolin ve gömülü aromatik yan zincirler istikrarlı bir çekirdek oluştururken, bazı klasik stabilize edici özellikler —disülfid bağları veya tuz köprüleri gibi— burada beklendiği kadar önemli değil. Daha geniş alan için bu çalışma, mezofilik (orta sıcaklık) endolizinlerin belirli pozisyonlara dikkatlice triptofan veya prolin yerleştirerek antibakteriyel aktiviteyi feda etmeden daha dayanıklı hale getirilebileceğini öneriyor. Başka bir deyişle, doğanın kaynama yakınındaki sıcaklıklara meydan okuyan enzimleri nasıl inşa ettiğini öğrenerek, bilim insanları daha güvenilir, uzun ömürlü protein bazlı antibiyotikler tasarlamak için pratik bir şablon kazanıyor.
Atıf: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
Anahtar kelimeler: termostabil endolizin, bakteriyofaj enzimleri, protein termostabilitesi, antibiyotik direnci, protein mühendisliği