Clear Sky Science · tr
Vasküler düz kas hücrelerinin köpük hücrelerine dönüşümünü homosisteinin tetiklemesine ilişkin biyobelirteçler üzerine çalışma
Tıkalı atardamarlar küçük hücresel değişimlerle nasıl başlar
Ateroskleroz—atardamarların yavaşça tıkanması ve sertleşmesi—kalp krizi ve felçlerin önde gelen nedenlerindendir. Genellikle kolesterol ve diyet konuşulur, ancak hastalık gelişirken damar duvarındaki bireysel hücrelerin nasıl değiştiği daha az ele alınır. Bu çalışma, homosistein adlı bir kan molekülünü yakından inceliyor ve bunun atardamarlardaki normalde uyumlu kas hücrelerini yağ biriktirip sözde köpük hücrelerine dönüştürmeye nasıl itebildiğini gösteriyor; bu hücreler tehlikeli plakların yapıtaşlarıdır.
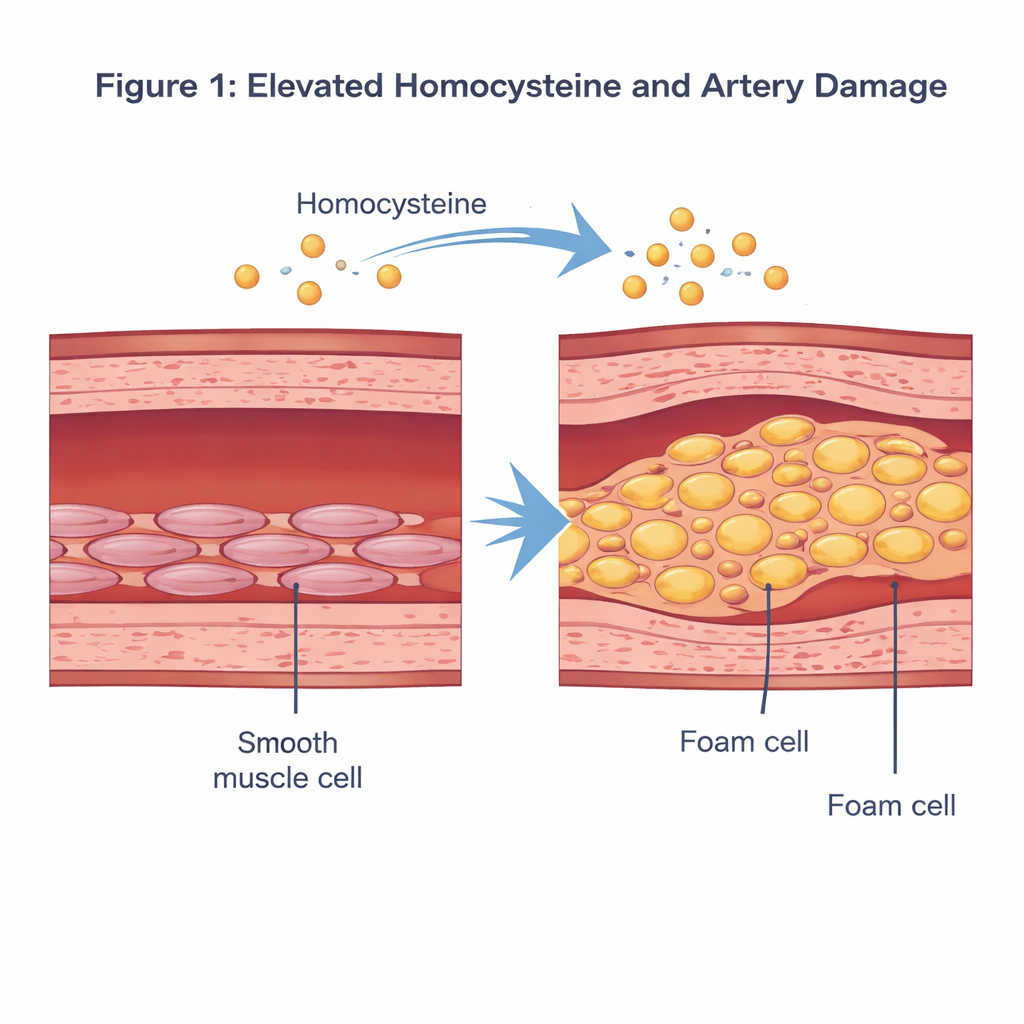
Kan dolaşımındaki kükürt içeren aminoasit sorunu
Homosistein, vücudumuzun diyetle alınan metiyonini işlerken ürettiği kükürt içeren bir aminoasittir. Normal koşullarda kan düzeyi düşüktür. Yaklaşık 15 mikromol/L’nin üzerine çıktığında—hiperhomosisteinemi olarak adlandırılan bir durum—epidemiyolojik çalışmalar bunun kardiyovasküler hastalık riskini artırdığını ilişkilendirmiştir. Önceki araştırmalar aşırı homosisteinin atardamarların iç tabakasına zarar verebileceğini, iltihabı körükleyebileceğini ve damar duvarının orta tabakasında yer alan ve kan basıncını kasılıp gevşeyerek düzenlemeye yardımcı olan vasküler düz kas hücrelerinin davranışını değiştirebileceğini öne sürmüştü.
Atardamar kas hücrelerinin yağ yüklü köpük hücrelere dönüşümü nasıl gerçekleşiyor
Araştırmacılar, homosisteinin bu düz kas hücrelerini nasıl yeniden şekillendirdiğine odaklandı. Laboratuvar ortamında, insan vasküler düz kas hücrelerini hastalığı taklit edecek düzeyde homosisteine maruz bıraktılar ve bunları tedavi edilmeyen hücrelerle karşılaştırdılar. Standart boyalar ve biyokimyasal testler kullanarak, homosistein ile muamele edilen hücrelerin kırmızı renkli yağ damlacıklarıyla dolduğunu ve kolesterol ile trigliserid düzeylerinin keskin şekilde arttığını gözlemlediler. Aynı zamanda, hücrelerin tipik “kasılgan” kimliğinin protein belirteçleri azalırken, daha sentetik ve plak oluşturan bir durumu işaret eden belirteçler arttı. Bir arada ele alındığında, bu değişiklikler homosisteinin düz kas hücrelerini normal rollerinden uzaklaştırıp doğrudan plak oluşumuna katkıda bulunan yağ yüklü, köpük hücre benzeri bir fenotipe doğru sürükleyebileceğini gösteriyor.
Hücre içindeki moleküler parmak izlerini aramak
Bu dönüşüm sırasında hangi proteinlerin değiştiğini anlamak için ekip, aynı anda binlerce proteini ölçebilen modern proteomik yöntemlerine başvurdu. Homosistein ile muamele edilen hücrelerle kontroller arasındaki protein düzeylerini karşılaştırdılar ve neredeyse 4.800 proteini güvenilir şekilde nicelendirildi. Bunların arasında 54 protein anlamlı şekilde öne çıktı: 13’ü artmış, 41’i azalmıştı. Değişime uğrayan birçok protein lipit işleme, hücre sağkalımı, oksidatif stres ve hücresel yapısal yeniden düzenleme ile ilişkiliydi. Yazarlar daha sonra bu proteinleri işlevsel yollar halinde gruplandırmak ve bunların birbirleriyle nasıl etkileşime girdiğini haritalamak için biyoinformatik araçlar kullandı; bu analizler damar duvarında kolesterol metabolizması ve stres yanıtlarıyla bağlantılı ağları vurguladı.
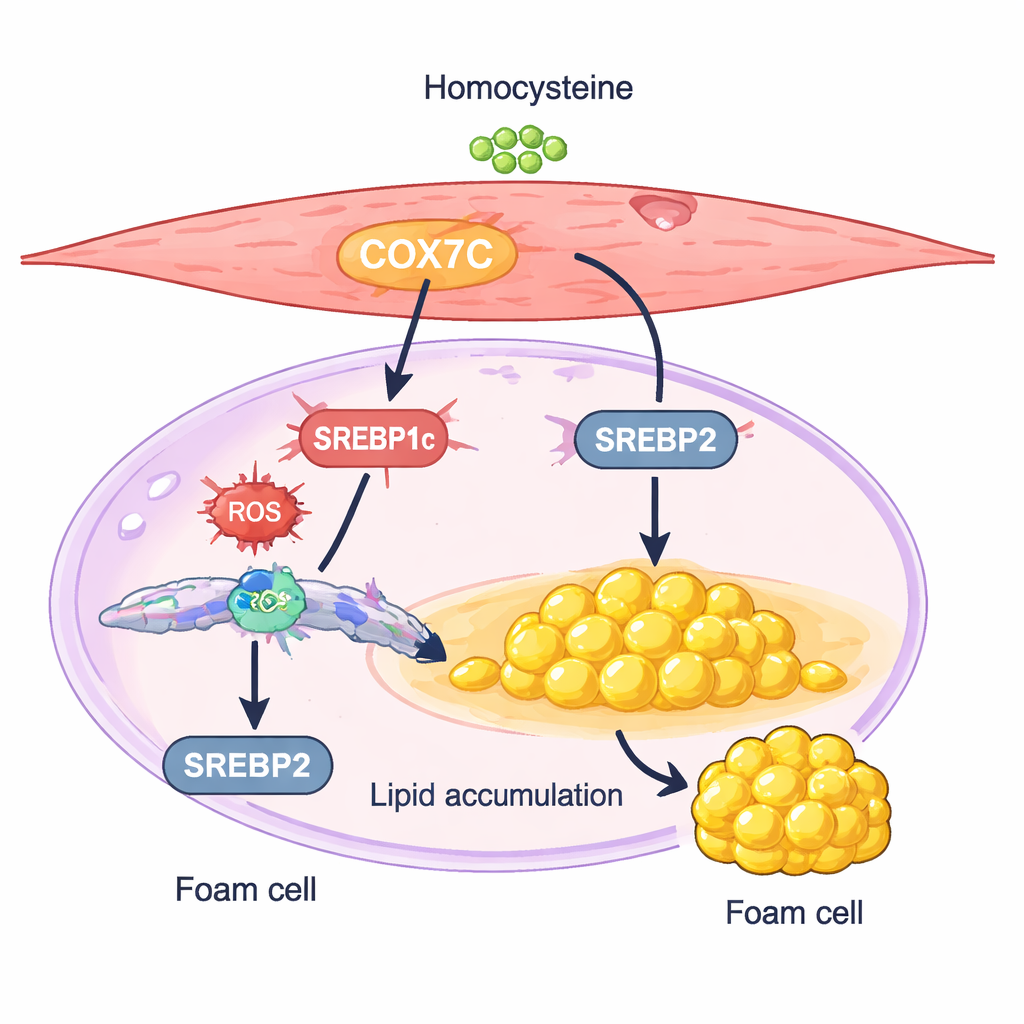
Hücreleri yağ depolamaya iten mitokondriyal anahtar
COX7C adlı bir protein özellikle ilgi çekici bir şüpheli olarak öne çıktı. COX7C, hücrenin enerji üretimini yöneten mitokondrilerinin bir bileşenidir. Homosistein ile muamele edilen düz kas hücrelerinde COX7C düzeyleri kontrollere göre daha yüksekti. Araştırmacılar COX7C’yi daha da artırmanın hücrelerin daha fazla yağ biriktirmesine ve lipit üretiminin iki ana düzenleyicisi olan SREBP1c ile SREBP2’nin daha yüksek düzeyde ifade edilmesine yol açtığını gösterdi. COX7C’nin susturulması ters etki yaptı: SREBP aktivitesini azalttı, kolesterol ve trigliserid birikimini düşürdü ve köpük hücre benzeri değişiklikleri hafifletti. Bu sonuçlar, homosisteinin mitokondride COX7C’yi artırıp hücresel stres sinyallerini yükselttiği ve bunun da SREBP aracılı yağ sentezini etkinleştirerek düz kas hücrelerini lipit biriktiren bir duruma ittiği modelini destekliyor.
Kalp sağlığı ve gelecekteki tedaviler için anlamı
Bu çalışma henüz insan atardamarlarında ne olduğunu kanıtlamıyor ve hasta yerine kültüre edilmiş hücreler üzerinde yapıldı. Yine de yüksek homosisteinin yardımcı atardamar kas hücrelerini zarar verici köpük hücrelerine dönüştürmesine nasıl katkıda bulunabileceğine ayrıntılı bir bakış sunuyor ve COX7C ile ilişkili proteinleri potansiyel biyobelirteçler veya ilaç hedefleri olarak tanımlıyor. Halk için temel mesaj, “iyi” ve “kötü” kolesterolün ötesinde, aşırı homosistein gibi kandaki küçük kimyasal değişimlerin damar duvarını içeriden yeniden programlayabileceğidir. COX7C ve SREBP yolunu gibi moleküler oyuncuları belirleyerek, bu çalışma plaklar oluşmadan önce küçük damar hücrelerinin mini yağ depolarına dönüşmesini engellemeye yönelik gelecek stratejiler için temel oluşturuyor.
Atıf: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
Anahtar kelimeler: ateroskleroz, homosistein, köpük hücreleri, vasküler düz kas hücreleri, COX7C