Clear Sky Science · tr
LncRNA FTX, miR-335-3p’yi süngerleyerek TFEC/ILK sinyalini düzenleyip miyokardiyal fibrozisi teşvik eder
Kalp skarlaşmasının önemi
Kalp yetmezliği dünya genelinde onlarca milyonu etkiler ve genellikle yıllar içinde sessizce ilerler. Bu düşüşün başlıca nedeni miyokardiyal fibrozistir—kalp kasının yavaş, ilerleyici biçimde skar dokusu ile değişmesi; bu durum kalbi daha sert hale getirir ve kan pompalama yeteneğini azaltır. Bu çalışma, kalp hücrelerine fazla skar dokusu üretmeleri talimatını veren moleküler “devreyi” inceliyor ve bu zararlı süreci yavaşlatmak veya tersine çevirmek için hedeflenebilecek yeni bir molekül zinciri tanımlıyor.
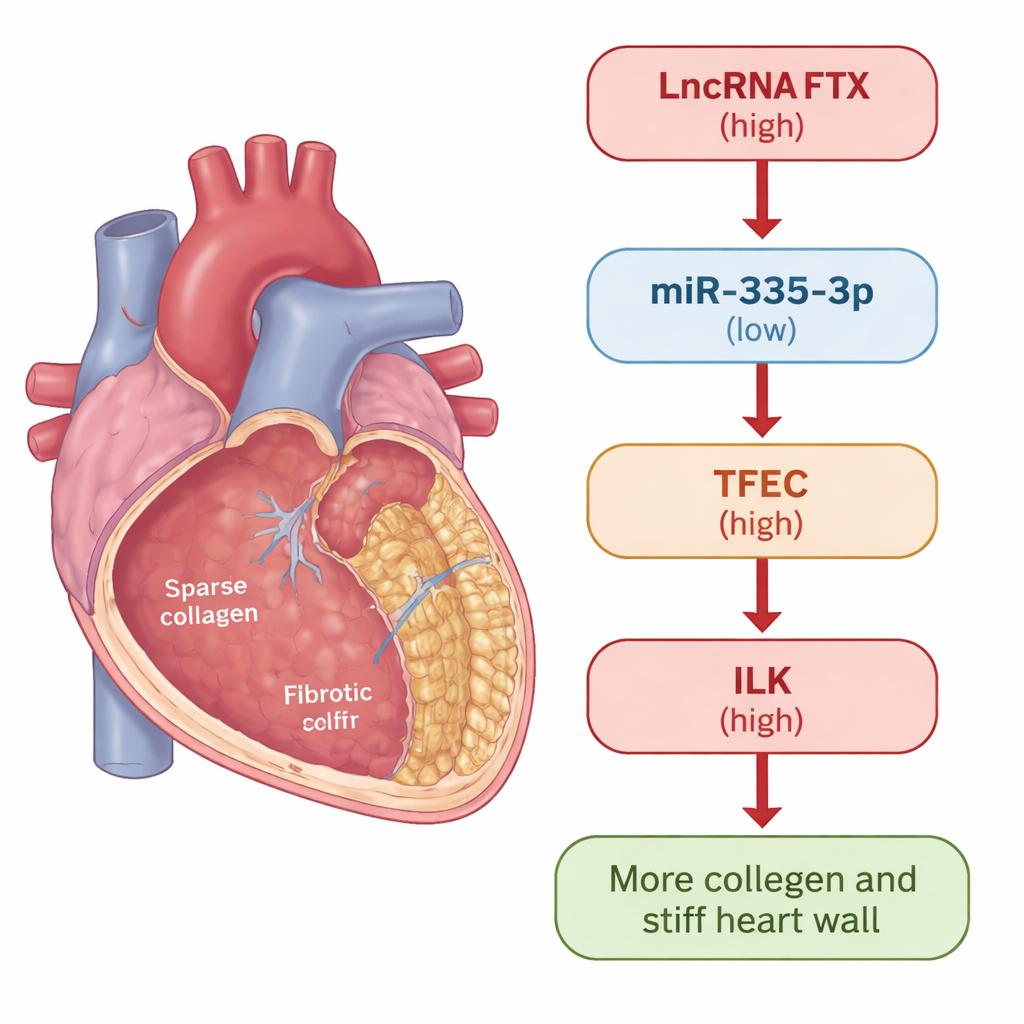
Kalp skarlaşmasına daha yakından bakış
Kalp yaralandığında veya strese girdiğinde, kardiyak fibroblast adı verilen destek hücreleri harekete geçer. Sağlıklı onarımda hasarı yamalarlar. Ancak kronik hastalıkta aşırı aktif bir duruma geçip fazla kollajen ve ekstracellular matriks bileşenleri üretirler, bu da zamanla kalp duvarını sertleştirir. Araştırmacılar bu süreci incelemek için iki model kullandılar: kalp fibrozisini güvenilir şekilde indükleyen isoproterenol verilen fareler ve skar oluşumunun bilinen tetikleyicilerinden TGF-β1’e maruz bırakılmış insan kardiyak fibroblastları. Her iki durumda da fibrozis gelişirken belirli gen ve proteinlerin nasıl değiştiğini ölçtüler.
Hücre içindeki zararlı zincirleme reaksiyon
Ekip, çekirdekte yer alan ve diğer genleri açan bir transkripsiyon faktörü olan TFEC’e odaklandı. TFEC’in, integrin-bağlı kinaz (ILK) adlı başka bir proteinle birlikte, fibroblastlar fibrotik, skar oluşturucu bir duruma itildiğinde sürekli olarak arttığını buldular. TFEC veya ILK susturulduğunda α-düz kas aktini ve kollajen I ile III gibi klasik fibrozis belirteçleri belirgin şekilde azaldı; ayrıca doku skarlaşmasını teşvik ettiği bilinen Akt/GSK3β ve Hippo gibi büyüme-kontrol yolları baskılandı. DNA bağlanma haritalama deneyleri TFEC’in ILK geninin promotörüne doğrudan bağlandığını ve onun aktivitesini artırdığını gösterdi; bu da TFEC’i pro-fibrozis sinyal kaskadında ILK’in açıkça üstünde konumlandırdı.
Usta düzenleyiciyi kontrol eden RNA anahtarları
TFEC’i neyin kontrol ettiğini anlamak için araştırmacılar protein üretmeyen ancak gen aktivitesinin ince ayarını yapan kodlamayan RNA’lara yöneldiler. Fibrotik kalplerde ve hücrelerde azalmış olan küçük bir RNA, miR‑335‑3p’yi tespit ettiler. miR‑335‑3p düzeylerini yükseltmek TFEC’i düşürürken, engellemek TFEC’i artırdı; raporör testleri miR‑335‑3p’nin TFEC mesajlarına doğrudan bağlanıp onları kontrol altında tuttuğunu doğruladı. Ardından fibroziste yükselmiş ve fiziksel olarak miR‑335‑3p ile etkileşen uzun bir kodlamayan RNA olan FTX’i buldular. FTX moleküler bir sünger gibi davrandı: miR‑335‑3p’yi bağlayıp onu TFEC’i sınırlamaktan alıkoydu. Sonuç olarak TFEC ve ILK arttı ve fibroblastlar daha fazla skar oluşturan kollajen üretti.
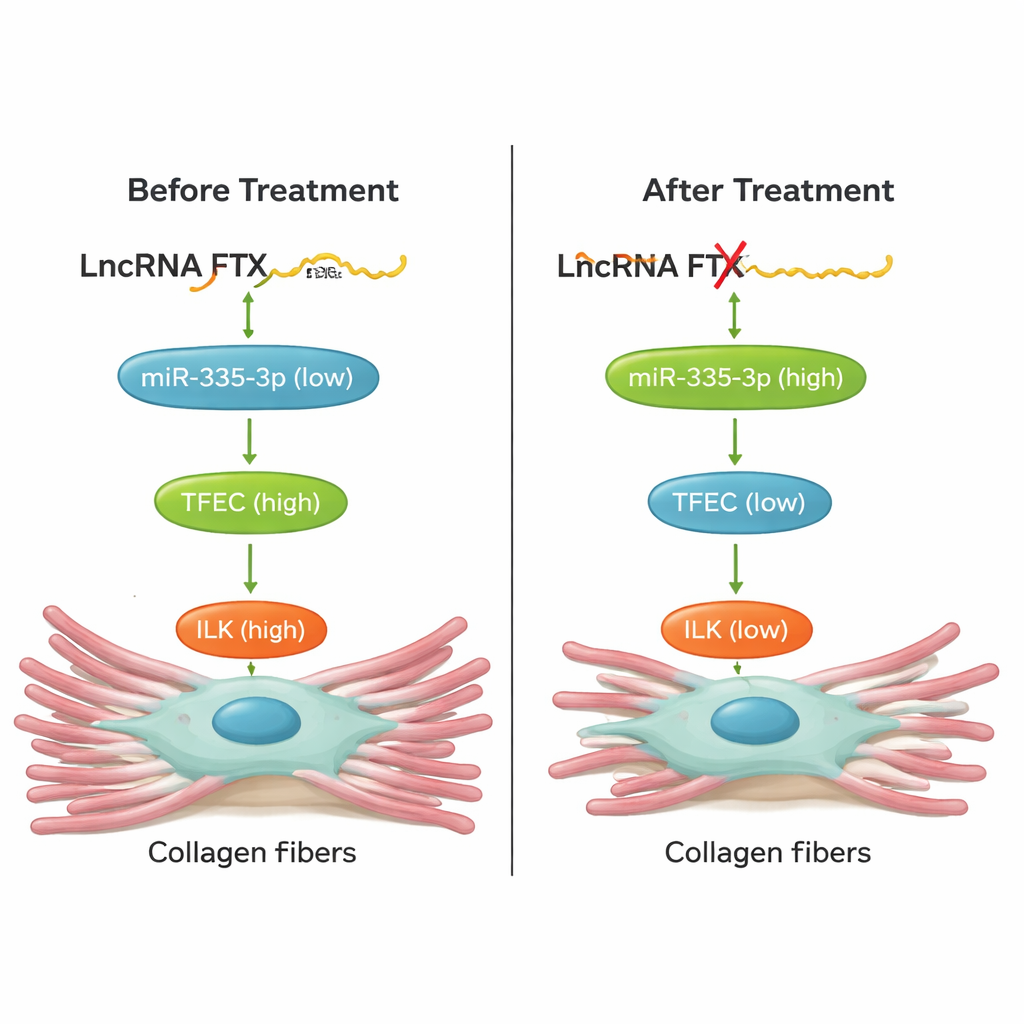
Hücre kültüründen canlı kalplere
Hayati olarak, ekip bu zinciri bozmanın hayvanların kalplerini gerçekten koruyup koruyamayacağını test etti. İsoproterenole maruz kalan farelerde TFEC’i düşürmek, AAV9 gen terapisi vektörü ile kalpte FTX’i sessize almak veya kimyasal olarak stabilize edilmiş bir “agomir” ile miR‑335‑3p’yi yükseltmek; kalp dokusunda daha az kollajen birikmesine ve fibrozis belirteçlerinde düşüşe yol açtı. Bu müdahaleler ayrıca kalp fonksiyonunu iyileştirdi: strok hacmi ve ejeksiyon fraksiyonu normale doğru hareket etti ve kalp hızındaki zararlı artışlar azaltıldı. Hücrelerde yapılan kurtarma deneyleri, FTX/miR‑335‑3p/TFEC/ILK ekseninin bir bileşenindeki değişikliğin diğerlerini öngörülebilir şekilde kaydırdığını göstererek bunun gevşek bir korelasyon değil, sıkı bağlı bir yolak olduğunu teyit etti.
Gelecekteki tedaviler için anlamı
Uzman olmayan biri için çıkarılacak mesaj, yazarların kalp skarlaşması için yeni bir “kontrol kolu” tespit etmiş olmalarıdır. FTX adlı uzun bir RNA, bir ana anahtarı (TFEC) frenleyen miR‑335‑3p’yi etkisiz kılar; TFEC bunun ardından ILK ve aşağı yönlü pro-skarlaşma sinyallerini açar, aşırı kollajen birikimini ve kalbin sertleşmesini tetikler. FTX’i azaltmak, miR‑335‑3p’yi eski haline getirmek veya doğrudan TFEC’i engellemek farelerde skarlaşmayı azaltıp pompalama fonksiyonunu iyileştirebildi. Bu yolun insan hastalarda doğrulanması ve güvenli terapilerin geliştirilmesi için daha fazla çalışma gerekli olmakla birlikte, RNA tabanlı bu düzenleyici zincir fibrozise bağlı kalp yetmezliğinde müdahale edilebilecek birkaç umut verici hedef sunuyor.
Atıf: Yao, F., He, Z., Zheng, C. et al. LncRNA FTX promotes myocardial fibrosis by sponging miR-335-3p to regulate TFEC/ILK signaling. Sci Rep 16, 7340 (2026). https://doi.org/10.1038/s41598-026-38615-3
Anahtar kelimeler: miyokardiyal fibrozis, kalp yetmezliği, kodlamayan RNA, kardiyak fibroblastlar, fibrozis sinyalleşmesi