Clear Sky Science · tr
Aktiveleşmiş T hücreleri, TRPV4 aracılı kalsiyum akışı yoluyla A549 akciğer adenokarsinom hücrelerinde apoptozu indükler
Bu araştırma akciğer kanseri için neden önemli
Akciğer kanseri, kısmen tümörlerin kemoterapi ve radyasyon gibi standart tedavilere direnç geliştirmesi nedeniyle hâlâ en ölümcül kanserlerden biridir. Son yıllarda vücudun kendi bağışıklık sisteminden yararlanmak yeni umutlar sundu. Bu çalışma, bu fikre yeni bir boyut kazandırıyor: aktive edilmiş bir T hücresi türünün, TRPV4 olarak bilinen moleküler bir “kapı”dan kalsiyum içeri alınmasını zorlayarak akciğer kanseri hücrelerini kendi kendine yok olmaya ittiğini gösteriyor. Bu yolun anlaşılması, bilim insanlarının daha güçlü ve hassas immünoterapiler tasarlamasına yardımcı olabilir.
Bağışıklık sisteminin askerleri ile akciğer tümör hücreleri karşılaşıyor
Araştırmacılar, A549 olarak bilinen insan akciğer adenokarsinomu hücrelerine odaklandı; bunlar küçük hücre dışı akciğer kanserinin yaygın kullanılan bir modelidir. Bu kanser hücrelerini, vücudun öldürücü T hücrelerinin yerini alan Jurkat T hücreleriyle eşleştirdiler; bu hücreler normalde enfekte veya kötü huylu hücreleri arayıp yok eder. Jurkat hücrelerini kimyasal olarak aktive ederek ekip, gerçek bir bağışıklık yanıtında son derece tetikte olan T hücrelerinin durumunu taklit etti. Ardından aktive edilmiş veya pasif T hücrelerini farklı oranlarda akciğer kanser hücreleriyle karıştırıp bir ila üç gün boyunca neler olduğunu izlediler; özellikle kaç kanser hücresinin hayatta kaldığı ve kaçının programlanmış hücre ölümü (apoptoz) geçirdiğine dikkat ettiler.
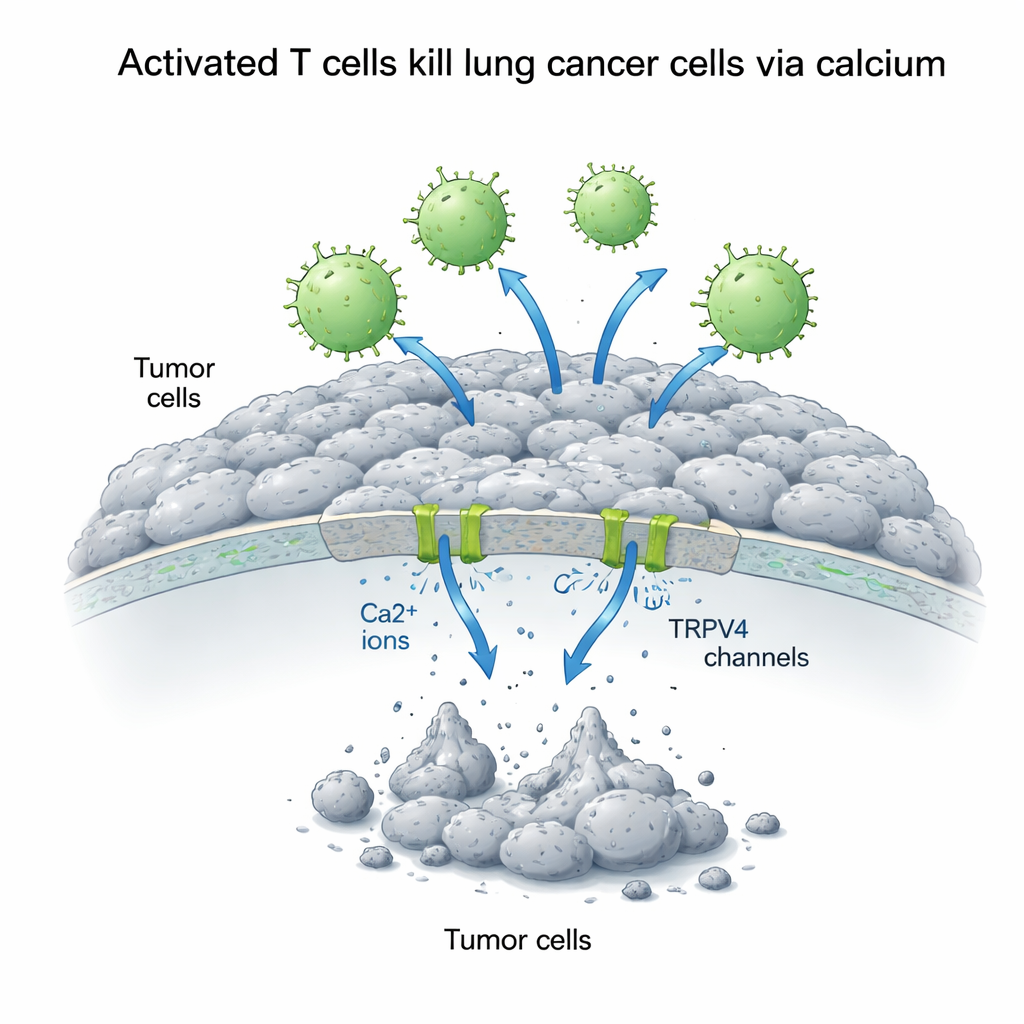
Kalsiyum: kanser hücreleri için çift taraflı bir sinyal
Hücre içi kalsiyum, nasıl işlendiğine bağlı olarak ya büyümeyi destekleyen ya da ölümü tetikleyen çok yönlü bir sinyal anahtarı gibi davranır. Bilim insanları A549 hücrelerinin dışındaki kalsiyum miktarını artırdı ve bunun T hücreleri ile tümör hücreleri arasındaki mücadeleyi nasıl etkilediğini ölçtü. Sürpriz bir şekilde, yalnızca ek kalsiyum akciğer kanseri hücrelerinin daha iyi büyümesini sağladı; bu, sakin koşullarda kalsiyumun hayatta kalma yolaklarını beslediğini düşündürüyor. Ancak aktive T hücreleri var olduğunda durum tersine döndü: daha yüksek dış kalsiyum, T hücresi kaynaklı öldürmeyi dramatik şekilde güçlendirdi. 72 saat içinde, hem aktive T hücreleri hem de ekstra kalsiyum bir arada olduğunda kanser hücresi sağkalımı normalin üçte birinden daha azına düştü; oysa pasif T hücrelerinin etkisi azdı ve kalsiyum eklendiğinde büyümeyi bile destekleyebiliyordu.
Stres ve hücre ölümüyle bağlantılı bir kalsiyum “kapısı”
Bu büyümeden ölüme geçişin nasıl gerçekleştiğini anlamak için ekip, hücre zarında kalsiyumun içeri akmasına izin veren bir protein kanalı olan TRPV4’e baktı. Protein analizleri kullanılarak, A549 hücreleri ek kalsiyuma maruz kaldığında TRPV4 düzeylerinin belirgin şekilde yükseldiği; T hücreleri olsun ya da olmasın bu artışın görüldüğü ve en yüksek düzeyin kalsiyum ile aktive T hücrelerinin birlikte olduğu durumda saptandığı bulundu. Aynı zamanda kanser hücreleri açıkça oksidatif stres işaretleri gösterdi: koruyucu antioksidanlar aleyhine denge kaydı (düşük toplam antioksidan kapasite) ve zararlı oksidanlar lehine bir artış oldu (yüksek toplam oksidan düzeyi). Hücreleri floresan boyalarla işaretleyen bir teknik olan akış sitometrisi, aktive T hücrelerinin özellikle kalsiyum bol olduğunda hem erken hem de geç apoptoz aşamalarında artışa neden olduğunu doğruladı. Bu gözlemler bir araya geldiğinde, TRPV4 kanallarının daha fazla kalsiyum alınmasına izin verdiği, bunun hücre içinde kimyasal strese yol açtığı ve hücreyi ölüm yönüne ittiği bir olay zincirini işaret ediyor.
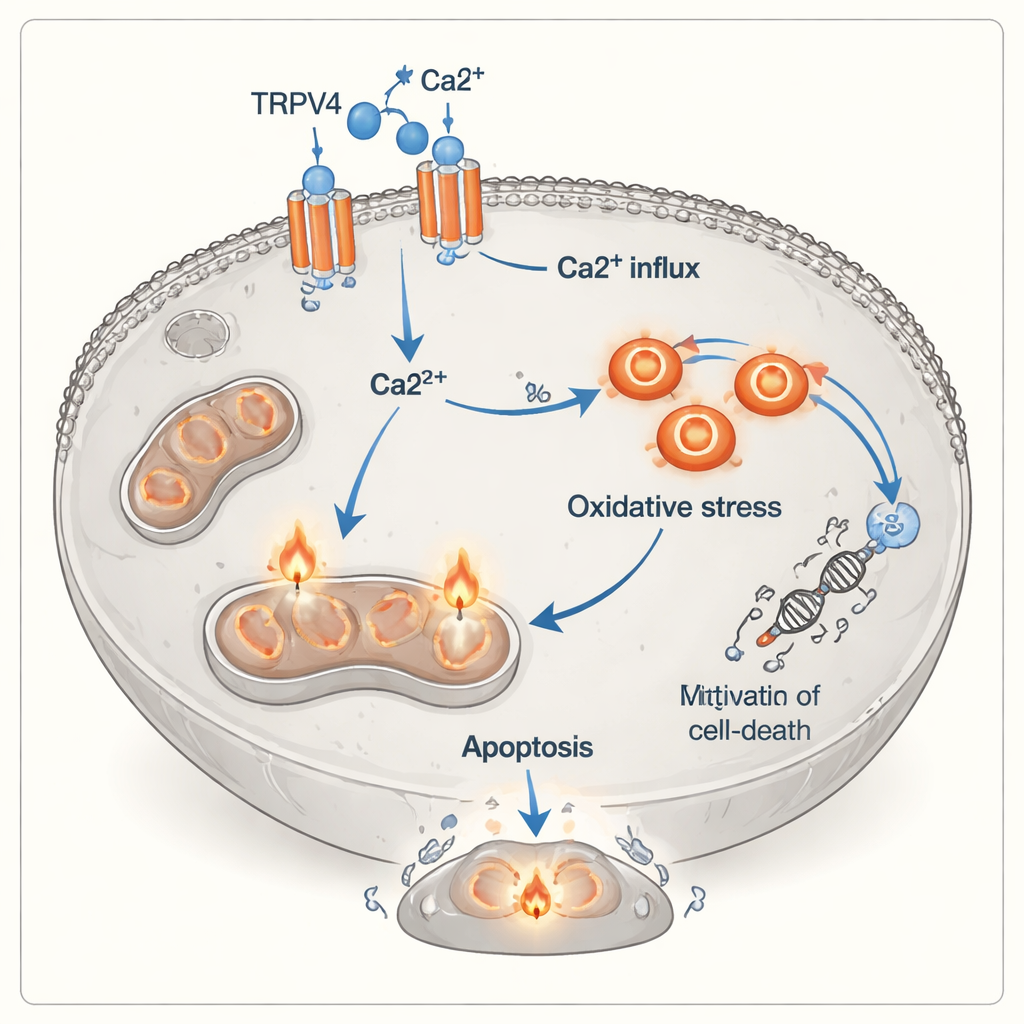
Bağışıklık hücrelerinin tümörleri öldürme biçimine yeni bir katman
Klasik olarak, öldürücü T hücreleri hedeflerini toksik proteinler salgılayarak veya kanser hücresi yüzeyindeki ölüm reseptörlerini tetikleyerek yok eder. Bu çalışma, daha dolaylı bir yol olduğunu öne sürüyor: aktive T hücrelerinden gelen sinyaller—iltihap yapıcı moleküller ve yakın hücre-hücre teması dahil—akciğer kanseri hücrelerini TRPV4’e daha bağımlı ve kalsiyum yüklenmesine ve oksidatif hasara karşı daha savunmasız hale getiriyor gibi görünüyor. Bu bakış açısında TRPV4, aksi takdirde büyümeyi teşvik eden kalsiyumu öldürücü bir sinyale çeviren duyarlılığı artıran bir anahtar görevi görüyor. Deneyler kaplarda ve tek bir kanser hücre hattı kullanılarak yapılmış olsa da, bunlar bağışıklık saldırısı, iyon kanalları ve tümör hücrelerinin iç stres mekanizmaları arasında potansiyel olarak önemli bir köprüyü vurguluyor.
Gelecekteki tedaviler için anlamı
Uzman olmayanlar için çıkarım, immünoterapinin başarısının sadece T hücrelerini güçlendirmeye değil, aynı zamanda kanser hücrelerini öldürmeyi kolaylaştırmaya da bağlı olabileceğidir. TRPV4 veya ilgili kalsiyum kanallarını hedefleyerek, klinisyenler bir gün T hücrelerinin akciğer tümörlerini yok etme yeteneğini artırabilir veya sağlıklı dokulara zarar vermeyi önleyecek şekilde tedavileri hassaslaştırabilir. Bu çalışma hâlâ erken aşamada ve yazarlar hayvanlarda ve daha karmaşık modellerde ek deneylere duyulan ihtiyacı vurguluyor. Yine de, TRPV4–kalsiyum–oksidatif stres ekseninin keşfi, akciğer kanserine karşı bağışıklığa dayalı tedavileri geliştirmek için umut verici yeni bir hedef ekliyor.
Atıf: Alavi, F., Kazemi-Lomedasht, F., Eftekhari, Z. et al. Activated T cells induce apoptosis in A549 lung adenocarcinoma cells via TRPV4-mediated calcium influx. Sci Rep 16, 7155 (2026). https://doi.org/10.1038/s41598-026-38589-2
Anahtar kelimeler: akciğer kanseri immünoterapisi, T hücreleri, kalsiyum sinyalleşmesi, TRPV4 kanalı, oksidatif stres