Clear Sky Science · tr
Hidroksamat olmayan [1,2,4]triazolo[4,3-a]kinolin bileşikleri ile hedeflenmiş HDAC8 inhibisyonu
Çocukluk Çağı Kanseri İçin Yeni Umut
Nöroblastom, sinir hücrelerinden kaynaklanan ve yayıldıktan sonra sıklıkla tedavi edilmesi güç olan agresif bir çocukluk çaresidir. Bu çalışma, HDAC8 adlı hücresel bir anahtarın kapatılması yoluyla nöroblastom hücrelerini yavaşlatma veya öldürme konusunda yeni bir yaklaşımı araştırıyor. Anahtara çok seçici şekilde etki eden yeni bir ilaç benzeri molekül ailesi geliştirerek araştırmacılar, tümörlere karşı daha etkili ve vücuda karşı daha nazik tedaviler yaratmayı hedefliyor.
Kanserin Kalbindeki Moleküler Bir Anahtar
Hücrelerimizde genler sürekli olarak açılıp kapanır. Bu kontrol sistemlerinden biri, DNA ile ilişkili proteinlere bağlanan asetil grupları adı verilen küçük kimyasal etiketlere dayanır. Histon deasetilazlar (HDAC'lar) adı verilen enzimler bu etiketleri uzaklaştırır, DNA paketlenmesini sıkılaştırır ve gen aktivitesini genellikle azaltır. HDAC8, bu enzim ailesinin bir üyesidir ve nöroblastom da dahil olmak üzere çeşitli kanserlerle ilişkilendirilmiştir. HDAC8 aşırı aktif olduğunda, kanser hücreleri daha kolay büyüyebilir, hayatta kalabilir ve yayılabilir; bu da onu yeni ilaçlar için çekici bir hedef haline getirir.
Eski HDAC İlaçlarının Sınırlamaları
Bazı kan kanserleri için hâlihazırda onaylanmış birkaç HDAC engelleyici ilaç vardır, ancak bunlar genellikle birçok HDAC türünü aynı anda hedef alır. Bu ilaçların çoğu, enzimin aktif bölgesindeki bir metal iyonuna tutunmak için bir hidroksamat kimyasal grubu kullanır. Etkili olmasına rağmen bu grup metallere çok güçlü bağlandığı için yan etkilere yol açabilir ve ilacın farklı HDAC'ları ayırt etme hassasiyetini sınırlar. Sonuç olarak hastalarda toksisite görülebilir ve sağlıklı hücreler kanser hücreleriyle birlikte zarar görebilir. Bu yüzden araştırmacılar, kanserle savaşan faydaları korurken istenmeyen zararları azaltacak alternatif kimyasal tasarımlar aramaktadır.
Hedefe Yönelik Yeni Bir İnhibitör Sınıfı Tasarlamak
Bu çalışmada ekip, triazoloquinoline iskeleti etrafında inşa edilmiş 21 yeni bileşiği sentezledi; bu iskelet esnek bir bağlantı aracılığıyla HDAC8’in aktif bölgesindeki çinkon atomuna bağlanabilen bir “α-amino amid” bölgesine bağlanıyor. Bilgisayar yönlendirmeli tasarım kullanılarak bu mimari, HDAC8’e özgü dar bir “asetat salım kanalı”na uyacak şekilde seçildi; bu yapısal özellik yüksek özgüllüğe ulaşmaya yardımcı olur. Detaylı yerleştirme çalışmaları ve moleküler dinamik simülasyonlar, özellikle 9m ve 9r adlı yeni moleküllerin HDAC8 cebinde kararlı, uzun süreli etkileşimler oluşturduğunu ve iyi bilinen bir referans inhibitör kadar ya da daha güçlü bir şekilde bağlandığını gösterdi. Önemli olarak, biyokimyasal testler en iyi bileşiklerin diğer HDAC aile üyelerine büyük ölçüde dokunmadan HDAC8’i güçlü şekilde engellediğini doğruladı.
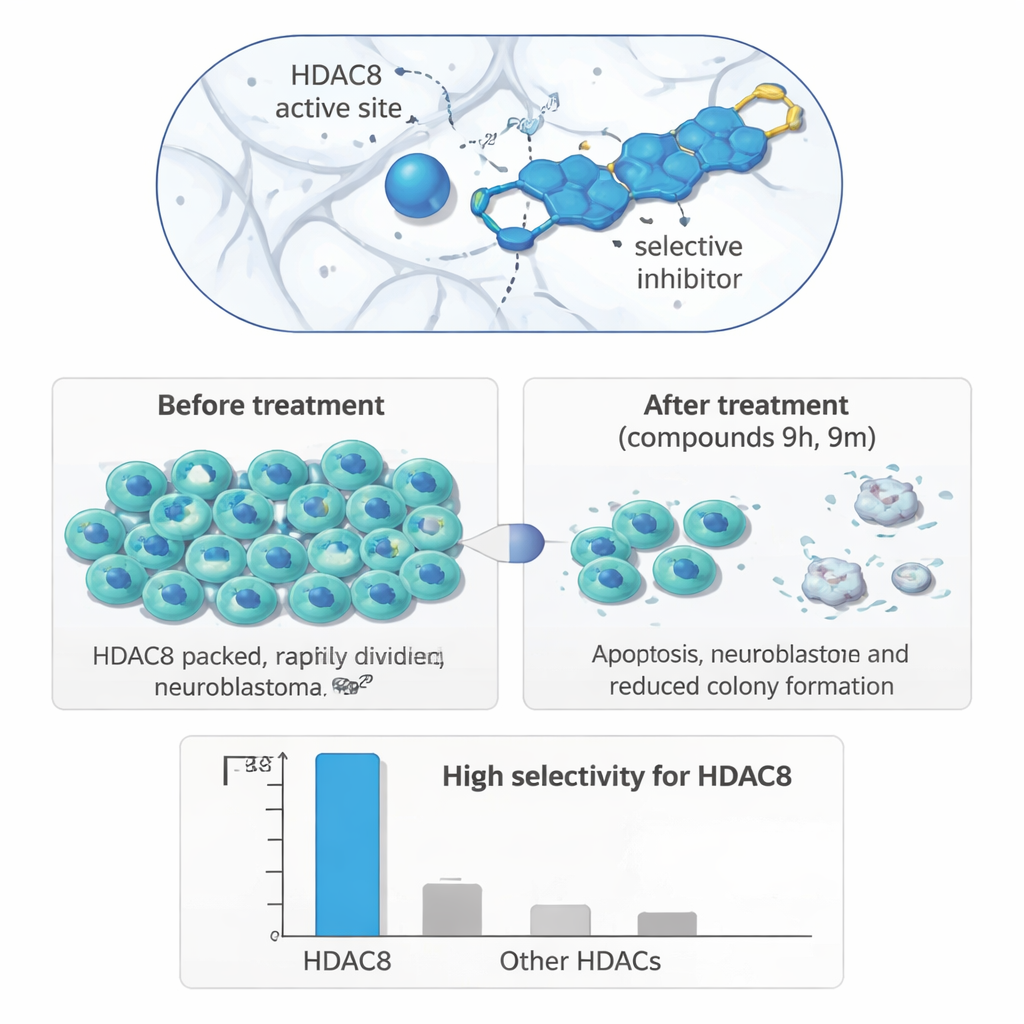
Test Tüpünden Tümör Hücrelerine
Bu hassas enzim hedeflemesinin faydalı biyolojik etkilere dönüşüp dönüşmediğini görmek için araştırmacılar bileşiklerini insan hücre hattı panelinde test ettiler. Nöroblastom hücrelerinde (IMR‑32), iki molekül olan 9h ve 9m öne çıktı: mikromolar konsantrasyonlarda hücre büyümesini azalttılar ve bu etki meme veya kolon kanseri hücrelerine ya da kanser olmayan böbrek hücrelerine göre nöroblastomda daha belirgindi. Uzun süreli koloni oluşum deneyleri, tedavi edilen nöroblastom hücrelerinin ilaç maruziyetinden sonra tekrar çoğalma yeteneklerini büyük ölçüde kaybettiklerini gösterdi. Bir yara kapatma (wound‑healing) testinde, hücre katmanındaki bir çizik kapanırken hücrelerin göç etme hızını izleyen deneyde, her iki bileşik de nöroblastom hücrelerinin hareketini yavaşlatarak metastatik potansiyelde azalma olabileceğine işaret etti.
Bileşiklerin Kanser Hücrelerini Nasıl Öldürdüğünü İncelemek
Akım sitometrisi deneyleri, 9h ve 9m’nin nöroblastom hücrelerinde programlanmış hücre ölümü (apoptoz) tetiklediğini ve DNA hasarı veya ölüme bağlı bir hücre döngüsü fazı olan Sub‑G1’de hücre birikimine neden olduğunu ortaya koydu. Bu etkilerin gerçekten HDAC8 bloke edilmesinden kaynaklandığını doğrulamak için ekip, kardeş kromozomların bölünme sırasında birlikte tutulmasında rol oynayan bilinen bir HDAC8 hedefi olan SMC3 adlı proteinin asetilasyon durumunu ölçtü. HDAC8 engellendiğinde asetile SMC3 birikir. 9h veya 9m ile tedavi sonrası asetile SMC3 seviyeleri keskin şekilde yükseldi, oysa toplam SMC3 proteini değişmeden kaldı—bu, bu bileşiklerin canlı hücrelerde doğrudan HDAC8’i hedeflediğine ve kromozom kontrolündeki normal işlevini bozduğuna dair güçlü kanıttır.
Gelecekteki Tedaviler İçin Anlamı
Kimya, bilgisayar modellemesi, enzim testleri ve hücre tabanlı deneyler birlikte tutarlı bir tablo çiziyor: yeni geliştirilen triazoloquinoline bileşikleri, nöroblastom hücrelerinin büyümesini ve yayılmasını sınırlayabilen, güçlü ve yüksek derecede seçici HDAC8 bloklayıcılarıdır ve diğer HDAC enzimlerini büyük ölçüde etkilemezler. Geleneksel hidroksamat grubundan kaçındıkları için, HDAC8’i terapötik hedef olarak kullanmanın daha güvenli bir yolunu sunabilirler. Ancak yapılması gereken çok iş var—özellikle hayvan çalışmaları ve nihai klinik denemeler—bu araştırma çocukluk çağı nöroblastomu ve muhtemelen HDAC8 kaynaklı diğer hastalıklar için daha hassas ilaçlar geliştirmek adına sağlam bir temel oluşturuyor.
Atıf: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
Anahtar kelimeler: HDAC8 inhibitörleri, nöroblastom, epigenetik tedavi, triazolokinolin, hedefe yönelik kanser ilaçları