Clear Sky Science · tr
İnsan iPSC kaynaklı nöronlarda GluN2A aracılı akımlar ve kalsiyum sinyali
Neden küçük laboratuvarda yetiştirilen beyin hücreleri önemli?
Bilim insanları, beynimizin nasıl geliştiğini incelemek ve otizm, epilepsi ve Alzheimer gibi durumlarda nelerin yanlış gittiğini araştırmak için giderek daha fazla laboratuvarda yetiştirilen insan beyin hücrelerine yöneliyor. Bu çalışma basit ama hayati bir soruyu soruyor: bu laboratuvarda üretilen nöronlar, özellikle glutatamat adı verilen ana kimyasal sinyalle başa çıkma biçimleri bakımından, gerçekten insan beynine benzer şekilde olgunlaşıp bağlantı kuruyor mu? Yanıt, daha gerçekçi “mini-beyin” modelleri oluşturmanın yollarını açıyor ve beyin sağlığı ile hastalığını incelemek için yeni yaklaşımlara işaret ediyor.
Yeniden programlanmış hücrelerden nöron inşası
Araştırmacılar insan indüklenmiş pluripotent kök hücreleriyle başladı—sıradan hücrelerin kök hücre durumuna “yeniden programlandığı” hücreler. Buradan, hücreleri sinir öncül hücrelere ve nihayetinde nöronlar ile destekleyici astrositlerden oluşan ağlara yönlendirdiler; bu, gelişen insan korteksini taklit ediyor. İki yaygın olarak kullanılan kültür koşulunu karşılaştırdılar. Birincisi, BrainPhys adlı ortam, aktif, elektriksel olarak yanıt veren nöronları teşvik edecek şekilde tasarlanmış olup daha fazla astrosit üretme eğilimindedir. Diğeri ise daha geleneksel bir sinir bakım ortamı olup daha az astrosit içeren nöronları tercih eder. Altmış gün boyunca ekip, bu kültürlerin görünüm, gen etkinliği ve hücre tipleri açısından nasıl değiştiğini izledi ve BrainPhys’te yetişen kültürlerin daha karmaşık nöron biçimleri ve gerçek insan beynine daha yakın bir nöron–astrosit oranı geliştirdiğini buldu.
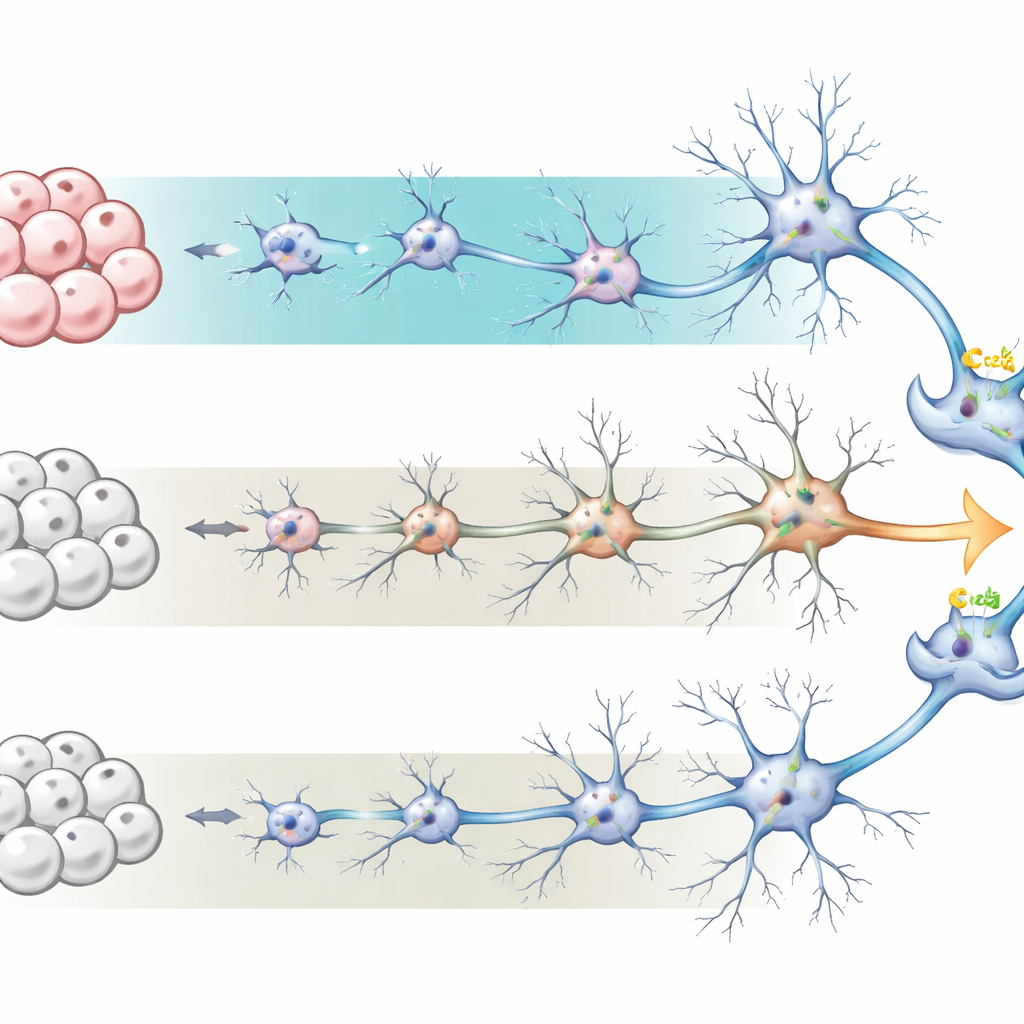
Hücrelerin olgunlaştığının işaretleri
Nöronların ne kadar “olgun” olduğunu görmek için ekip, gün 60’ta RNA dizileme ile küresel gen etkinliğini ölçtü. BrainPhys’te büyütülen hücreler, standart ortama kıyasla neredeyse iki bin gende farklı ifade düzeyi gösterdi; bunların birçoğu nöron farklılaşması, sinaps oluşumu ve elektriksel aktivite ile ilişkilendiriliyordu. Astrosit işlevi ve iltihapla ilişkili genler de daha yüksek bulundu; bu da daha büyük astrosit popülasyonunu yansıtıyordu. Bu desenler birlikte, BrainPhys kültürlerinin nöronlar arasındaki iletişim noktalarının daha rafine olduğu ve destekleyici ortamın canlı dokuya daha yakın olduğu gelişimsel beyin evrelerini daha iyi yeniden oluşturduğunu gösteriyor.
Kimyasal iletişimdeki kilit anahtarlar
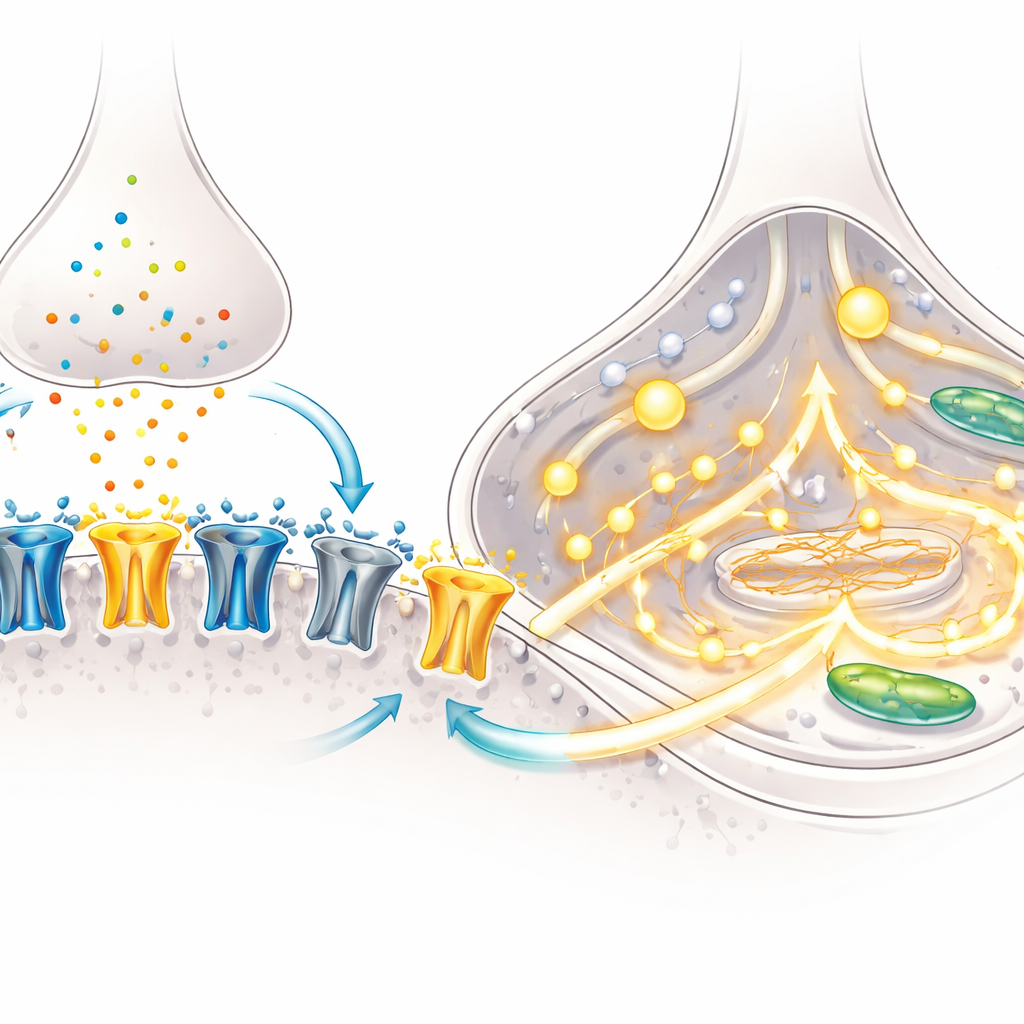
Beyin olgunlaşmasının ayırt edici özelliklerinden biri, NMDA reseptörlerinin bileşiminin değişmesidir—nöronlardaki, glutatamata yanıt olarak açılan ve öğrenmeyle ilişkili bağlantıların kurulmasına yardımcı olan moleküler kapılar. Gelişimin erken döneminde GluN2B adlı alt birim baskınken; daha sonra GluN2A devreye girer ve reseptörlerin ne kadar süre ve ne kadar güçlü açık kaldığını değiştirir. Mikroskopi kullanarak ekip, zamanla daha fazla NMDA reseptörünün özellikle BrainPhys kültürlerinde nöronlar arası temas noktalarına, yani sinapslara yerleştiğini gösterdi. Hedefli gen ölçümleri, “erken” GluN2B alt biriminde bir azalma ve “daha sonra” GluN2A alt biriminde bir artış olduğunu ortaya koydu; bu da nöronların klasik gelişimsel anahtarı geçirdiğine işaret ediyor.
Hücre içindeki akımların ve kalsiyumun izlenmesi
Fonksiyonel testler, bu moleküler değişimlerin önemli olduğunu doğruladı. İnce uçlu elektrotlarla araştırmacılar, NMDA tarafından tetiklenen elektrik akımlarını kaydetti; NMDA, NMDA reseptörlerini seçici olarak aktive eden bir ajandır. Her iki kültür yönteminden nöronlar da güçlü akımlar gösterdi, ancak GluN2A alt birimini bloke etmek bu akımları yaklaşık yarıya indirdi; bu da GluN2A’nın artık sinyal akışında önemli bir rol oynadığını gösteriyor. Ekip ayrıca floresan bir boya kullanarak kalsiyumu, hücre içi önemli bir haberciyi takip etti. NMDA’ya maruz kaldığında, BrainPhys’te yetişen nöronların çok daha büyük bir kısmı güçlü kalsiyum dalgalanmaları gösterdi ve sinyalin büyüklüğü daha fazlaydı. Gen analizi bunun nedenini açıkladı: BrainPhys kültürleri, kalsiyum kanalları ve salım yollarının çok sayıda bileşenini yukarı düzenleyerek hücreleri NMDA reseptör aktivasyonunu geniş, koordineli kalsiyum sinyallerine dönüştürmeye daha hazırlıklı hale getiriyordu.
Beyin bozukluklarını çalışmak için ne anlama geliyor?
Bu bulgular, insan kök hücre kaynaklı nöronların sadece iki ay içinde fonksiyonel olarak olgun bir duruma ulaşabileceğini gösteriyor; özellikle aktif ağları ve gerçekçi bir nöron–astrosit karışımını destekleyen koşullar altında. Bu durumda, “erişkin-benzeri” GluN2A alt birimi NMDA reseptör akımlarına hâkim oluyor ve kalsiyum sinyalleşmesine güçlü katkıda bulunuyor; tıpkı gelişen insan beyninde olduğu gibi. Uzman olmayanlar için çıkarılacak ders, araştırmacıların artık insan eksitatör nöronlarının nasıl olgunlaştığını, birbirine nasıl bağlandığını ve glutatamata nasıl yanıt verdiğini daha sadık bir şekilde modelleyebildiğidir. Bu, ince genetik değişikliklerin veya hastalık süreçlerinin bu hassas anahtarları nasıl bozduğunu incelemeyi mümkün kılarak epilepsiden Alzheimer hastalığına kadar uzanan durumlara bir pencere açıyor ve gelecekteki terapilerin tasarımı ile testine rehberlik ediyor.
Atıf: Escamilla, S., Avilés-Granados, C., Peralta, F.A. et al. GluN2A-mediated currents and calcium signal in human iPSC-derived neurons. Sci Rep 16, 9736 (2026). https://doi.org/10.1038/s41598-026-38482-y
Anahtar kelimeler: NMDA reseptörleri, kök hücre nöronları, beyin gelişimi, kalsiyum sinyalleşmesi, sinyaptik olgunlaşma