Clear Sky Science · tr
INHBA: OSCC prognostiği ve bağışıklığı ile ilişkili mitokondriyle bağlantılı pan-hücre ölümü geni
Ağız kanseri için neden önemli
Oral skuamöz hücreli karsinom (OSCC), ağızda sık görülen bir kanser türü, konuşma, yemek yeme ve rahatça gülümseme gibi temel yetileri elinden alabilir. Cerrahi, radyasyon ve kemoterapiye rağmen birçok hasta yine de nüks ve kötü uzun dönem sağkalım ile karşılaşıyor. Bu çalışma, INHBA adındaki tek bir genin hücre ölümü, tümörün çevresindeki destek hücreleri ve immünoterapi gibi modern tedavilerin başarısı ya da başarısızlığı üzerindeki rolüne odaklanarak ağız kanserine yeni bir bakış getiriyor.
Öldürücü bir ağız kanserine daha yakından bakış
Baş ve boyun kanserlerinin çoğu ağız yüzeyinden başlar ve bunların %90’dan fazlası oral skuamöz hücreli karsinomdur. Dünya genelinde OSCC vakaları ve buna bağlı ölümler artıyor ve 2040’a kadar yaklaşık %40 artması bekleniyor. Standart bakım cerrahi artı radyasyon ve kemoterapiye dayanıyor, ancak birçok tümör tedaviye dirençli olup geri geliyor. Vücudun kendi savunmasını harekete geçirmeyi amaçlayan yeni immünoterapiler yalnızca hastaların bir kısmına fayda sağlıyor. Deneme‑yanılma yaklaşımının ötesine geçmek için araştırmacıların OSCC’ye hangi genlerin yol verdiğini ve bunların bağışıklık sistemiyle nasıl etkileştiğini anlaması gerekiyor.
Hücre ölümü, enerji santralleri ve yeni bir gen kategorisi
Hücrelerimiz, apoptoz, otofaji, ferroptoz ve benzeri isimlere sahip birkaç dikkatle düzenlenmiş şekilde ölme programına sahiptir. Kansere dönüşmüş hücrelerde bu ölüm programları sıklıkla yeniden düzenlenir, böylece tümör hücreleri ölmesi gereken zamanda hayatta kalır. Bu çalışmanın ekibi, farklı ölüm yollarının kesiştiği noktada yer alan "pan‑hücre ölümü" genleri olarak adlandırdıkları geniş bir gruba odaklandı ve özellikle hücre içindeki küçük enerji santralleri olan mitokondri ile ilişkili olanları daralttı. Büyük halka açık kanser veri setlerini özel bir mitokondri gen kataloğuyla birleştirerek "mitokondri‑ilişkili pan‑hücre ölümü genleri" setini tanımladılar ve OSCC davranışı ve hasta sonucu ile en güçlü bağlantıya sahip olanları aradılar.
Çok sayıda şüpheli arasında INHBA’yı bulmak
Gelişmiş istatistik ve dokuz farklı makine öğrenimi algoritması kullanarak araştırmacılar binlerce geni elekten geçirdi ve OSCC’de prognostikle güçlü bağları olan 19 mitokondri pan‑hücre ölümü geni belirledi. Bunların arasında INHBA öne çıktı. Etkinliği tümör örneklerinde normal ağız dokusuna göre sürekli olarak daha yüksek bulundu ve hem OSCC hem de daha geniş baş ve boyun kanserleri grubunda daha kötü sağkalımla ilişkilendirildi. Tümörler yüksek‑ ve düşük‑INHBA gruplarına ayrıldığında, yüksek INHBA düzeyine sahip olanlar doku istila, damar oluşumu ve mitokondri stresi ile ilişkili yollar gibi daha agresif biyolojik işaretler gösterdi. Hasta örnekleri üzerinde yapılan laboratuvar testleri, INHBA ifade düzeylerinin gerçek dünya tümörlerinde gerçekten yükselmiş olduğunu doğruladı.
Tümör çevresindeki destek hücrelerinin gizli rolü
INHBA’nın en çok nerede aktif olduğunu anlamak için ekip, tek hücre RNA dizileme ve mekânsal transkriptomik gibi gen aktivitesini bireysel hücrelerde ve doku kesitleri boyunca haritalayan teknolojilere yöneldi. INHBA’nın esas olarak kanser hücreleri tarafından üretilmediğini, bunun yerine dokuyu yeniden şekillendiren ve bağışıklık ortamını şekillendiren kansere ilişkili fibroblastlar (CAF) tarafından yapıldığını buldular. Myofibroblastik CAF adı verilen belirli bir alt tip özellikle yüksek INHBA düzeyleri gösteriyordu. Ayrıntılı iletişim haritaları, INHBA‑zengini fibroblastların immün hücreler ve tümör hücreleriyle yoğun biçimde iletişim kurduğunu, kanserin etrafında skar‑benzeri, immünsüprese edici bir niş yaratarak tümörü desteklediğini gösterdi. Bu mikroçevre tümör büyümesini teşvik ediyor ve bazı immünoterapi türlerinin etkinliğini azaltıyor olabilir.
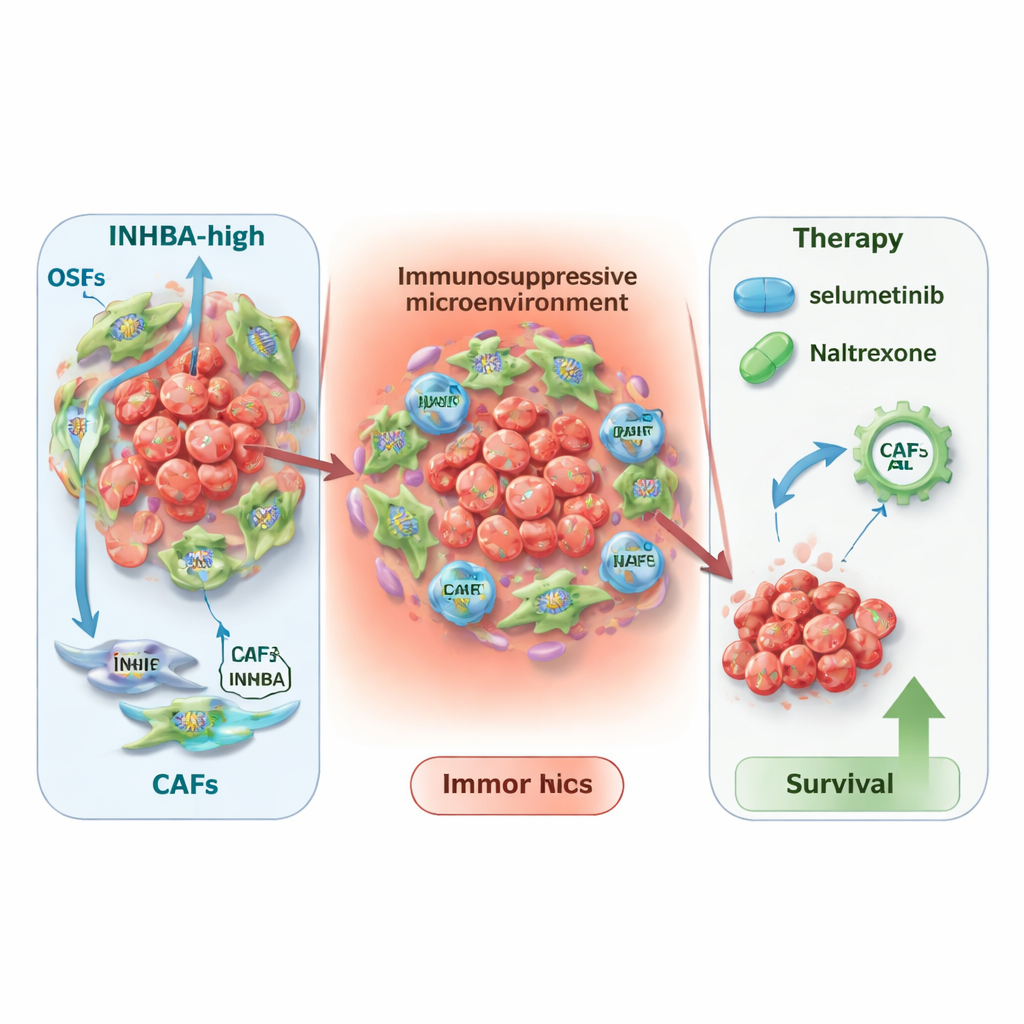
Yeni tedavi açısı ve daha geniş etkiler
INHBA’nın daha tehlikeli bir tümör ortamını işaret ettiğini bilerek, araştırmacılar bunun tedaviyi nasıl yönlendirebileceğini sordular. İmmünoterapi alan hastalarda düşük INHBA düzeyleri, PD‑L1 veya CTLA4 hedefleyen yaygın ilaçlarla daha iyi sonuçlarla ilişkilendirildi; oysa yüksek INHBA düzeyleri CAR‑T hücre yaklaşımlarından daha fazla fayda öngörüyor gibi görünüyordu. İki büyük ilaç‑yanıt veri tabanını tarayarak, yüksek INHBA’lı tümörlerde özellikle umut vaat eden iki mevcut ilacı—selumetinib ve naltrekson—da işaretlediler. Bilgisayar modellemesi her iki ilacın da INHBA proteiniyle güçlü şekilde bağlanabileceğini gösterdi ve bu doğrudan bir etkiye işaret ediyor olabilir. Son olarak, pan‑kanser analizi INHBA’nın birçok başka tümör tipinde de yükselmiş olduğunu ve kötü sağkalımla ilişkili bulunduğunu gösterdi; bu da öneminin ağız kanserinin ötesine uzandığını düşündürüyor.
Hastalar için bunun anlamı
Basitçe söylemek gerekirse, bu çalışma INHBA’yı, esas olarak kanser hücrelerinin kendisinden çok özel destek hücreleri aracılığıyla hareket ederek öldürücü ağız tümörlerinin büyümesine, yayılmasına ve bağışıklıktan kaçmasına yardımcı olan bir "ana anahtar" geni olarak tanımlıyor. Tümörlerde INHBA’yı ölçmek doktorların yüksek riskli hastaları belirlemesine, farklı immünoterapi türlerinden kimlerin yarar göreceğini tahmin etmesine ve bu durumda daha etkili olabilecek hedefe yönelik ilaçları seçmesine yardımcı olabilir. INHBA birçok başka kanserde benzer zararlı bir rol oynadığından, bu gene ve onun fibroblast ortaklarına yönelik tedaviler nihayetinde geniş bir hasta grubuna fayda sağlayarak bakımı daha kesin, kişiselleştirilmiş bir noktaya taşıyabilir.
Atıf: Zhang, X., Sun, M., Qiu, T. et al. INHBA: a mitochondrial-related pan-cell death gene associated with the prognosis and immunity of OSCC. Sci Rep 16, 7642 (2026). https://doi.org/10.1038/s41598-026-38131-4
Anahtar kelimeler: oral skuamöz hücreli karsinom, INHBA, tümör mikroçevresi, kansere ilişkili fibroblastlar, immünoterapi