Clear Sky Science · tr
Obinutuzumab, TRPML2’nin sphingomyelin’e bağlı inhibisyonu yoluyla lizozomal destabilizasyona neden oluyor
Bu antikor öyküsü neden önemli
B-hücreli lenfoma olan birçok insan için, modern antikor ilaçlar bir zamanlar neredeyse her zaman ölümcül olan tanıyı tedavi edilebilir bir hastalığa dönüştürdü. Ancak tüm antikorlar eşit yaratılmamıştır: bazıları kanser hücrelerini diğerlerinden daha güçlü ve daha güvenilir bir şekilde öldürür. Bu makale, obinutuzumab adlı ilacın, selefi rituksimabdan neden lenfoma hücrelerini doğrudan öldürmede daha iyi olduğunu inceliyor; bunun için hücrenin derinlerindeki beklenmedik bir suçluya — hücrenin kendi geri dönüşüm merkezleri olan lizozomlara ve bunların zarlarındaki yağ ve iyon kanalları dengesine — yakından bakıyor.
Yüzey hedefinden içsel kendi kendini yok etmeye
Hem rituksimab hem de obinutuzumab B hücrelerindeki aynı hedefi, CD20 adlı bir proteini tanır. Ancak yazarlar obinutuzumab’ın hücre içine çok daha hızlı ve daha verimli alındığını gösteriyor. Kanser hücresi yüzeyinde CD20’ye bağlandıktan sonra antikor–reseptör kompleksleri endositoz yoluyla içeri çekilir ve lizozomlar da dahil olmak üzere asidik bölmelere iletilir. Orada obinutuzumab lizozomal membran geçirgenliğini tetikler: normalde sağlam olan lizozomal zarı sızdırgan hale gelir, kathepsinler gibi sindirim enzimlerinin hücre içine dökülmesine ve hücre öldürme yollarının başlatılmasına izin verir. Bu bölmelerdeki tuz ve su dengesindeki değişikliklerin lizozomları şişirerek bu öldürücü etkiyi büyük ölçüde artırdığı bulundu.
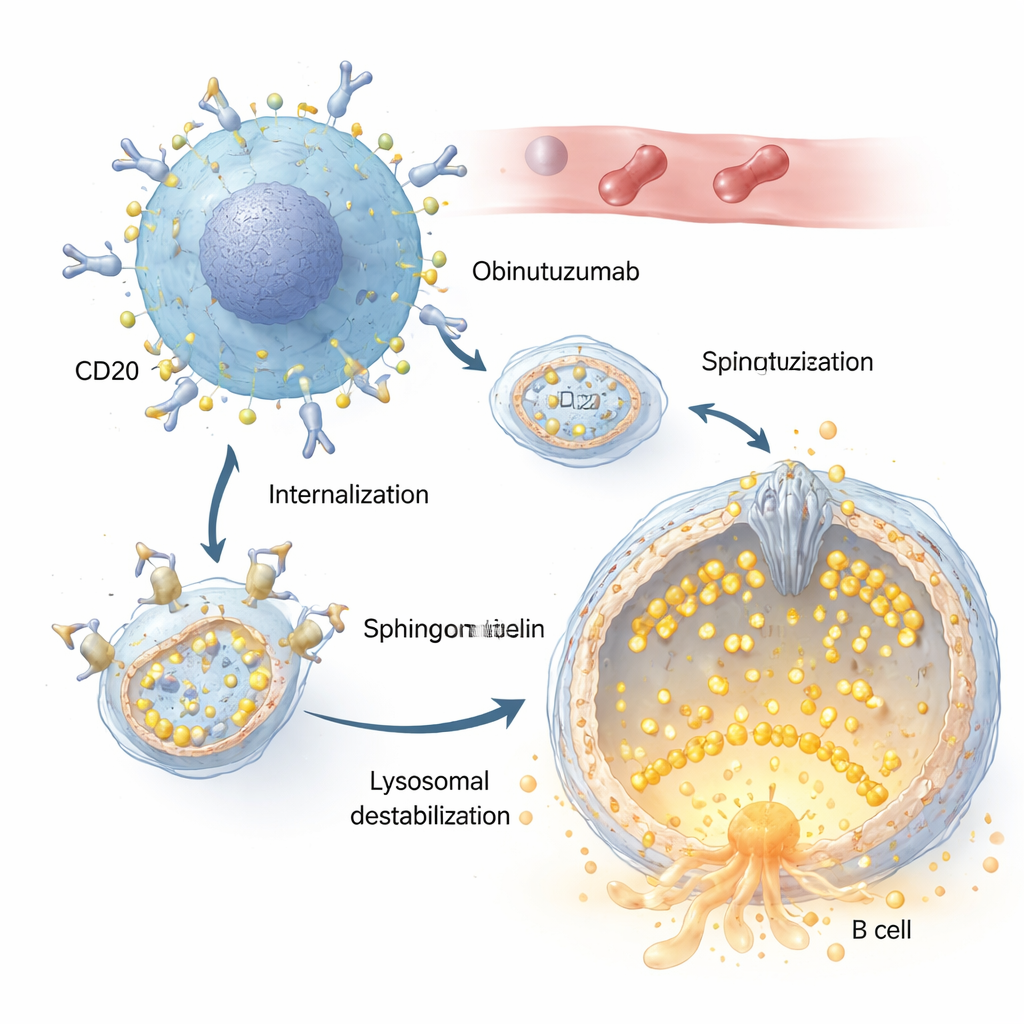
Ufak ama kilit bir kapı görevi gören kanal
Bu öykünün merkezinde lizozomal zarın içine gömülü bir kalsiyum kanalı olan TRPML2 var. Normal koşullarda TRPML2, lizozomların mekanik ve osmotik stresle başa çıkmasına yardımcı olur; kalsiyum salınımı membran onarımını, taşıma süreçlerini ve hacim kontrolünü destekler. Floresan kalsiyum boyaları ve tasarlanmış kalsiyum algılayıcı TRPML2 sürümlerinin kombinasyonunu kullanan araştırmacılar, obinutuzumab’ın bu kanalı hızla kapattığını gösteriyor: tedaviden dakikalar içinde, normalde TRPML kanallarını açan bir ilaç artık kalsiyum patlaması üretmiyor. TRPML2 düzeylerini genetik olarak azaltan yaklaşımlar veya TRPML aktivitesini bloke eden küçük moleküller, her ikisi de lenfoma hücrelerini obinutuzumab’a karşı daha savunmasız hale getiriyor; bu, daha fazla lizozomal sızıntı ve daha yüksek doğrudan hücre ölümü oranlarına yol açıyor.
Zar yağlarının dengeyi nasıl etkilediği
Çalışma daha sonra antikor alımını kanal kapanışına neyin bağladığını sorguluyor. Dikkat, hücre zarlarında bol bulunan ve TRPML kanallarına müdahale ettiği bilinen bir lipid (yağ) olan sphingomyeline yöneliyor. Floresan sphingomyelin-bağlayıcı bir problar kullanarak yazarlar, obinutuzumab içeren veziküllerin asidik bölmelere ulaştıklarında sphingomyelin bakımından zengin olduğunu; bu durumda rituksimab içeren veziküllerden çok daha fazla sphingomyelin içerdiğini buluyorlar. Hücreler sphingomyelinaz ile muamele edildiğinde — sphingomyelin’i kıran bir enzim — TRPML2’nin kalsiyum salınım aktivitesi obinutuzumab varlığında bile geri geliyor. Bu koşullar altında lizozomlar daha az sızma eğiliminde oluyor ve daha az hücre ölüyor; bu da biriken sphingomyelin’in TRPML2’yi etkisiz hale getirip lizozomları yırtılmaya hazır hale getirdiğini güçlü biçimde düşündürüyor.
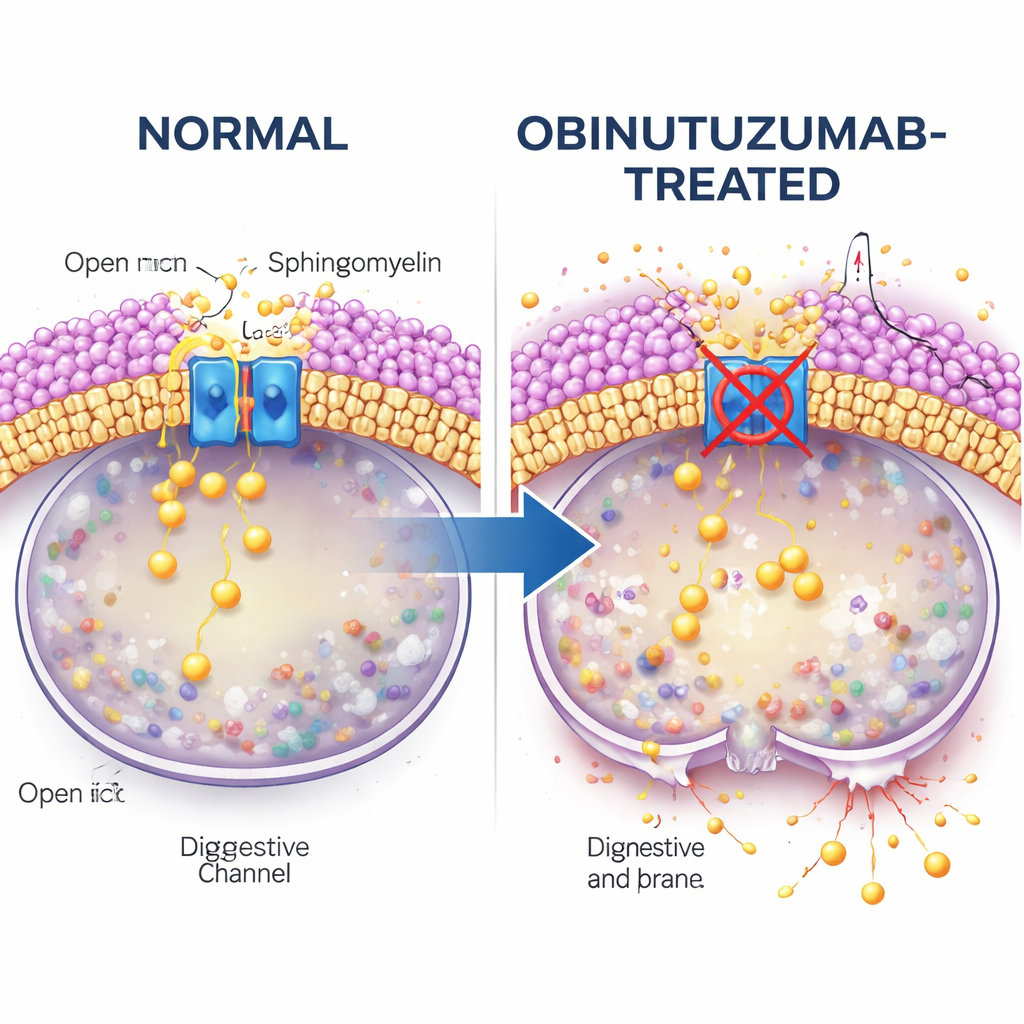
Taşıma yolları ve kolesterol kontrol noktaları
Obinutuzumab’ın hücre içine girdiği yol da önem taşıyor. Elektron mikroskobu ve pH’a duyarlı antikor etiketleme, obinutuzumab’ın hücre yüzeyinden ayrılıp hücre içi veziküllere rituksimabdan daha hızlı girdiğini ortaya koyuyor. Araştırmacılar belirli alım yollarını bozduklarında, kolesterol-bağımlı bir endositoz biçimini (filipin adlı bir bileşikle) bloke etmenin obinutuzumab’ın TRPML2’yi kapatmasını engellediğini ve kısmen lizozomal hasar ile hücre ölümünü azalttığını buluyorlar. Diğer endositoz inhibitörleri bu koruyucu etkiye sahip değil. Bu, obinutuzumab’ı TRPML2 inhibisyonunu ve sonrasındaki membran destabilizasyonunu hazırlayacak şekilde lizozomlara taşıyan, kolesterol ve sphingomyelin açısından zengin, uzmanlaşmış bir yol olduğunu işaret ediyor.
Gelecekteki kanser tedavileri için anlamı
Basitçe söylemek gerekirse, bu çalışma obinutuzumab’ın B-hücreli lenfomaları bu kadar etkili öldürmesinin nedeninin lizozomları kırılgan bir duruma zorlaması olduğunu gösteriyor. Antikor–CD20 komplekslerini sphingomyelin açısından zengin bölmelere iterek ilaç dolaylı olarak koruyucu bir kalsiyum kanalını, TRPML2’yi kapatıyor. Bu koruma ortadan kalktığında lizozomlar stres altında patlamaya daha yatkın hale geliyor ve yıpratıcı enzimler hücreyi içten parçalayarak öldürüyor. Bu lipid–iyon kanal ekseninin anlaşılması, obinutuzumab’ın rituksimabdan neden üstün olduğunu açıklamaktan daha fazlasını yapıyor; aynı zamanda antikor terapilerini güçlendirmek için yeni stratejiler öneriyor — örneğin, bunları sphingolipidleri değiştiren veya TRPML2 aktivitesini artıran ilaçlarla eşleştirerek tümör hücresi lizozomlarının ne zaman ve nasıl kendi kendini yok edeceğini ince ayarlamak mümkün olabilir.
Atıf: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
Anahtar kelimeler: obinutuzumab, B-hücreli lenfoma, lizozom, sphingomyelin, TRPML2