Clear Sky Science · tr
Tüm-hücre modellemesi, arkeon Methanococcus maripaludis’te alternatif proteom dağılım stratejilerini öngörüyor
Neden küçük metan üreticiler önemli
Methanococcus maripaludis, karbondioksit ve format gibi basit kimyasalları metana — doğalgazın önemli bir bileşenine — çeviren mikroskobik bir arkeondur. Bu mikrobün iç kaynaklarını — özellikle proteinlerini — nasıl bütçelendiğini anlamak, enerji kısıtlılığında yaşamın genel kurallarını ortaya çıkarabilir ve onu biyolojik metan fabrikası veya yeşil kimya için bir platform olarak kullanma çabalarını yönlendirebilir.
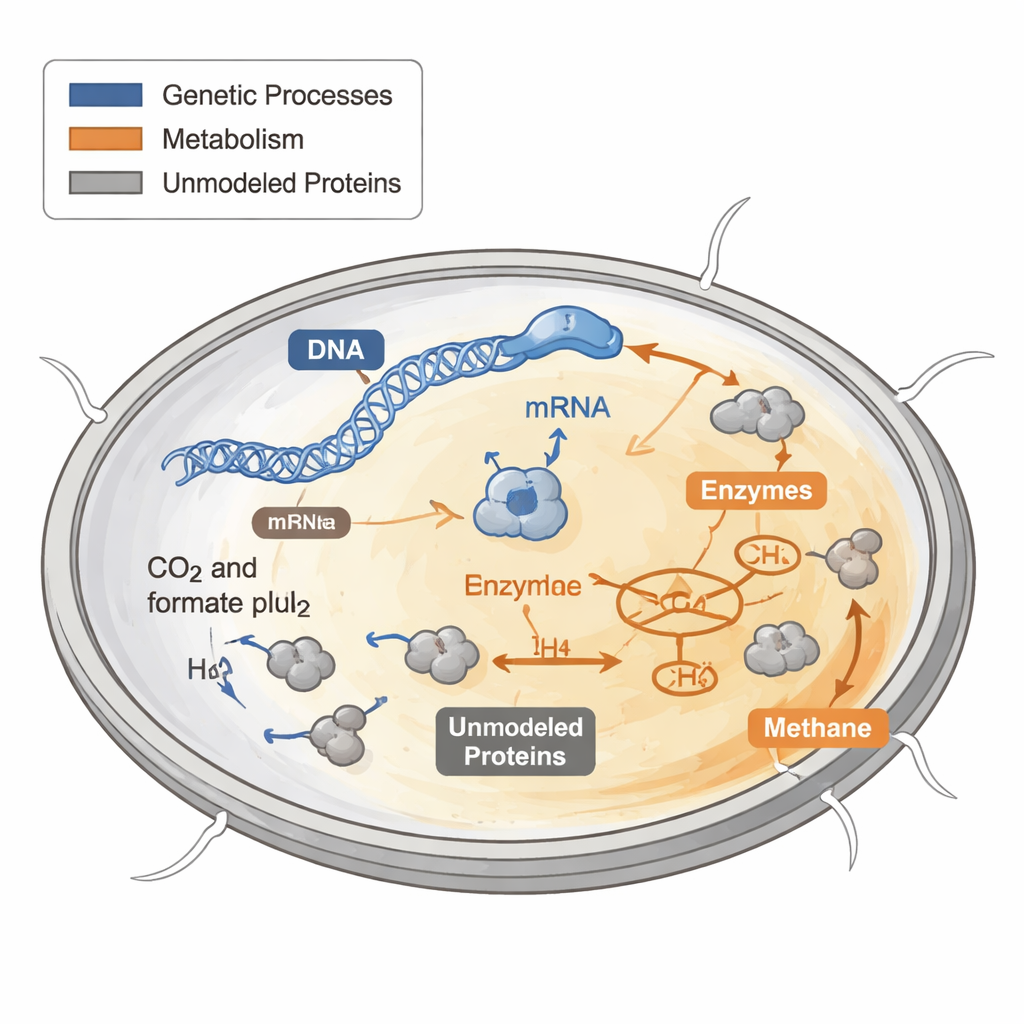
Hücreler protein bütçelerini nasıl harcar
Her hücre sınırlı protein “bütçesini” nasıl harcayacağına karar vermek zorundadır. Bazı proteinler yeni hücresel parçalar inşa eder, bazıları enerji toplar ve diğerleri bakım görevlerini yerine getirir. Önceki metabolizma bilgisayar modelleri bu proteinleri ücretsiz ve sınırsızmış gibi ele aldı; bu yaklaşım zorlu veya besin fakiri koşullar altında büyümeyi öngörmeye çalışırken kötü sonuç verdi. Bakteri ve mayada yapılan deneyler, hızlı büyüyen hücrelerin protein bütçelerinden ribozomlara — yeni proteinleri üreten moleküler makinelere — daha büyük bir pay ayırdığını, yavaş büyüyen hücrelerin ise kaynaklarını başka yerlere kaydırdığını gösterdi.
Kuralı bozan bir arkeon
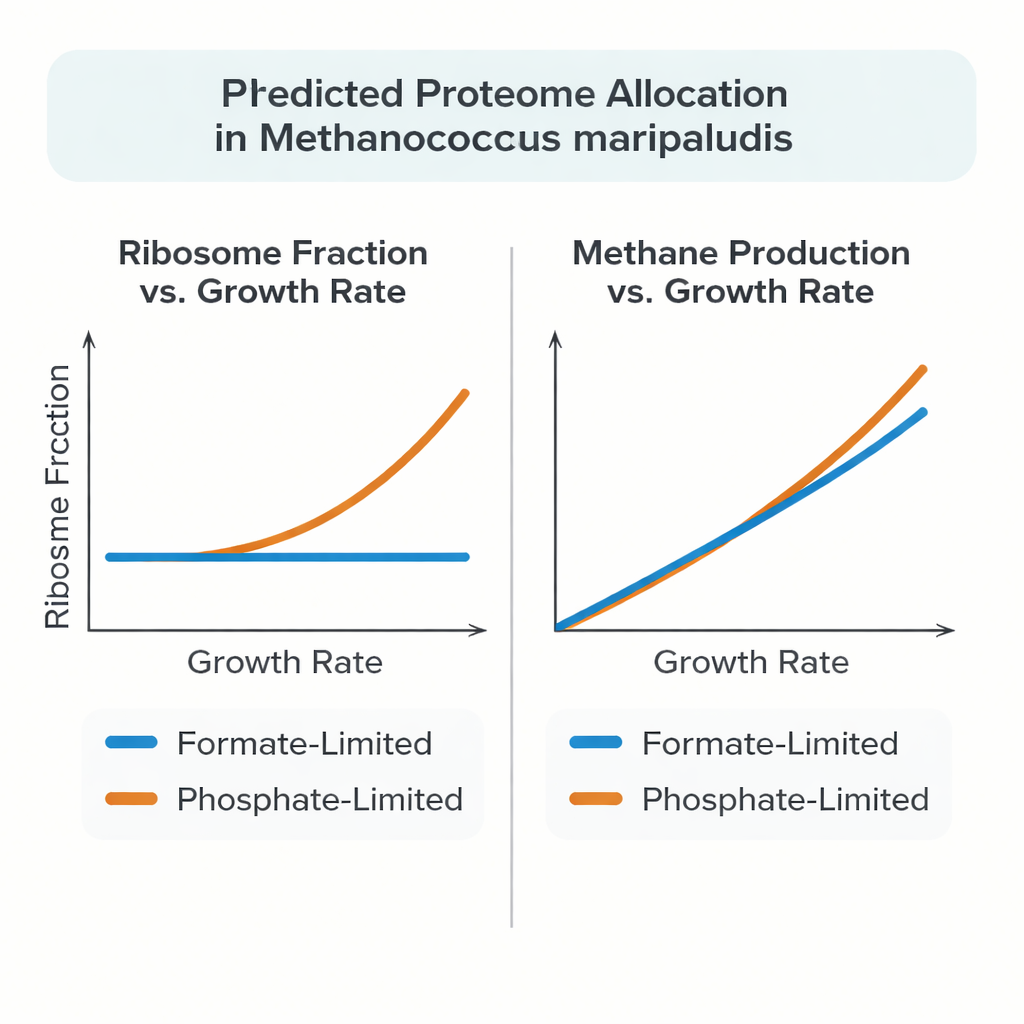
Son deneyler, M. maripaludis’ün her zaman bu desene uymadığını ortaya koydu. Format hem besin hem de enerji kaynağı olarak kullanıldığında, büyüme yavaşlasa bile ribozomlara ayrılan protein bütçesinin payı neredeyse sabit kalıyor. Ancak fosfat sınırlaması altında, arkeon daha geleneksel davranıyor: ribozom payı büyüme hızıyla birlikte artıyor; bu, Escherichia coli ve mayayla benzer bir eğilim. Bu sıra dışı davranışı açıklamak için yazarlar, metabolizmayı protein ve RNA’nın yapımı ve montajı gibi enerji maliyetli süreçlere bağlayan, proteinleri soyut reaksiyon hızları olarak ele almayan ayrıntılı bir tüm-hücre tarzı model inşa ettiler.
Tüm-hücre tarzı model kurulması
Araştırmacılar, M. maripaludis’ün mevcut bir metabolik haritasından başladılar ve DNA’dan RNA’ya kopyalama, taşıyıcı RNA’ların şarj edilmesi, ribozom ve enzim komplekslerinin birleştirilmesi ve hücre bölünmesi sırasında bu bileşenlerin seyreltilmesi gibi gen ekspresyonunu tanımlayan binlerce ek reaksiyon eklediler. Enzim hız limitlerini biyokimya veri tabanları ve literatürden topladılar ve protein kütlesinin haritada doğrudan reaksiyonlara bağlanmamış “model dışı” proteinlerden ne kadar oluştuğunu tahmin ettiler. Ardından toplam protein ve RNA kütlesini sınırlayan, reaksiyon hızlarını mevcut enzim miktarına bağlayan ve protein üretimini ribozom kapasitesine bağlayan küresel kısıtlar koydular. Bu kısıtlarla model, büyümeyi desteklemek için sabit bir protein bütçesini nasıl dağıtacağına karar vermek zorunda kalıyor.
Simülasyonların ortaya koydukları
Yüksek kaliteli şant deneyleriyle test edildiğinde model, ölçülen protein ve RNA kütlelerini, metan üretim hızlarını ve çeşitli yavaş büyüme hızları aralığındaki büyüme verimlerini doğru biçimde yeniden üretti. Format sınırlaması altında, simüle edilen hücre büyüme değişse bile neredeyse sabit bir ribozomal protein payında doğal olarak kararlı hale geldi; bu, deneysel verileri yansıtıyor. Fosfat sınırlaması altında model, ribozom payındaki gözlenen artışı yalnızca ribozomların düşük büyüme hızlarında daha hızlı çalışmasına izin verildiğinde yakaladı; bu da daha fazla ribozomun aktif olarak protein sentezine katıldığını gösteren ölçümlerle tutarlı. Model ayrıca M. maripaludis’teki proteinlerin önemli bir kısmının minimal büyüme için kesinlikle gerekli olmadığını ve fazladan karbon ile enerjinin hangi besin sınırlayıcıysa ona bağlı olarak glikojen veya serbest amino asitler gibi diğer büyük moleküllerde depolanabileceğini veya yönlendirilebileceğini öne sürdü.
Mutantları ve büyüme sınırlarını incelemek
Model her yolun protein maliyetini açıkça hesaba kattığından, sadece bir genetik mutantın büyüyüp büyüyemeyeceğini değil, vahşi tipe göre ne kadar iyi büyüyeceğini de öngörebilir. Yazarlar farklı hidrojen işleyen enzimlerden yoksun suşları simüle etti ve hidrojen ve karbon monoksit varlığı/dokunulmazlığı dahil olmak üzere birkaç büyüme koşulu boyunca laboratuvar ölçümleriyle karşılaştırdılar. Birçok durumda model, mutantların büyüyüp büyüyemeyeceğini yakaladı ve ilişkili göreli büyüme hızları için makul tahminler üretti; bu, yalnızca evet/hayır yanıtı verebilen önceki modellerden ileriydi. Aynı çerçeve, farklı substrat kombinasyonları için şarj koşullarında mümkün olan maksimum büyüme hızlarını tahmin etmek amacıyla da kullanıldı.
Bilim ve teknoloji için anlamı
Günlük ifadeyle bu çalışma, M. maripaludis’ün protein iş gücünü bütçelemek için alternatif bir strateji kullandığını; bazı koşullar altında büyüme yavaşlarken protein fabrikalarını bütçenin sabit bir payında çalışır durumda tuttuğunu, onları geri çekmediğini gösteriyor. Bu davranışı ayrıntılı, veri odaklı bir modele gömerek çalışma, enerji kısıtlı mikropların büyüme, bakım ve depolama dengesini nasıl kurduğunu araştırmak için bir test zemini sağlıyor. Uygulamaya dönük araştırmalar için model, hangi enzimlerin ve yolların protein yatırımı açısından en maliyetli olduğunu belirleyerek bu arkeonu daha fazla metan veya başka ürünler üretmesi üzere mühendisleştirme yolunu haritalandırıyor. Daha geniş anlamda, çalışma güçlü tüm-hücre tarzı modellemeyi bakteriler ve mayanın ötesine arkeal alana genişleterek moleküler ayrıntılar ile iklim, enerji ve endüstriyel biyoteknoloji ile ilgili mikrobiyal toplulukların büyük ölçekli davranışı arasındaki boşluğu kapatmaya yardımcı oluyor.
Atıf: Kasem, G.S., Soliman, T.H.A., Mousa, M.A.A. et al. Whole-cell modeling predicts alternative proteome allocation strategies in the archaeon Methanococcus maripaludis. Sci Rep 16, 7386 (2026). https://doi.org/10.1038/s41598-026-37887-z
Anahtar kelimeler: Methanococcus maripaludis, proteom dağılımı, tüm-hücre modelleme, metanojenez, arkeaların metabolizması