Clear Sky Science · tr
Kürkümin yüklü gümüş-amin fonksiyonlu silika nanopartiküllerin antikanser aktivitesi
Mutfak Baharatını Daha Akıllı Bir Kanser Savaşçısına Dönüştürmek
Pek çok körinin parlak sarı rengi olan zerdeçal, uzun süredir sağlık yararları—bunların arasında antikanser etkinlik—iddia edilen doğal bir bileşik olan kürkümin içerir. Ancak tek başına kürkümin suda kötü çözünür, vücutta çabuk parçalanır ve tümörlere faydalı dozlarda ulaşmakta zorlanır. Bu çalışma, kürkümini küçük mühendislik parçacıklarının içine paketlemenin yeni bir yolunu anlatıyor; böylece kürkümin daha kararlı, tümörlere daha hedefli ve kanser hücrelerine karşı daha güçlü hale gelirken sağlıklı dokulara zarar verme ihtimali azaltılmaya çalışılıyor.
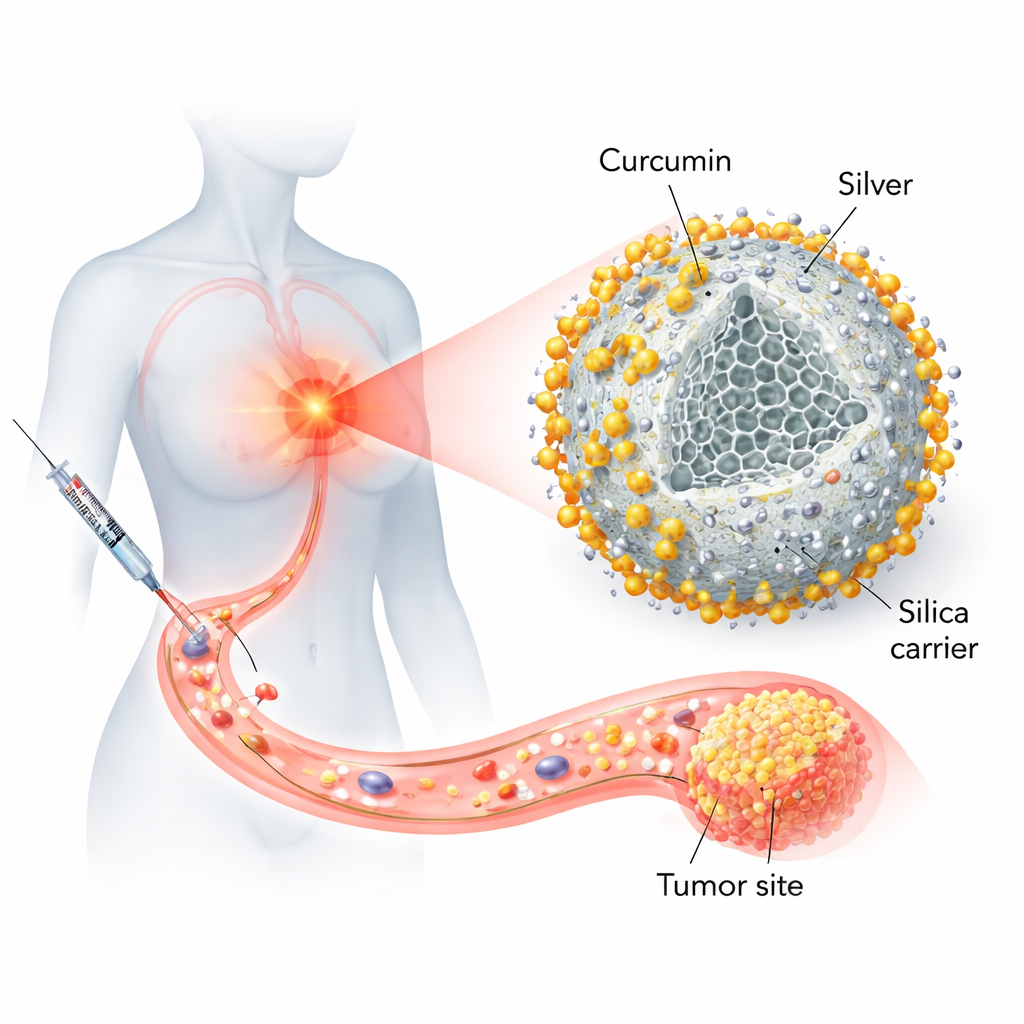
Neden Umut Vaadeden Bir Doğal İlaç Daha İyi Bir Taşıma Gerektirir
Kürkümin, kanser hücrelerinin büyüme ve hayatta kalma için güvendiği birden fazla süreci bozabilir. Ne yazık ki, insanlar kürkümin aldığında, çoğu asla tümöre ulaşmaz: çözünmek yerine topaklanır, kan dolaşımından hızla temizlenir ve yüksek dozda güvenli şekilde enjekte edilemez. Yağ bazlı parçacıklar veya polimer kapsüller gibi mevcut taşıma sistemleri durumu bir derece iyileştirdi, ancak genellikle sadece az miktarda ilaç taşıyabilir, kararsız olabilir veya karmaşık üretim gerektirebilir. Aynı zamanda, gümüş nanopartiküller reaktif moleküller üreterek bakteri ve kanser hücrelerine zarar verdiği bilinir, fakat bunlar da bazen kararsız ve toksik olabilir. Araştırmacılar, bu iki etkeni—kürkümin ve gümüşü—her ikisini de dengeleyebilecek ve ilacı gerektiği yerde salabilecek dikkatle tasarlanmış bir silika “kabuğu” içinde birleştirmeyi hedeflediler.
Kum, Gümüş ve Kürkümin ile Küçük Taşıyıcılar İnşa Etmek
Ekip önce silika nanopartiküller oluşturdu—kum ile aynı temel maddeden yapılmış nanometre ölçeğinde küreler—uniform, gözenekli parçacıklar üreten bir çözelti bazlı yöntem kullanarak. Ardından yüzeyi, hem gümüş iyonlarının hem de kürküminin tutunmasını iyileştiren amin gruplarıyla süslediler. Gümüş, bu aminlere sıkı bağlanacak şekilde eklendi ve hibrit bir gümüş–silika iskeleti oluştu. Son olarak, zerdeçal köklerinden ekstrakte edilen kürkümin bu yapıya bir alkol çözeltisinden yüklendi. Ortaya çıkan parçacıklar, CUR@Ag-AFS olarak adlandırıldı, göreli olarak yüksek miktarda ilaç barındırırken katı ve uniform kaldı. Bir dizi laboratuvar tekniği, parçacıkların küresel olduğunu, silikon, oksijen, azot, karbon ve gümüş elementlerinin tümünün mevcut olduğunu ve kürküminin gevrek kristaller halinde değil daha düzensiz, kararlı bir formda gömülü olduğunu doğruladı.
Tümörlerin İçinde Daha Fazla İlaç Salacak Şekilde Tasarlandı
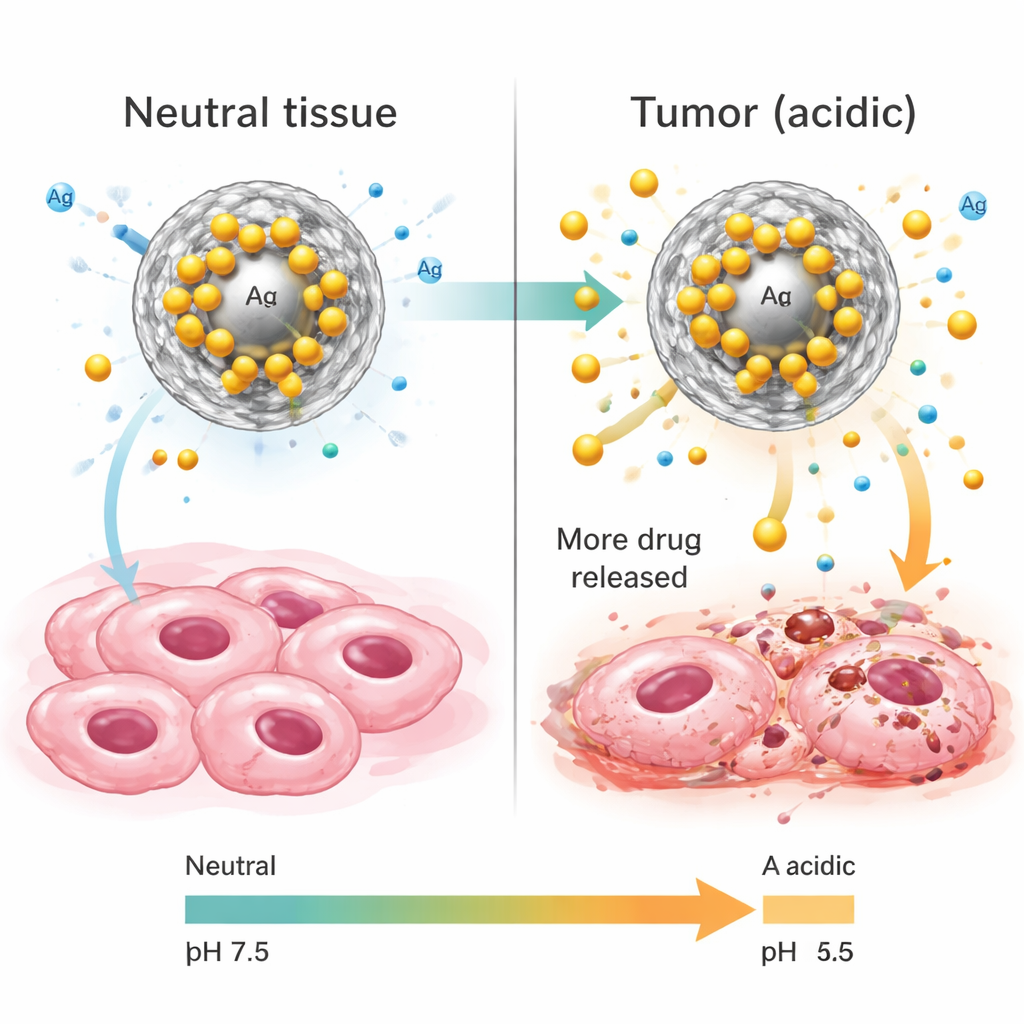
Yeni taşıyıcıların farklı ortamlarda nasıl davrandığını test etmek için araştırmacılar bunları normal kan ve dokuyu taklit eden (nötr pH) sıvılarla ile tümörlerin ve kanser hücresi kompartmanlarının tipik daha asidik çevresi arasında koydu. 24 saat boyunca parçacıklar kürkümini yavaş ve istikrarlı şekilde saldı, ancak belirgin bir pH bağımlılığıyla: en fazla ilacı—yüklerinin yüzde 90’ından fazlasını—tümör hücreleri içindeki benzer asidik koşullar altında verdiler ve nötr koşullar altında çok daha az salındı. Salım verilerinin matematiksel analizi, kürküminin öncelikle silikanın gözenekleri aracılığıyla difüze olduğunu, asiditenin ise kürkümin ile parçacık yüzeyi arasındaki çekimi zayıflattığını gösterdi. Pratik anlamda, bu sistemin sağlıklı dokularda nispeten sessiz kalacak, ancak kanserli dokularda çok daha aktif hale gelecek şekilde ayarlandığı; böylece yan etkileri azaltırken güçlü lokal etkiyi koruyabileceği anlamına geliyor.
Parçacıkları Kanser Hücrelerine Karşı Test Etmek
Ekip daha sonra insan meme kanseri hücrelerini (MCF-7) çeşitli formülasyonlara maruz bıraktı: sade silika, amin gruplu silika, gümüşlü silika, serbest kürkümin ve birleşik CUR@Ag-AFS parçacıkları. Tedavi sonrası hücre hayatta kalımını metabolik aktiviteyi yansıtan standart bir renk-değiştirme testi ile ölçtüler. Tüm nanoparçacık sistemleri arasında kürkümin–gümüş–silika hibriti kanser hücrelerini öldürmede en etkili olanıydı; pozitif kontrol olarak kullanılan klasik kemoterapi ilacı doksorubisin hariç en yüksek etkiye sahipti. Hibrit parçacıklar, aynı seviyede kanser hücresi ölümünü serbest kürkümin veya yalnız gümüş içeren parçacıklardan belirgin şekilde daha düşük konsantrasyonlarda elde etti; bu da sinerjistik bir etkiye işaret ediyor. Önemli olarak, altta yatan silika iskeleti kendisi nispeten düşük toksisite gösterdi; bu da antikanser etkinin büyük ölçüde kürkümin–gümüş kombinasyonundan ve bunun sunum şeklinden kaynaklandığını gösteriyor.
Geleceğin Kanser Bakımı İçin Ne Anlama Gelebilir
Erişilebilir terimlerle, araştırmacılar kürkümin ve gümüşü emecek, dolaşım sırasında onları koruyacak ve bir tümörün asidik ortamına ulaştıklarında daha hızlı salıverecek türden silikadan yapılmış akıllı, mikroskobik bir sünger inşa ettiler. Bu tasarım hem kürküminin kanser öldürücü gücünü artırıyor hem de onu hastalıklı hücrelere daha doğrudan yönlendirmeye yardımcı oluyor; silika yapısı ise stabilite ve kontrol sağlıyor. Bu çalışma laboratuvarda ve hücre kültürlerinde yapıldı—henüz hayvanlarda veya hastalarda değil—ancak kürkümin gibi doğal bileşiklerin dikkatle tasarlanmış nanomalzemelerle eşleştirilmesinin, daha hedefli, daha uzun süreli ve muhtemelen vücudun geri kalanına daha az zarar veren kanser tedavilerine katkıda bulunabileceği bir geleceğe işaret ediyor.
Atıf: Shafqat, S.S., Wakeel, M., Zubair, M. et al. Anticancer activity of curcumin loaded hybrid system of silver-amine functionalized silica nanoparticles. Sci Rep 16, 7026 (2026). https://doi.org/10.1038/s41598-026-37829-9
Anahtar kelimeler: kürkümin nanopartikülleri, hedefe yönelik kanser tedavisi, gümüş nanotaşımacılar, pH-duyarlı ilaç taşıma, meme kanseri hücreleri