Clear Sky Science · tr
Çok görevli öğrenmeye dayalı Alzheimer hastalığı karmaşık özellik tahmininin modellenmesi ve uygulaması
Bu araştırma aileler ve hastalar için neden önemli
Alzheimer hastalığı, zamanımızın en korkulan teşhislerinden biridir; buna rağmen doktorlar hâlâ kimin hızla kötüleşeceğini, kimin yıllarca stabil kalacağını ve hangi erken bulguların gerçekten önemli olduğunu öngörmekte zorlanıyor. Bu çalışma basit ama güçlü bir soruyu soruyor: Alzheimer ile ilgili birkaç test sonucu ve beyin taramalarını birlikte değerlendirip bunları bir kişinin genetik bilgileriyle birleştirirsek, modern yapay zeka hastalığın seyrini daha doğru tahmin etmemize yardımcı olacak desenleri öğrenebilir mi?
Aynı hastalığın birçok yüzü
Alzheimer sadece hafıza kaybı değildir. Hastalar düşünme testlerindeki performansları, günlük işleri yönetme becerileri ve beyin taramalarının görünümü açısından farklılık gösterir. Yaygın bellek ve bilişsel ölçekler, günlük işlevselliğe dair anketler ve beyin metabolizması veya amiloid birikimini gösteren PET taramaları gibi bu farklı ölçümler genler tarafından kısmen etkilenir. Önemli olarak, bunlar bazı ortak genetik kökenleri de paylaşır. Geleneksel tahmin yöntemleri genellikle bir ölçüme odaklanır ve bu ilişkili özelliklerin ortak bilgisini göz ardı eder. Yazarlar, tek bir testi görmek yerine bütünü gören bir doktor gibi, modellerin de birden çok özelliği birlikte öğrenmesi gerektiğini savunuyor.
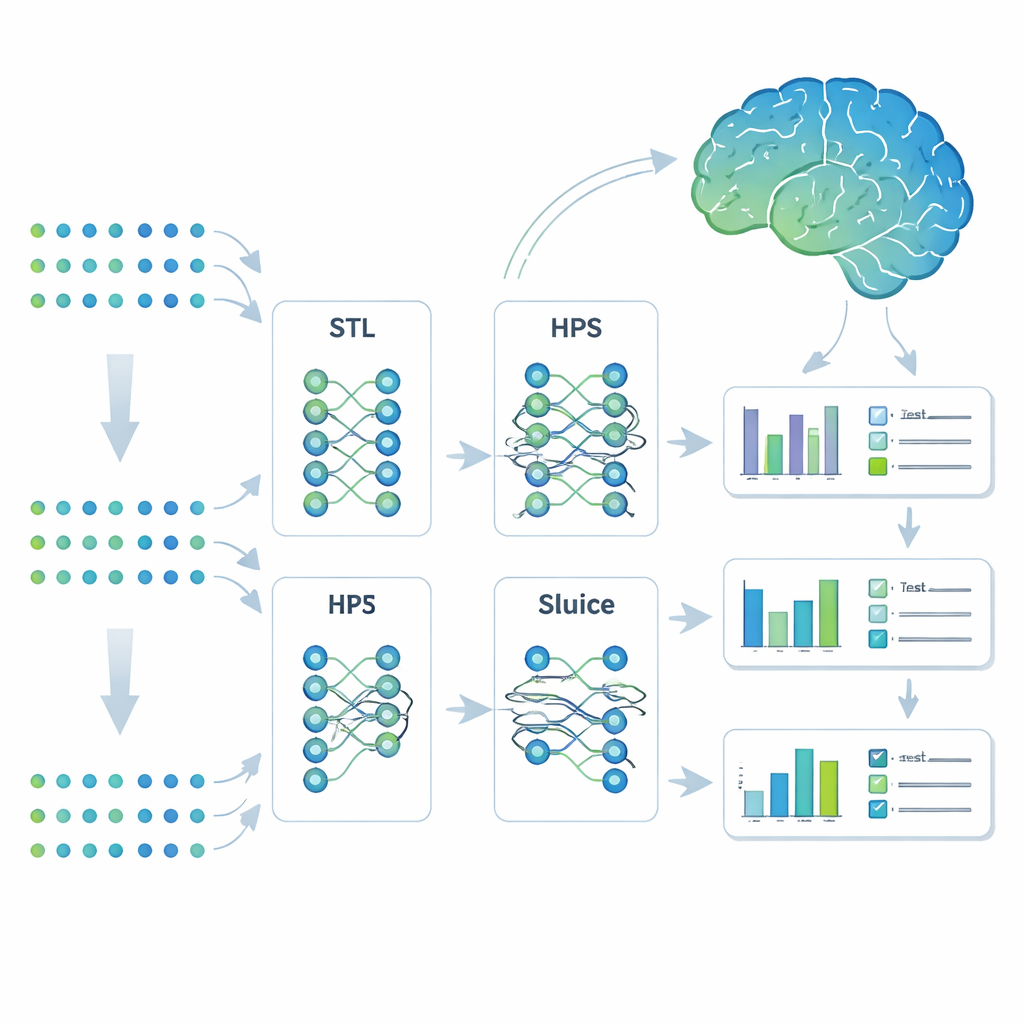
Tek bir modele birçok ilişkili görevi öğretmek
Araştırmacılar çok görevli öğrenme adını verdiğimiz bir makine öğrenmesi stratejisine yöneldi. Her sonuç için ayrı modeller oluşturmak yerine, tek bir sistemi aynı anda yedi Alzheimer ilişkili özelliği tahmin edecek şekilde eğittiler. Dört yaklaşımı karşılaştırdılar: tamamen ayrı modeller (tek görevli öğrenme), yalnızca en sonda ayrım yapan basit paylaşımlı model (katı parametre paylaşımı), görevleri alt gruplara ayırabilen daha esnek bir dallanma tasarımı ve ağın her katmanında ne kadar bilginin paylaşıldığını ince ayar yapabilen oldukça uyarlanabilir bir tasarım olan Sluice Ağı. Dört model de aynı genetik girdileri gördü; fark, öğrendiklerini özellikler arasında nasıl paylaştıklarındaydı.
Simüle edilmiş genomlarda fikirleri test etmek
Herhangi bir modeli gerçek hastalar üzerinde kullanmadan önce, ekip Alzheimer’s Disease Neuroimaging Initiative (ADNI) tarafından elde edilen gerçek genetik desenleri kullanarak, ancak çıktıları tamamen kontrol edebildikleri ayrıntılı simülasyonlar kurdu. Tüm özelliklerin aynı genetik nedenleri paylaştığı senaryolar, özelliklerin örtüşen gruplar oluşturduğu senaryolar ve her özelliğin farklı nedenlere sahip olduğu senaryolar yarattılar. Ayrıca genetik sinyallerin ne kadar güçlü olduğunu ve ne kadar gürültü eklediklerini değiştirerek insan verilerinin karışık gerçeğini taklit ettiler. Neredeyse tüm koşullarda Sluice Ağı en doğru tahminleri verdi ve özellikler sadece zayıf ilişkili olduğunda bile istikrarlı kaldı. Daha basit paylaşımlı modeller, özelliklerin birçok genetik faktörü ortak kullandığı durumlarda iyi performans gösterdi ancak paylaşım düşük olduğunda başarısız oldu; tamamen ayrı modeller ise daha istikrarlı ama genel olarak daha az doğru çıktı.
Gerçek dünya verileri ve genlerin gruplanmasının gücü
Yazarlar daha sonra bu modelleri 463 bireyden oluşan gerçek ADNI verisine uyguladılar; burada daha önce Alzheimer ile ilişkilendirilmiş 56 genden alınan yaklaşık 3.800 genetik belirteci kullandılar. Buna biyolojik ilhamlı bir dokunuş eklediler: binlerce ayrı genetik belirteci doğrudan beslemek yerine, önce belirteçleri gene göre grupladılar ve ağın yedi çıktıyı tahmin etmeden önce her gen için kompakt bir “özet” sinyal öğrenmesine izin verdiler. Bu gen seviyesi toplulaştırma çoğu model için performansı artırdı ve özellikle Sluice Ağı için ortalama korelasyonunu yaklaşık iki katına çıkardı. Kazanımlar PET görüntüleme ölçümleri ile bazı bilişsel ve işlevsel skorlar için daha belirgindi; bu da izole belirteçler olarak ele alındıklarında zayıf kalan genetik etkilerin gen düzeyinde birleştirildiğinde daha tespit edilebilir hale geldiğini düşündürüyor.
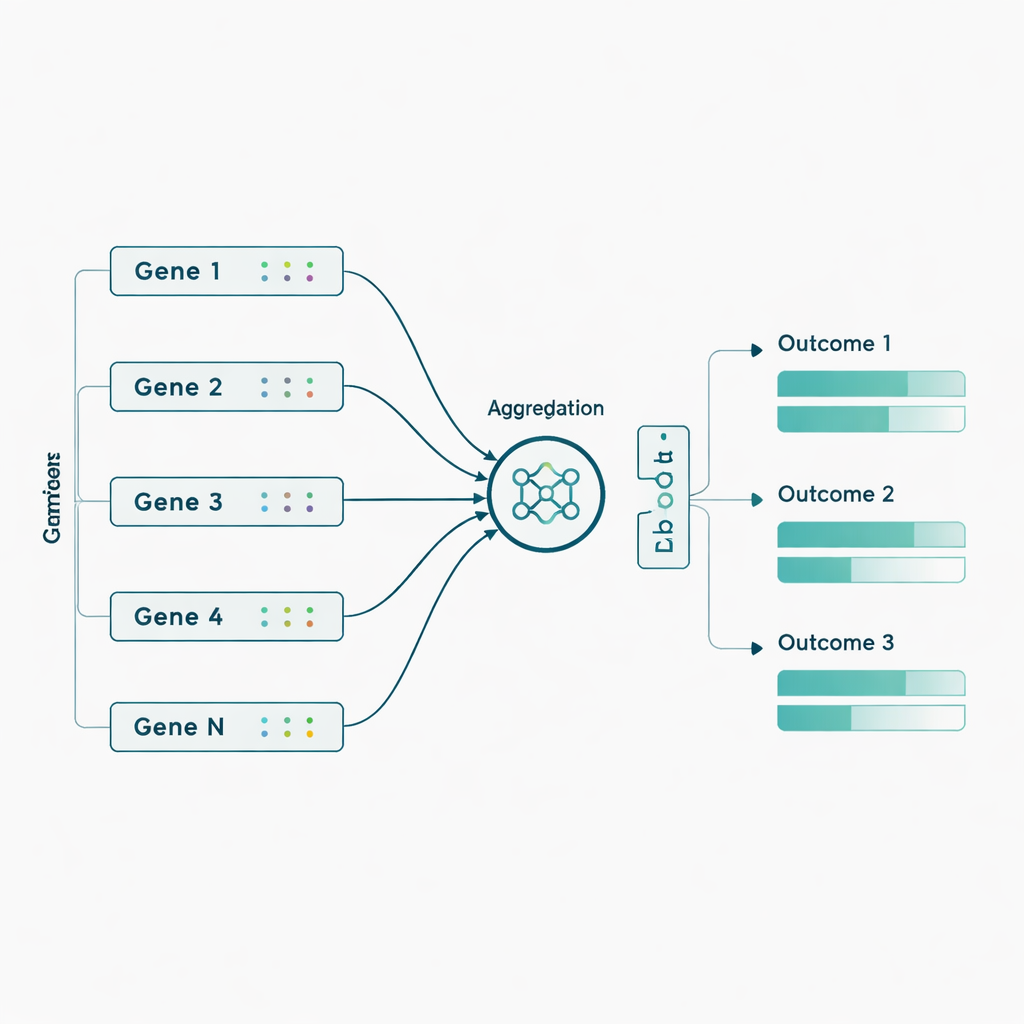
Gelecekteki tahmin ve bakım için anlamı
Bir uzman olmayan için çıkarılacak mesaj şudur: Daha akıllı, daha esnek yapay zeka modelleri, aynı genetik ve klinik verilerden, ilişkili birkaç çıktıyı aynı anda öğrenerek ve biyolojinin genler halinde organize olma biçimine saygı göstererek daha fazla içgörü çıkarabilir. Mevcut kazanımlar mütevazı ve klinik bir testten uzak olsa da, bu yaklaşım bir kişinin risk profilini tahmin etme, muhtemel ilerlemeyi izleme ve belki izlemi veya müdahaleleri kişiselleştirme yönünde daha güvenilir araçlara işaret ediyor. Birçok küçük genetik etkinin etkileştiği Alzheimer gibi karmaşık hastalıklarda, özellikler arasında bilgi paylaşan ve zayıf sinyalleri toplulaştıran yöntemler, geleneksel tek özellikli skorlamadan daha net ve bilgilendirici bir tablo sunabilir.
Atıf: Zhou, W., Xue, Z., Liang, J. et al. Modeling and application of alzheimer’s disease complex trait prediction based on multi-task learning. Sci Rep 16, 7749 (2026). https://doi.org/10.1038/s41598-026-37820-4
Anahtar kelimeler: Alzheimer hastalığı genetiği, çok görevli öğrenme, derin öğrenme tahmini, nörogörüntüleme biyobelirteçleri, gen seviyesi toplulaştırma