Clear Sky Science · tr
Wnt-3a, β-katenin kanonik yolundan bağımsız olarak LPS ile uyarılmış mikroglialarda TNF-α üretimini kötüleştirir
Beyin iltihabının önemi
Parkinson hastalığı da dahil olmak üzere birçok beyin bozukluğunun kronik iltihabı içerdiği artık bilinmektedir. Bu süreçte, mikroglia adı verilen beyin hücrelerine yerleşik bağışıklık hücreleri, koruyucu yardımcı rolünden komşu nöronlara zarar veren aşırı aktif saldırganlara dönüşebilir. Bu çalışma zamanlı bir soruyu gündeme getiriyor: uzun süredir yatıştırıcı, koruyucu etkileri olduğu düşünülen Wnt‑3a adlı bir sinyal molekülü, belirli koşullar altında gerçekten iltihabı kötüleştirebilir mi? Cevap beklenenden daha karmaşık çıktı ve aynı molekülün bir bağlamda yararlı, başka bir bağlamda zararlı olmasının nedenini vurguluyor.
İki yüzlü bir haberci
Wnt proteinleri, beyin gelişimini yönlendiren, erişkinlikte beyin hücrelerini koruyan ve hücrelerin yaralanmaya yanıt verme şeklini şekillendiren bir kimyasal haberci ailesidir. En iyi incelenen üyelerden biri olan Wnt‑3a genellikle hücre içinde β‑katenin adlı bir proteinin stabilize edilmesini sağlayan “kanonik” bir sinyal yoluyla ilişkilendirilir. Birçok sistemde bu yolun etkinleştirilmesi iltihabı azaltıyor ve nöron hayatta kalmasını destekliyor gibi göründüğünden, bazı araştırmacılar Wnt‑3a’yı artırmanın Parkinson hastalığında hassas dopamin üreten nöronları korumaya yardımcı olup olmayacağını merak ettiler. Ancak Wnt proteinleri, yerine göre iltihabı tetikleyebilecek alternatif “kanonik olmayan” yollardan da sinyal verebilir ve hangi yolun baskın olduğu hücre tipi ve hücrenin durumuna bağlı olabilir.
Sakin hücreler sakin kaldığında
Bu olasılıkları araştırmak için araştırmacılar fare beyinlerinden yetiştirilmiş birincil mikrogliaları inceledi. Önce dinlenme, homeostatik durumda olan mikroglialara yalnızca Wnt‑3a uyguladılar. Bu sakin koşullar altında Wnt‑3a, TNF‑α veya IL‑1β gibi anahtar iltihap moleküllerinin salımını artırmadı. Hücre içindeki bazı sinyaller aktive olsa da mikroglialar güçlü bir iltihap moduna geçmedi. Bu, sağlıklı, iltihaplı olmayan bir beyinde tek başına Wnt‑3a eklemenin mikrogliaların iltihapçı çıktısı üzerinde doğrudan az etkisi olabileceğini gösterir.
İltihaplı hücreler daha da zorlandığında
Görüntü, mikroglialar önce enfeksiyon taklidi yapmak için kullanılan laboratuvarda yaygın bir araç olan bakteriyel lipopolisakkarit (LPS) ile iltihaplı duruma getirildiklerinde dramatik şekilde değişti. Beklendiği gibi, yalnızca LPS TNF‑α üretiminde güçlü bir artış sağladı. Ancak Wnt‑3a LPS ile birlikte eklendiğinde, mikroglialar yalnızca LPS ile kıyaslandığında anlamlı şekilde daha fazla TNF‑α saldı; IL‑1β ise daha fazla artış göstermedi. Ayrıntılı ölçümler, bu TNF‑α artışının alışılmış NFκB iltihap yolunun daha fazla aktivasyonundan veya kanonik β‑katenin yolunun ek aktivasyonundan kaynaklanmadığını gösterdi. DKK1 adlı bir proteinle β‑katenin yolunun engellenmesi, Wnt‑3a kaynaklı TNF‑α patlamasını değiştirmedi; bu da beklenen “anti‑iltihap” yolun sorumlu olmadığını gösteriyordu.
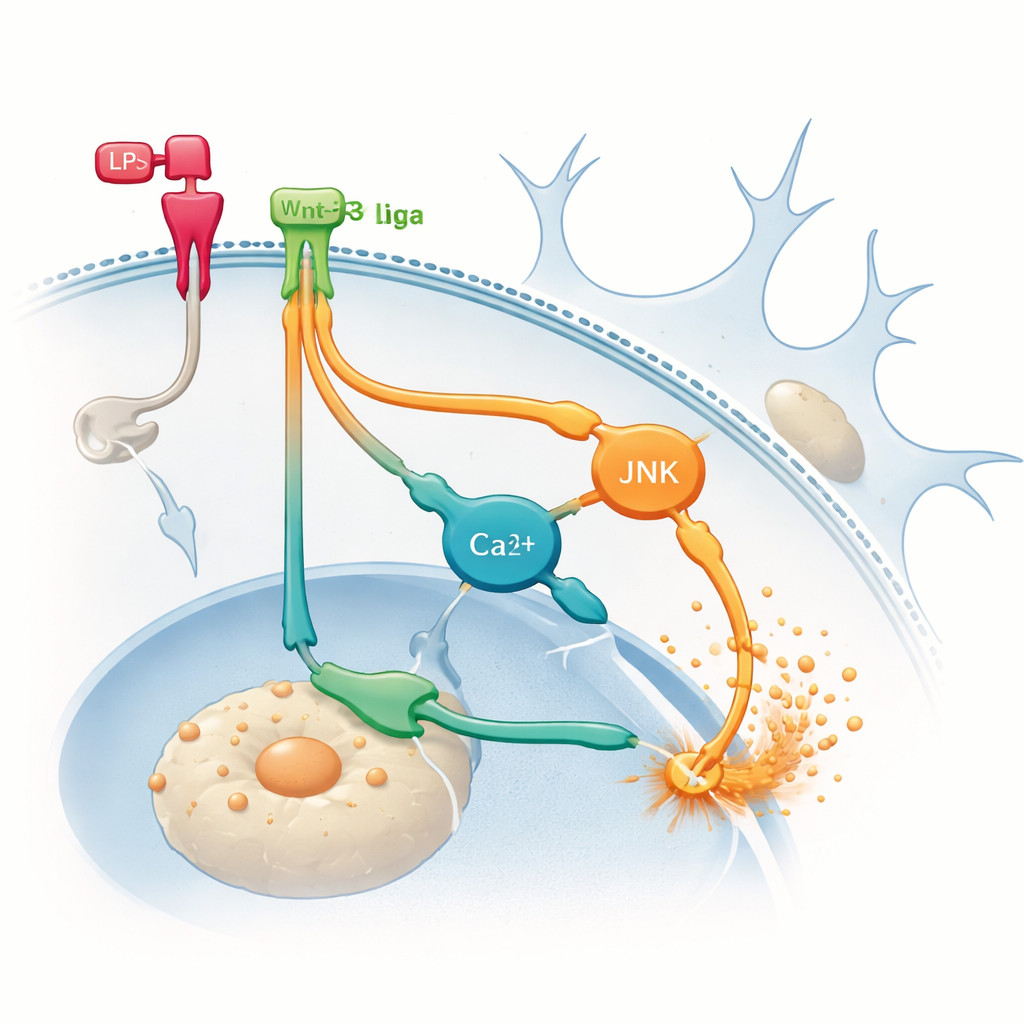
Alevleri körükleyen gizli yollar
Fazladan iltihabın nereden geldiğini bulmak için ekip Wnt proteinlerinin kullanabileceği alternatif kanonik olmayan yollara yöneldi. Mikroglialar içinde iki sinyal dalını farmakolojik olarak bloke ettiler: biri JNK adlı bir proteini içeren dal, diğeri ise hücre içindeki kalsiyum düzeylerindeki değişikliklere bağlı olan dal. Bu dallardan herhangi birinin inhibisyonu, LPS ile indüklenen TNF‑α üretimini azalttı ve önemlisi, Wnt‑3a’nın TNF‑α’yı daha da artırmasını engelledi. Bu sonuçlar, mikroglialar zaten iltihaplı olduğunda Wnt‑3a’nın iltihap sinyallerini yatıştırmak yerine güçlendiren kanonik olmayan yollara ağırlık verebileceğini düşündürür. Başka bir deyişle, aynı haberci hücrenin başlangıç durumuna bağlı olarak farklı iç yollardan giderek çok farklı sonuçlar doğurabilir.
Parkinson modeliyle test
Araştırmacılar daha sonra mikroglialardaki bu Wnt‑3a davranışının canlı bir beyinde nöronlar üzerinde daha büyük etkilere dönüşüp dönüşmeyeceğini sordular. Farelerin beyin ventriküllerine doğrudan Wnt‑3a infüze ettiler; fareler aynı zamanda dopamin nöronlarına ve mikroglial aktivasyona benzer zarar veren toksin olan MPTP’yi aldı; bu, Parkinson benzeri hasarı modellemek için yaygın kullanılan bir yaklaşımdır. Beklendiği gibi, MPTP dopamin nöronlarının sayısını azalttı ve hareket için kritik bir orta beyin bölgesinde mikroglia sayısını artırdı. Ancak ekstra Wnt‑3a, araç (vehicle) verilen hayvanlarla karşılaştırıldığında nöron kaybını daha da kötüleştirmedi veya mikroglia sayısını anlamlı şekilde değiştirmedi. Bu karmaşık in vivo ortamda Wnt‑3a, çalışılan zaman diliminde toksinin zararlı etkilerini ne kurtardı ne de belirgin şekilde artırdı.
Gelecek tedaviler için ne anlama geliyor
Genel olarak, çalışma Wnt‑3a’nın beyin iltihabı için basit bir açma‑kapama düğmesi olmadığını gösteriyor. Sakin mikroglialarda etkisi azdır, ancak zaten iltihaplı hücrelerde klasik β‑katenin yolundan bağımsız olarak kanonik olmayan sinyal yollarıyla TNF‑α salımını seçici olarak artırabilir. Aynı zamanda, Parkinson benzeri bir fare modelinde Wnt‑3a eklemek kısa vadede dopamin nöronlarını açıkça korumadı veya daha da zarar vermedi. Gelecekte tedavi geliştirmekle ilgilenenler için ana mesaj, Wnt sinyalizasyonunu hedeflemenin hücresel bağlamın dikkatli şekilde değerlendirilmesini gerektirdiğidir. Wnt‑3a veya ilişkili moleküllere dayanan tedaviler bazı durumlarda yardımcı olabilir, ancak istemeden zararlı iltihabı şiddetlendirirlerse başka durumlarda ters etki yapabilirler.
Atıf: Federici, G., Stayte, S., Rentsch, P. et al. Wnt-3a exacerbates production of TNF-α in LPS stimulated microglia independent of the β-catenin canonical pathway. Sci Rep 16, 8222 (2026). https://doi.org/10.1038/s41598-026-37653-1
Anahtar kelimeler: beyin iltihabı, mikroglia, Wnt sinyalizasyonu, Parkinson hastalığı, TNF-alfa